河北省沧衡八校联盟2021-2022学年高一上学期期中考试化学试题
试卷更新日期:2022-07-01 类型:期中考试
一、单选题
-
1. “碳达峰”“碳中和”成为全国两会的热词.下列有关12C和14C的说法中正确的是( )A、12C和14C的质子数相同,互称为同位素 B、12C和14C的质量数相同,互称为同位素 C、12C和14C的质子数相同,是同一种核素 D、12C和14C的核外电子数相同,中子数不同,不能互称为同位素2. 下列反应不属于氧化还原反应的是( )A、 B、 C、 D、3. 分类法是学习和研究化学的一种常用的科学方法,下列分类合理的是( )A、石灰石、石灰水、生石灰的主要成分分别属于碱、盐、氧化物 B、金属氧化物一定是碱性氧化物,非金属氧化物一定是酸性氧化物 C、根据化学反应中是否有电子的得失或偏移,可将化学反应分为氧化还原反应和非氧化还原反应 D、根据分散系是否可产生丁达尔效应可将分散系分为溶液、胶体和浊液4. 某同学在用某固体物质做焰色反应实验时,观察到焰色为黄色,下列有关说法错误的是( )A、该固体物质可能为钠盐 B、实验用的铂丝可用铜丝代替 C、若透过蓝色钴玻璃观察到有紫色,则说明该固体物质中还含有K元素 D、铂丝使用前需要先用盐酸洗涤,再在酒精灯火焰上灼烧至火焰呈无色,方可使用5. 下列试剂瓶可用于盛放新制氯水的是( )A、无色广口瓶 B、无色细口瓶 C、棕色细口瓶 D、棕色广口瓶6. 下列物质在水溶液中的电离方程式书写正确的是( )A、 B、 C、 D、7. 相同质量的和下列关系正确的是( )A、含氢原子个数比为 B、分子数之比为 C、含氢元素质量比为 D、原子总数之比为8. 下列有关含氯化合物的说法错误的是( )A、将固体加入新制氯水中,有无色气泡生成 B、可用“84”消毒液对图书馆桌椅消毒 C、可以用pH试纸测定新制氯水的pH D、漂白粉在空气中易发生化学反应而变质9. 下列有关物质的量浓度的说法正确的是( )A、将4g NaOH溶解在1L水中,可以得到的NaOH溶液 B、将的NaOH溶液分成两等份,其物质的量浓度变为原来的一半 C、将的NaOH溶液分成两等份,其溶质的物质的量变为原来的一半 D、向50mL NaOH溶液中加入50mL水,可以得到的NaOH溶液10. 下列实验装置不能达到相应实验目的的是( )
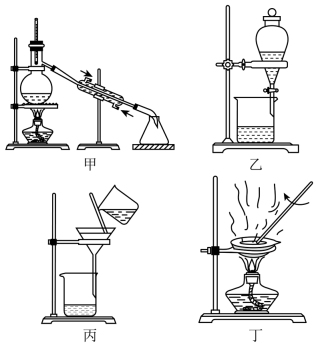 A、利用图甲装置分离乙醇和水 B、利用图乙装置分离植物油和水的混合物 C、利用图丙装置除去氯化钾溶液中的二氧化锰 D、利用图丁装置分离含有少量NaCl的碘的混合物11. 已知常温下,在溶液中发生如下反应:
A、利用图甲装置分离乙醇和水 B、利用图乙装置分离植物油和水的混合物 C、利用图丙装置除去氯化钾溶液中的二氧化锰 D、利用图丁装置分离含有少量NaCl的碘的混合物11. 已知常温下,在溶液中发生如下反应:①
②
③
由此推断下列说法错误的是( )
A、反应可以进行 B、X元素在反应③中被氧化,在反应①中被还原 C、氧化性由强到弱的顺序是 D、还原性由强到弱的顺序是12. 已知是阿伏加德罗常数的值。下列说法正确的是( )A、常温常压下,1.6g由和组成的混合气体中含有氧原子数为 B、的溶液中,所含数目为 C、含2 mol HCl的浓盐酸与43.5g 反应,生成的分子数为 D、11.2L 与足量钠反应,转移的电子数目为13. 下列检验Cl-的方法正确的是( )A、向某溶液中滴加AgNO3溶液,若产生白色沉淀说明该溶液中有Cl- B、向某溶液中先滴加盐酸,再滴加AgNO3溶液,若产生白色沉淀,说明溶液中有Cl- C、向某溶液中先滴加AgNO3溶液,产生白色沉淀,再滴加盐酸,沉淀不消失,说明溶液中有Cl- D、向某溶液中滴加用HNO3酸化的AgNO3溶液,若产生白色沉淀,说明溶液中有Cl-二、多选题
-
14. 在下列反应中,HCl作还原剂的是( )A、 B、 C、 D、15. 下列说法正确的是( )A、某微粒核外电子排布为2、8、8结构,则该微粒一定是氩原子 B、最外层电子达到稳定结构的微粒一定为稀有气体 C、、、、都具有相同的电子层结构 D、某元素原子的最外层只有2个电子,则该元素可能是非金属元素
三、综合题
-
16. 观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题。
 (1)、上述结构示意图中,表示离子的是(填离子符号),表示原子的是(填原子符号)。(2)、B、C、E三种粒子中性质最稳定的是(填粒子符号,下同),最容易失去电子的是 , 最容易得到电子的是。(3)、写出1~18号元素中符合下列条件的原子(或离子)的微粒符号,并画出其结构示意图。
(1)、上述结构示意图中,表示离子的是(填离子符号),表示原子的是(填原子符号)。(2)、B、C、E三种粒子中性质最稳定的是(填粒子符号,下同),最容易失去电子的是 , 最容易得到电子的是。(3)、写出1~18号元素中符合下列条件的原子(或离子)的微粒符号,并画出其结构示意图。①某元素原子的最外层电子数等于次外层电子数的2倍:。
②某元素原子L层上的电子数为K层的一半:。
③某元素原子得到2个电子后形成电子总数与氩原子的电子总数相同的离子:。
17. 对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可替代的。(1)、Ⅰ.现有以下物质:①胶体 ② ③稀硫酸 ④新制氯水 ⑤ ⑥以上物质中属于混合物的是(填序号,下同),属于电解质的是。
(2)、向含⑥的溶液中通入过量的⑤,写出发生反应的化学方程式:。(3)、Ⅱ.虽然分类的方法不同,但四种基本反应类型和氧化还原反应之间也存在着一定的关系。分解反应、氧化还原反应和化合反应三者之间的关系如图,下列有关说法正确的是____(填标号)。
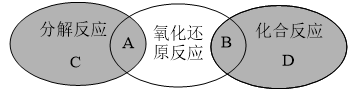 A、既属于分解反应又是氧化还原反应,例如: B、既属于化合反应,又是氧化还原反应,例如: C、属于分解反应,但不是氧化还原反应,例如: D、属于化合反应,但不是氧化还原反应,例如:(4)、高铁的快速发展方便了人们的出行,工业上利用铝热反应焊接钢轨间的缝隙,反应的化学方程式为 , 其中Al____(填标号)。A、是氧化剂 B、是还原剂 C、既是氧化剂又是还原剂 D、既不是氧化剂又不是还原剂(5)、氮化铝(AlN)具有耐高温、抗冲击、导热性好的优良性质广泛应用于电子工业陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成: , 请用双线桥法在化学方程式上标出该反应中电子转移的方向和数目: , 反应中被还原的元素为(填元素符号)。18. 根据所学知识,回答下列问题:(1)、0.5mol 的质量为g;200mL含个的溶液中溶质的物质的量浓度为 , 溶质的物质的量为mol。(2)、4.6g含有的中子的物质的量为mol。(3)、用的NaOH溶液吸收0.1mol 制取简易消毒液,发生反应的化学方程式为 , 若恰好被完全吸收,消耗NaOH溶液的体积为mL。(4)、某学生欲用的浓盐酸和蒸馏水配制500mL物质的量浓度为的稀盐酸。
A、既属于分解反应又是氧化还原反应,例如: B、既属于化合反应,又是氧化还原反应,例如: C、属于分解反应,但不是氧化还原反应,例如: D、属于化合反应,但不是氧化还原反应,例如:(4)、高铁的快速发展方便了人们的出行,工业上利用铝热反应焊接钢轨间的缝隙,反应的化学方程式为 , 其中Al____(填标号)。A、是氧化剂 B、是还原剂 C、既是氧化剂又是还原剂 D、既不是氧化剂又不是还原剂(5)、氮化铝(AlN)具有耐高温、抗冲击、导热性好的优良性质广泛应用于电子工业陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成: , 请用双线桥法在化学方程式上标出该反应中电子转移的方向和数目: , 反应中被还原的元素为(填元素符号)。18. 根据所学知识,回答下列问题:(1)、0.5mol 的质量为g;200mL含个的溶液中溶质的物质的量浓度为 , 溶质的物质的量为mol。(2)、4.6g含有的中子的物质的量为mol。(3)、用的NaOH溶液吸收0.1mol 制取简易消毒液,发生反应的化学方程式为 , 若恰好被完全吸收,消耗NaOH溶液的体积为mL。(4)、某学生欲用的浓盐酸和蒸馏水配制500mL物质的量浓度为的稀盐酸。①该学生需要量取mL上述浓盐酸进行配制。
②某同学观察液面时如图所示,对所配溶液的浓度将有何影响?(填“偏高”、“偏低”或“无影响”,下同)。

③若出现如下情况,对所配溶液的浓度将有何影响?
a.没有进行洗涤操作;;
b.加蒸馏水时不慎超过了刻度线:。
19. 制取无水氯化铜的实验装置如图所示(部分夹持装置已省略)。请回答下列问题: (1)、写出圆底烧瓶中发生反应的化学方程式:。(2)、C瓶中的试剂是 , 其作用是。(3)、装置A和装置D处均需要加热,则应该先加热的是(填“A”或“D”)处,其原因是。装置D中发生反应的化学方程式是 , 反应现象是。(4)、装置D导管口处棉花的作用是;干燥管E中盛有碱石灰(CaO和NaOH的混合物),其作用是。
(1)、写出圆底烧瓶中发生反应的化学方程式:。(2)、C瓶中的试剂是 , 其作用是。(3)、装置A和装置D处均需要加热,则应该先加热的是(填“A”或“D”)处,其原因是。装置D中发生反应的化学方程式是 , 反应现象是。(4)、装置D导管口处棉花的作用是;干燥管E中盛有碱石灰(CaO和NaOH的混合物),其作用是。