江苏省淮安市2022届高三下学期5月模拟测试化学试题
试卷更新日期:2022-06-23 类型:高考模拟
一、单选题
-
1. 2022年4月16日,神舟十三号载人飞船返回舱在东风着陆场顺利着陆。飞船的燃料为偏二甲肼(C2H8N2),发射时发生的反应为:C2H8N2+2N2O43N2+2CO2+4H2O,下列说法正确的是( )A、偏二甲肼在反应中作还原剂 B、燃烧时吸收大量的热 C、CO2的大量排放会导致酸雨 D、N2O4属于酸性氧化物2. 工业上利用MgCl2•6H2O+6SOCl2MgCl2+6SO2↑+12HCl↑制备无水MgCl2。下列说法正确的是( )A、SO2为非极性分子 B、MgCl2中既含离子键又含共价键 C、H2O的电子式为
 D、基态O原子的电子排布式为1s22s22p4
3. 下列由废铁屑制取无水Fe2(SO4)3的实验原理与装置不能达到实验目的的是( )
D、基态O原子的电子排布式为1s22s22p4
3. 下列由废铁屑制取无水Fe2(SO4)3的实验原理与装置不能达到实验目的的是( ) A、用装置甲除去废铁屑表面的油污 B、用装置乙溶解废铁屑制Fe2(SO4)3 C、用装置丙过滤得到Fe2(SO4)3溶液 D、用装置丁蒸干溶液获得Fe2(SO4)34. 下列关于氯及其化合物的性质与用途具有对应关系的是( )A、Cl2易液化,可用于生产盐酸 B、ClO2有强氧化性,可用于自来水消毒 C、CCl4难溶于水,可用作灭火剂 D、HCl极易溶于水,可用于检验NH35. 短周期主族元素X、Y、Z、W的原子序数依次增大,X原子2p轨道上有3个电子,Z是元素周期表中电负性最大的元素,W与Y同主族。下列说法正确的是( )A、原子半径:r(W)>r(Z)>r(Y)>r(X) B、X氧化物的水化物是一定是强酸 C、Y的第一电离能比同周期相邻元素小 D、W的简单气态氢化物的稳定性比Y的强6. 如NOx是大气中主要的污染物。大气中过量的NOx和水体中过量的NH、NO、NO均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为2NO(g)+2CO(g)2CO2(g)+N2(g) △H=-746.5kJ·mol-1];也可将水体中的NO、NO转化为N2。下列有关NO2、NO、NO的说法正确的是( )A、NO的空间构型为V形 B、NO2与NO中的键角相同 C、NO2易溶于水是因NO2能与H2O形成分子间氢键 D、配位离子[Fe(NO)]2+中NO提供空轨道7. 如NOx是大气中主要的污染物。大气中过量的NOx和水体中过量的NH、NO、NO均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为2NO(g)+2CO(g)2CO2(g)+N2(g) △H=-746.5kJ·mol-1];也可将水体中的NO、NO转化为N2。在指定条件下,下列选项所示的物质间转化不能实现的是( )A、N2(g)NO(g) B、NO(g)NaNO2(aq) C、NH3(g)N2(g) D、NO2(g)HNO3(aq)8. 如NOx是大气中主要的污染物。大气中过量的NOx和水体中过量的NH、NO、NO均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为 △H=-746.5kJ·mol-1];也可将水体中的NO、NO转化为N2。对于反应 , 下列说法正确的是( )A、该反应在任何条件下都能自发进行 B、反应的平衡常数可表示为K= C、使用高效的催化剂可以降低反应的焓变 D、其它条件不变,增大的值,NO的转化率下降9. 以含钴废渣(主要成分为CoO和Co2O3 , 含少量Al2O3和ZnO)为原料制备CoCO3的工艺流程如图:
A、用装置甲除去废铁屑表面的油污 B、用装置乙溶解废铁屑制Fe2(SO4)3 C、用装置丙过滤得到Fe2(SO4)3溶液 D、用装置丁蒸干溶液获得Fe2(SO4)34. 下列关于氯及其化合物的性质与用途具有对应关系的是( )A、Cl2易液化,可用于生产盐酸 B、ClO2有强氧化性,可用于自来水消毒 C、CCl4难溶于水,可用作灭火剂 D、HCl极易溶于水,可用于检验NH35. 短周期主族元素X、Y、Z、W的原子序数依次增大,X原子2p轨道上有3个电子,Z是元素周期表中电负性最大的元素,W与Y同主族。下列说法正确的是( )A、原子半径:r(W)>r(Z)>r(Y)>r(X) B、X氧化物的水化物是一定是强酸 C、Y的第一电离能比同周期相邻元素小 D、W的简单气态氢化物的稳定性比Y的强6. 如NOx是大气中主要的污染物。大气中过量的NOx和水体中过量的NH、NO、NO均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为2NO(g)+2CO(g)2CO2(g)+N2(g) △H=-746.5kJ·mol-1];也可将水体中的NO、NO转化为N2。下列有关NO2、NO、NO的说法正确的是( )A、NO的空间构型为V形 B、NO2与NO中的键角相同 C、NO2易溶于水是因NO2能与H2O形成分子间氢键 D、配位离子[Fe(NO)]2+中NO提供空轨道7. 如NOx是大气中主要的污染物。大气中过量的NOx和水体中过量的NH、NO、NO均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为2NO(g)+2CO(g)2CO2(g)+N2(g) △H=-746.5kJ·mol-1];也可将水体中的NO、NO转化为N2。在指定条件下,下列选项所示的物质间转化不能实现的是( )A、N2(g)NO(g) B、NO(g)NaNO2(aq) C、NH3(g)N2(g) D、NO2(g)HNO3(aq)8. 如NOx是大气中主要的污染物。大气中过量的NOx和水体中过量的NH、NO、NO均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N2[反应为 △H=-746.5kJ·mol-1];也可将水体中的NO、NO转化为N2。对于反应 , 下列说法正确的是( )A、该反应在任何条件下都能自发进行 B、反应的平衡常数可表示为K= C、使用高效的催化剂可以降低反应的焓变 D、其它条件不变,增大的值,NO的转化率下降9. 以含钴废渣(主要成分为CoO和Co2O3 , 含少量Al2O3和ZnO)为原料制备CoCO3的工艺流程如图:
下列说法正确的是( )
A、酸浸时可采用高温提高酸浸速率 B、除铝时加入Na2CO3溶液过滤后所得滤渣是Al2(CO3)3 C、萃取时萃取剂总量一定,分多次加入萃取比一次加入萃取效果更好 D、沉钴时将含Co2+的溶液缓慢滴加到Na2CO3溶液中,可提高CoCO3的产率10. 有机物Z为是合成某药物的重要中间体,可由下列反应制得。
下列有关化合物X、Y和Z的说法正确的是( )
A、1molX中含有6mol碳氧σ键 B、Y分子含有三种官能团 C、X、Y可用酸性KMnO4溶液鉴别 D、Z分子与足量H2加成后的产物中含有3个手性碳原子11. 检验淀粉水解,实验步骤如下:步骤1:向试管中加入4mL淀粉溶液,再加入少量稀硫酸,加热4分钟,冷却后将溶液分装在两支试管中;
步骤2:向一支试管中滴加几滴碘水,观察现象;
步骤3:向另一支试管中先加入烧碱溶液中和,再加入银氨溶液,水浴加热煮沸,观察现象。
下列说法错误的是( )
 A、步骤1中加入稀硫酸可以加快淀粉水解速率 B、步骤2中溶液变蓝色,说明淀粉没有完全水解 C、步骤3中水浴加热后观察到有光亮的银镜,说明淀粉已经水解 D、碘晶胞如图所示,则碘分子的配位数是812. 间接电解法可对大气污染物NO进行无害化处理,其工作原理如图所示,质子膜允许H+和H2O通过。下列有关说法正确的是( )
A、步骤1中加入稀硫酸可以加快淀粉水解速率 B、步骤2中溶液变蓝色,说明淀粉没有完全水解 C、步骤3中水浴加热后观察到有光亮的银镜,说明淀粉已经水解 D、碘晶胞如图所示,则碘分子的配位数是812. 间接电解法可对大气污染物NO进行无害化处理,其工作原理如图所示,质子膜允许H+和H2O通过。下列有关说法正确的是( ) A、电解后右侧Na2SO4溶液浓度不变 B、电极I的电极反应式为:2HSO+2e-=S2O+2OH- C、电解过程中电极II附近溶液的pH减小 D、工作时有0.4molH+通过质子膜时可处理4.48LNO13. 室温下,Ka1(H2SO3)=10-1.81 , Ka1(H2SO3)=10-6.99。室温下通过下列实验探究Na2SO3、NaHSO3溶液的性质。
A、电解后右侧Na2SO4溶液浓度不变 B、电极I的电极反应式为:2HSO+2e-=S2O+2OH- C、电解过程中电极II附近溶液的pH减小 D、工作时有0.4molH+通过质子膜时可处理4.48LNO13. 室温下,Ka1(H2SO3)=10-1.81 , Ka1(H2SO3)=10-6.99。室温下通过下列实验探究Na2SO3、NaHSO3溶液的性质。实验1:测定某浓度的NaHSO3溶液的pH,测得pH为5.2。
实验2:向0.10mol·L-1NaHSO3溶液中加氨水至pH=7。
实验3:向0.10mol·L-1Na2SO3溶液中滴几滴0.10mol·L-1FeCl3溶液,再滴加KSCN溶液,溶液不变红。
实验4:向0.10mol·L-1Na2SO3溶液中加入BaO2固体,有气体产生,同时有白色沉淀。
下列说法错误的是( )
A、实验1的溶液中:=10-1.6 B、实验2得到的溶液中有 C、实验3中加FeCl3溶液的离子方程式为: D、实验4的上层清液中有c(SO)•c(Ba2+)=Ksp(BaSO3),产生的气体中一定有SO214. 某科研小组研究臭氧脱除SO2和NO工艺,反应原理及反应热、活化能数据如下:反应I:NO(g)+O3(g)NO2(g)+O2(g) △H1=-200.9kJ·mol-1 Ea1=+3.2kJ·mol-1
反应II:SO2(g)+O3(g)SO3(g)+O2(g) △H2=-241.6kJ·mol-1 Ea2=+58kJ·mol-1
已知该体系中臭氧发生分解反应:2O3(g)3O2(g)。
向容积一定的反应器中充入含1.0molNO、1.0molSO2的模拟烟气和2.0molO3 , 改变温度,反应相同时间t后体系中NO和SO2的转化率如图所示,下列说法错误的是( )
 A、Q点一定为平衡状态点 B、相同温度下NO的转化率远高于SO2 , 主要原因是Ea1小于Ea2 C、300℃后,SO2转化率接近于零且不再变化,主要原因是O3分解 D、其他条件不变,扩大反应器的容积可以降低NO和SO2单位时间内的转化率
A、Q点一定为平衡状态点 B、相同温度下NO的转化率远高于SO2 , 主要原因是Ea1小于Ea2 C、300℃后,SO2转化率接近于零且不再变化,主要原因是O3分解 D、其他条件不变,扩大反应器的容积可以降低NO和SO2单位时间内的转化率二、综合题
-
15. 钒被称为“工业味精”、“工业维生素”,在发展现代工业、国防等方面发挥着重要的作用。一种用废钒催化剂(含V2O5、少量Al2O3、Fe2O3)制取V2O5的工艺流程如图:

已知:溶液中四种含钒微粒的存在形式和颜色:V2+紫色,V3+绿色,VO2+蓝色,VO黄色。回答下列问题:
(1)、“酸浸、还原”时,V2O5被还原为VO2+ , 该反应的离子方程式为。(2)、“碱浸、氧化”过程中会生成VO2+ , 在20.00mL0.1mol·L-1VO溶液中,加入0.195g锌粉,恰好完全反应,则所得溶液的颜色为。(3)、“操作1”包括转沉、沉钒和过滤等步骤。①“转沉”过程中先加石灰乳、再加(NH4)2CO3生成(NH4)3VO4。已知:Ksp(CaCO3)=m,Ksp[Ca3(VO4)2]=n;则反应Ca3(VO4)2(s)+3CO(aq)2VO(aq)+3CaCO3(s)的平衡常数为(用含m、n的代数式表示)。
②“沉钒”时加NH4Cl生成NH4VO3 , 沉钒率随温度的变化如图1所示,温度高于80℃沉钒率下降的原因可能是。
 (4)、有氧条件下,在V2O5的催化作用下NO可被NH3还原为N2。反应机理如图2所示。NO、NH3在有氧条件下的总反应化学方程式是。
(4)、有氧条件下,在V2O5的催化作用下NO可被NH3还原为N2。反应机理如图2所示。NO、NH3在有氧条件下的总反应化学方程式是。 (5)、测定产品中V2O5的纯度:称取2.000g产品用硫酸溶解得(VO2)2SO4溶液,加入50.00mL0.5000mol·L-1(NH4)2Fe(SO4)2溶液,发生的反应为VO+2H++Fe2+=VO2++Fe3++H2O,再用0.2000mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为5.00mL。已知MnO被还原为Mn2+ , 假设杂质不参与反应。则产品中V2O5的质量分数是。(写出计算过程)。16. 实验室研究从炼铜烟灰(主要成分为CuO、Cu2O、ZnO、PbO等)中分别回收铜、铅元素的流程如图:
(5)、测定产品中V2O5的纯度:称取2.000g产品用硫酸溶解得(VO2)2SO4溶液,加入50.00mL0.5000mol·L-1(NH4)2Fe(SO4)2溶液,发生的反应为VO+2H++Fe2+=VO2++Fe3++H2O,再用0.2000mol·L-1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为5.00mL。已知MnO被还原为Mn2+ , 假设杂质不参与反应。则产品中V2O5的质量分数是。(写出计算过程)。16. 实验室研究从炼铜烟灰(主要成分为CuO、Cu2O、ZnO、PbO等)中分别回收铜、铅元素的流程如图:
已知:Cu+在酸性环境中能转化为Cu和Cu2+。
(1)、“酸浸”过程中,金属元素均由氧化物转化为硫酸盐,其中Cu2O生成CuSO4的化学方程式为。Cu2O粉末和Cu粉末外观均为红色,设计实验证明实验室制得的Cu粉中是否混有Cu2O。(2)、“置换”过程中,铁屑加入初期反应速率迅速加快,其可能原因有:①反应放热,温度升高,速率加快,②;铁屑完全消耗后,铜的产率随时间延长而下降,其可能的原因为。(3)、已知:PbSO4、PbCl2均难溶于水,25℃时,PbSO4(s)+2Cl-(aq)PbCl2(s)+SO(aq)。一定条件下,在不同浓度的NaCl溶液中,温度对铅浸出率的影响、PbCl2的溶解度曲线分别如图所示。
结合题给信息,请补充完整利用酸浸后的滤渣制备PbCl2晶体的实验方案:取一定量的滤渣,。(可选用的试剂有:蒸馏水,5mol·L-1NaCl溶液,1mol·L-1NaCl溶液,NaCl固体)
17. 化合物G是一种重要的合成中间体,其合成路线如图: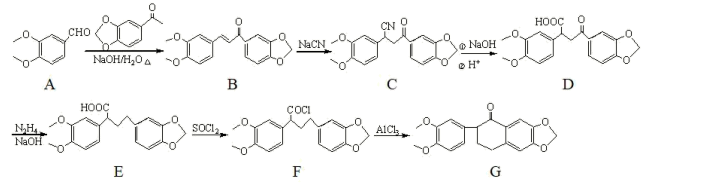 (1)、A的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式。
(1)、A的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式。①遇FeCl3溶液显色
②能发生水解反应和银镜反应
③分子中不同化学环境的氢原子个数比是1∶1∶2∶6
(2)、A→B的转化分两步完成,该过程可表示为A→X→B,则X的结构简式为。(3)、D→E的反应类型为。(4)、G分子中采取sp2杂化的碳原子数目是。(5)、设计以 、CH3CHO为原料制备
、CH3CHO为原料制备 的合成路线。(无机试剂和有机溶剂任用,合成路线示例见本题题干)。 18. 硫化氢的转化是资源利用和环境保护的重要研究课题。(1)、工业上将含有硫化物的废水(以H2S、HS-、S2-的形式存在)引入氧化池,加入高锰酸钾溶液氧化。已知高锰酸钾在酸性条件下的还原产物为Mn2+ , 碱性条件下的为MnO2。
的合成路线。(无机试剂和有机溶剂任用,合成路线示例见本题题干)。 18. 硫化氢的转化是资源利用和环境保护的重要研究课题。(1)、工业上将含有硫化物的废水(以H2S、HS-、S2-的形式存在)引入氧化池,加入高锰酸钾溶液氧化。已知高锰酸钾在酸性条件下的还原产物为Mn2+ , 碱性条件下的为MnO2。①pH>7时高锰酸钾将废水中的硫化物氧化为S,该反应的离子方程式为。
②研究发现:其他条件相同时,废水呈酸性时硫化物的去除率明显大于呈碱性时去除率,则可能的原因。
(2)、常温下,H2S的Ka1=1.3×10-7、Ka2=7.0×10-15 , Ksp(MnS)=1.4×10-15。向含有0.0020mol·L-1Mn2+废水中通入一定量的H2S,当溶液的pH=a、c(HS-)=1.0×10-4mol·L-1时,Mn2+开始沉淀,则a=。(3)、表面喷淋水的活性炭可用于吸附氧化H2S,其原理可用图1表示。其它条件不变时,水膜的酸碱性与厚度会影响H2S的去除率。
①适当增大活性炭表面的水膜pH,H2S的氧化去除率增大的原因是。
②若水膜过厚,H2S的氧化去除率减小的原因是。
(4)、甲硫醇是一种恶臭、有毒物质。生物法去除甲硫醇反应为2CH3SH+7O2=2CO2+2H2O+2H2SO4。研究表明,在H2S存在条件下,可改变甲硫醇(用 表示)生物降解途径,反应历程如图2所示,请用简洁的语言描述图中甲硫醇的降解过程。
表示)生物降解途径,反应历程如图2所示,请用简洁的语言描述图中甲硫醇的降解过程。