湖南省郴州市2020-2021学年高二下学期期末考试化学试题
试卷更新日期:2022-06-22 类型:期末考试
一、单选题
-
1. 化学与生活、科技等密切相关。下列说法正确的是( )A、N95口罩所使用的聚丙烯材料属于合成纤维,是纯净物 B、陈薇院士团队开发的腺病毒载体新冠疫苗(Ad5-nCoV疫苗)性质稳定,该疫苗需在高温下保存 C、屠呦呦用乙醚从青蒿中提取出对治疗疟疾有特效的青蒿素,该过程包括萃取操作 D、华为5G芯片巴龙5000的主要材料是二氧化硅2. 下列有关化学用语表示正确的是( )A、葡萄糖和果糖的实验式: B、的电子式:
 C、对硝基苯酚的结构简式:
C、对硝基苯酚的结构简式: D、四氯化碳分子的比例模型:
D、四氯化碳分子的比例模型: 3. 下列实验操作或相关说法合理的是( )
3. 下列实验操作或相关说法合理的是( )A
B
C
D



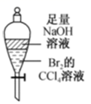
混合浓硫酸和乙醇
验证SO2的漂白性
蒸干MgCl2溶液制取无水MgCl2
充分振荡后下层为无色
A、A B、B C、C D、D4. 下列物质性质与用途对应关系正确的是( )性质
用途
A
具有氧化性
漂白纸浆
B
溶液呈弱碱性
防火材料
C
溶液具有氧化性
蚀刻铜制电路板时作为“腐蚀液”
D
具有弱酸性
蚀刻玻璃
A、A B、B C、C D、D5. 物质X的结构式如图所示,是一种高效低毒杀虫剂,有关物质X说法正确的是( ) A、分子式为 B、X最多能与氢气发生加成反应 C、可用溶液检验是否发生水解 D、能与溴水在铁作用下发生苯环上的取代反应6. 通常监测SO2含量是否达到排放标准的反应原理是SO2+H2O2+BaCl2=BaSO4↓+2HCl。NA表示阿伏加德罗常数的值,下列说法正确的是( )A、0.1molBaCl2晶体中所含微粒总数为0.1NA B、25℃时,pH=1的HCl溶液中含有H+的数目为0.1NA C、17gH2O2中含有非极性键数目为0.5NA D、生成2.33gBaSO4沉淀时,转移电子数目为0.01NA7. 下列实验设计及其对应的离子方程式均正确的是( )A、酸性溶液与酒精反应: B、与反应制备: C、将氯气溶于水制备次氯酸: D、用浓盐酸酸化的溶液与反应,证明具有还原性:8. 往1.0 mol·L-1KI溶液中加入固体I2 , 发生反应:I2(aq)+I- (aq) I3-(aq) △H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示。已知反应第一次达到平衡时用时10s,则下列说法正确的是( )
A、分子式为 B、X最多能与氢气发生加成反应 C、可用溶液检验是否发生水解 D、能与溴水在铁作用下发生苯环上的取代反应6. 通常监测SO2含量是否达到排放标准的反应原理是SO2+H2O2+BaCl2=BaSO4↓+2HCl。NA表示阿伏加德罗常数的值,下列说法正确的是( )A、0.1molBaCl2晶体中所含微粒总数为0.1NA B、25℃时,pH=1的HCl溶液中含有H+的数目为0.1NA C、17gH2O2中含有非极性键数目为0.5NA D、生成2.33gBaSO4沉淀时,转移电子数目为0.01NA7. 下列实验设计及其对应的离子方程式均正确的是( )A、酸性溶液与酒精反应: B、与反应制备: C、将氯气溶于水制备次氯酸: D、用浓盐酸酸化的溶液与反应,证明具有还原性:8. 往1.0 mol·L-1KI溶液中加入固体I2 , 发生反应:I2(aq)+I- (aq) I3-(aq) △H;I-的物质的量浓度c(I-)随温度T的变化曲线如图所示。已知反应第一次达到平衡时用时10s,则下列说法正确的是( ) A、该反应的△H>0 B、a、c两点对应的I-反应速率相等 C、b点时0~10s I-的平均反应速率为0.04mol·L-1·s-1 D、d点时该反应在对应温度下处于平衡状态9. 锂-空气动力电池存储的能量是目前常规电池的数倍,放电原理如图(隔膜只允许通过)。下列关于锂-空气电池的有关说法正确的是( )
A、该反应的△H>0 B、a、c两点对应的I-反应速率相等 C、b点时0~10s I-的平均反应速率为0.04mol·L-1·s-1 D、d点时该反应在对应温度下处于平衡状态9. 锂-空气动力电池存储的能量是目前常规电池的数倍,放电原理如图(隔膜只允许通过)。下列关于锂-空气电池的有关说法正确的是( ) A、放电时负极反应式 B、充电时的电池反应为 C、放电时移向有机电解液 D、充电时,“充电专用电极”接外电源的负极10. 元素铬()的几种化合物存在下列转化关系,下列判断错误的是( )
A、放电时负极反应式 B、充电时的电池反应为 C、放电时移向有机电解液 D、充电时,“充电专用电极”接外电源的负极10. 元素铬()的几种化合物存在下列转化关系,下列判断错误的是( )固体
A、反应①表明有酸性氧化物的性质 B、反应②的离子方程式为 C、反应③加碱可使溶液由橙红色变黄色 D、反应①②③中铬元素的化合价均发生了变化11. 短周期主族元素X、Y、Z、W的原子序数依次增大。X的气态氢化物能与其最高价含氧酸化合成盐,Z是同周期元素中原子半径最大的元素,Y和W同主族且二者可形成和两种物质。下列说法正确的是( )A、简单离子半径: B、氢化物的沸点: C、Y和Z两种元素形成的化合物中可能存在共价键 D、Y、Z、W三种元素只能形成两种化合物12. 25℃时,将的溶液加水稀释,混合溶液中与与的关系如图所示。下列说法正确的是( ) A、 B、P、Q点对应的稀释程度: C、若将溶液无限稀释,溶液中 D、25℃时,加入适量可使P点移至W点
A、 B、P、Q点对应的稀释程度: C、若将溶液无限稀释,溶液中 D、25℃时,加入适量可使P点移至W点二、多选题
-
13. 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
选项
实验操作和现象
结论
A
向某溶液中先滴加稀硝酸,再滴加溶液,出现白色沉淀
该溶液中一定含有
B
向溶液中滴加少量溶液,再滴加几滴淀粉溶液,溶液变蓝色
的氧化性比的强
C
向、的混合溶液中滴加少量溶液,有黑色沉淀生成
D
用试纸测得的溶液与的溶液的分别为3、5
酸性:
A、A B、B C、C D、D14. 一定温度下,向2L恒容容器中充入A和B,发生反应 , 经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确的是( )0
5
15
25
35
1.0
0.85
0.81
0.80
0.80
A、前5s的平均反应速率 B、由题目信息可知,正反应为放热反应 C、保持温度不变,起始时向容器中充入A、B和C,反应达平衡前 D、保持温度不变,起始时向容器中充入C,达平衡时,C的转化率等于80%三、综合题
-
15. 电解精炼铜的阳极泥中含有、、、、、、等,从其中提取、、、的单质的流程如图所示,回答下列问题:
 (1)、粗铜中含有、两种元素的单质,但在阳极泥中几乎检测不到,原因是。(2)、已知阳极泥进行“硫酸化(隔绝空气)焙烧”,烟气中含有 , 等。
(1)、粗铜中含有、两种元素的单质,但在阳极泥中几乎检测不到,原因是。(2)、已知阳极泥进行“硫酸化(隔绝空气)焙烧”,烟气中含有 , 等。①写出“焙烧”过程中与浓硫酸反应的化学方程式:。
②将、通入水中即可生成单质硒,该反应的离子方程式为。
③实验室中将粗硒从溶液中分离出来的操作为。
(3)、用惰性电极电解“浸液”时,溶液中发生的总反应离子方程式为。(4)、“银电解”时,阳极材料是。(5)、上述流程中,可以循环利用的物质是(填写化学式)。16. 亚氯酸钠()是重要漂白剂,某化学实验小组设计如下实验探究亚氯酸钠的制备与性质。已知:①饱和溶液在低于38℃时析出 , 高于38℃时析出无水 , 温度高于60℃时,分解为和。②易溶于水。

回答下列问题:
(1)、仪器a的名称是。(2)、A装置中发生的主要反应的离子方程式为。(3)、装置C中混合溶液反应生成的化学方程式为。(4)、从装置C反应后的溶液获得晶体的操作步骤为:①减压,55℃蒸发至形成大量晶体;②趁热过滤;③用洗涤;④低于60℃干燥,得到成品。
(5)、设计实验检验所得晶体是否含有杂质 , 操作是:。(6)、测定产品中(相对分子质量:90.5)的纯度。准确称取3.00g样品,加入适量蒸馏水和过量的晶体,在酸性条件下发生反应:。将所得混合液稀释成待测溶液。用酸式滴定管量取待测溶液置于锥形瓶中,加入淀粉溶液作指示剂,用标准液滴定(已知:),滴定终点时的现象为 , 平行滴定3次,测得消耗标准溶液体积的平均用量为。所称取的样品中质量百分含量为。17. 碳、氮、硫及其化合物对生产、生活有重要的意义。
以与为原料可合成尿素[]。已知:①
②
③
(1)、写出和合成尿素和液态水的热化学方程式。(2)、高温下,与足量的碳在密闭容器中实现反应:。向容积为1L的恒容容器中加入和足量的碳,在不同温度下达到平衡时的物质的量浓度随温度的变化如图所示。则该反应为(填“放热”或“吸热”)反应;某温度下若向该平衡体系中再通入 , 达到新平衡后,体系中的百分含量(填“变大”、“变小”或“不变”)。 (3)、与能发生反应: 在固定体积的密闭容器中,使用某种催化剂,改变原料气配比进行多次实验(各次实验的温度可能相同,也可能不同),测定的平衡转化率。部分实验结果如图所示:
(3)、与能发生反应: 在固定体积的密闭容器中,使用某种催化剂,改变原料气配比进行多次实验(各次实验的温度可能相同,也可能不同),测定的平衡转化率。部分实验结果如图所示:
①当容器内(填标号)不再随时间的变化而改变时,反应达到平衡状态。
A.气体的压强
B.气体的平均摩尔质量
C.气体的密度
D.的体积分数
②如果要将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是。
③若A点对应实验中,(g)的起始浓度为 , 经过达到平衡状态,该时段化学反应速率。
④图中C、D两点对应的温度分别为℃和℃,通过计算判断(填“>”、“=”或“<”)。
18. (聚己二酸对苯二甲酸丁酯)可被微生物几乎完全降解,成为包装、医疗和衣用薄膜等领域的新兴材料,它可由聚合物和共聚制得,一种合成路线如下:
已知:;
回答下列问题:
(1)、①的反应类型为;D的官能团名称为。(2)、E的化学名称为。(3)、E中共面原子数目最多为。(4)、反应②的化学方程式为。(5)、M与G互为同系物,M的相对分子质量比G大14;N是M的同分异构体,写出同时满足以下条件的N的结构简式:(任写一种即可,不考虑立体异构)。Ⅰ、既能与发生显色反应,又能发生水解反应和银镜反应;
Ⅱ、与溶液反应时,N能消耗;
Ⅲ、核磁共振氢谱有五组峰,峰面积比为。
(6)、仿照上述流程,设计由丙烯和乙醇为主要原料制备的合成路线(其它无机试剂可任选)。