广西百色市靖西市2022年中考二模化学试题
试卷更新日期:2022-06-21 类型:中考模拟
一、单选题
-
1. 化学在生产、生活中应用广泛。下列变化属于化学变化的是( )A、大米酿酒 B、干冰升华 C、矿石粉碎 D、苹果榨汁2. 空气是一种重要的资源。下列有关空气的说法正确的是( )A、氮气约占空气质量的78% B、二氧化碳不是空气污染物 C、空气污染指数越高,空气质量越好 D、食品包装袋中充入氧气可延长食品的保质期3. 臭氧(O3)主要分布在距离地面10~25km的高空,能吸收大部分紫外线,保护地球生物。它属于( )A、氧化物 B、单质 C、化合物 D、混合物4. 下列实验基本操作,正确的是( )A、测溶液的酸碱度
 B、溶解粗盐
B、溶解粗盐 C、滴加液体
C、滴加液体 D、移走蒸发皿
D、移走蒸发皿 5. 餐桌上的饮品种类丰富,下列饮品中属于溶液的是( )A、酸奶 B、玉米糊 C、冰水 D、可乐6. 在化肥中,硝酸铵(NH4NO3)属于( )A、复合肥 B、钾肥 C、磷肥 D、氮肥7. 人体中化学元素含量的多少直接影响健康。人体缺乏下列哪种元素易导致贫血症( )A、铁 B、钙 C、锌 D、碘8. 中国明确提出“2030年实现碳达峰和2060年实现碳中和目标”,这也是中国对世界做出的庄严承诺。 下列措施不符合上述发展理念的是( )A、使用光伏发电 B、尽量使用庄稼秸秆做饭 C、大量植树造林 D、推广使用氢燃料汽车9. 下列有关说法正确的是( )A、化学反应的实质是分子的重新组合 B、人体所需的微量元素只能用药物补充 C、人体胃液正常的pH在0.9-1.5,如果出现异常,就会导致疾病 D、自来水厂在净化水的过起中,向水中加入明矾能除去水中的异味和色素10. 2022年北京冬奥会将于2月4日开幕,下列做法从微观角度解释不合理的是( )A、运动场上用水造冰——温度降低,分子停止运动 B、开幕式上舞台云雾——干冰升华,分子间隔发生改变 C、奥运村中日常消毒——消毒液挥发,分子在不断运动 D、天然气公交车出行——天然气燃烧,分子种类发生改变11. 用下图装置可验证空气中O2的含量。下列现象能表明O2含量的是( )
5. 餐桌上的饮品种类丰富,下列饮品中属于溶液的是( )A、酸奶 B、玉米糊 C、冰水 D、可乐6. 在化肥中,硝酸铵(NH4NO3)属于( )A、复合肥 B、钾肥 C、磷肥 D、氮肥7. 人体中化学元素含量的多少直接影响健康。人体缺乏下列哪种元素易导致贫血症( )A、铁 B、钙 C、锌 D、碘8. 中国明确提出“2030年实现碳达峰和2060年实现碳中和目标”,这也是中国对世界做出的庄严承诺。 下列措施不符合上述发展理念的是( )A、使用光伏发电 B、尽量使用庄稼秸秆做饭 C、大量植树造林 D、推广使用氢燃料汽车9. 下列有关说法正确的是( )A、化学反应的实质是分子的重新组合 B、人体所需的微量元素只能用药物补充 C、人体胃液正常的pH在0.9-1.5,如果出现异常,就会导致疾病 D、自来水厂在净化水的过起中,向水中加入明矾能除去水中的异味和色素10. 2022年北京冬奥会将于2月4日开幕,下列做法从微观角度解释不合理的是( )A、运动场上用水造冰——温度降低,分子停止运动 B、开幕式上舞台云雾——干冰升华,分子间隔发生改变 C、奥运村中日常消毒——消毒液挥发,分子在不断运动 D、天然气公交车出行——天然气燃烧,分子种类发生改变11. 用下图装置可验证空气中O2的含量。下列现象能表明O2含量的是( ) A、集气瓶中产生大量白烟 B、红磷燃烧一段时间后熄灭 C、烧杯中的水倒吸进入集气瓶 D、集气瓶中水面最终上升至1处12. 2021年12月9日,“天空课堂”在中国空间站精彩开讲。铁酸镍(化学式:NiFe2O4)可以将航天员呼出的废气转化为航天员需要的气体,而本身的质量和化学性质都不变化,NiFe2O4中若铁元素的化合价是+3价,则镍(Ni)元素的化合价是( )A、+2 B、+4 C、-1 D、-213. 燃烧是人们生活中重要的化学反应,我们既要利用燃烧,也要注意防灾减灾。下列有关燃烧、灭火与安全的说法,正确的是( )A、炒菜时油锅着火,可用水浇灭 B、加油站、矿井等场所要严禁烟火 C、高层楼房失火时,立即乘电梯下楼逃生 D、用燃着的火柴很难直接点燃煤,是因为煤不具有可燃性14. 下列有关实验现象的描述正确的是( )A、向少量氧化铜中加入稀硫酸,有气泡产生,黑色粉末逐渐消失,溶液变蓝 B、用粗砂纸打磨后的铝片放入硫酸铜溶液中,一段时间后,划痕处出现红色物质 C、细铁丝在氧气中燃烧,火星四射,生成红棕色固体 D、向滴有石蕊的稀盐酸中滴加氢氧化钠溶液至过量,溶液由蓝色变紫色再变红色15. “飞扬”冬奥,火炬采用的燃料是氢燃料,不是传统燃料丙烷,丙烷(X)完全燃烧的化学方程式为: , 丙烷(X)的化学式为( )A、C3H4 B、C3H8O C、C3H8 D、C3H6O216. 下列是生活中一些常见物质的近似pH,其中能使紫色石蕊溶液变蓝的是( )A、炉具清洁剂pH=13 B、牛奶pH=6.5 C、洁厕灵pH=1 D、纯净水pH=717. 下列物质中,不能与稀盐酸发生反应的是( )A、Fe2O3 B、Na2CO3 C、NaCl D、NaOH18. 下列各组物质在水溶液中能够共存,而且加入石蕊显红色的是( )A、NaOH、CuSO4、H2SO4 B、NaCl、Na2SO4、NaHCO3 C、NaCl、Ba(NO3)2、HCl D、NH4NO3、NaOH、Na2SO419. 下列实验操作不能达到实验目的的是( )
A、集气瓶中产生大量白烟 B、红磷燃烧一段时间后熄灭 C、烧杯中的水倒吸进入集气瓶 D、集气瓶中水面最终上升至1处12. 2021年12月9日,“天空课堂”在中国空间站精彩开讲。铁酸镍(化学式:NiFe2O4)可以将航天员呼出的废气转化为航天员需要的气体,而本身的质量和化学性质都不变化,NiFe2O4中若铁元素的化合价是+3价,则镍(Ni)元素的化合价是( )A、+2 B、+4 C、-1 D、-213. 燃烧是人们生活中重要的化学反应,我们既要利用燃烧,也要注意防灾减灾。下列有关燃烧、灭火与安全的说法,正确的是( )A、炒菜时油锅着火,可用水浇灭 B、加油站、矿井等场所要严禁烟火 C、高层楼房失火时,立即乘电梯下楼逃生 D、用燃着的火柴很难直接点燃煤,是因为煤不具有可燃性14. 下列有关实验现象的描述正确的是( )A、向少量氧化铜中加入稀硫酸,有气泡产生,黑色粉末逐渐消失,溶液变蓝 B、用粗砂纸打磨后的铝片放入硫酸铜溶液中,一段时间后,划痕处出现红色物质 C、细铁丝在氧气中燃烧,火星四射,生成红棕色固体 D、向滴有石蕊的稀盐酸中滴加氢氧化钠溶液至过量,溶液由蓝色变紫色再变红色15. “飞扬”冬奥,火炬采用的燃料是氢燃料,不是传统燃料丙烷,丙烷(X)完全燃烧的化学方程式为: , 丙烷(X)的化学式为( )A、C3H4 B、C3H8O C、C3H8 D、C3H6O216. 下列是生活中一些常见物质的近似pH,其中能使紫色石蕊溶液变蓝的是( )A、炉具清洁剂pH=13 B、牛奶pH=6.5 C、洁厕灵pH=1 D、纯净水pH=717. 下列物质中,不能与稀盐酸发生反应的是( )A、Fe2O3 B、Na2CO3 C、NaCl D、NaOH18. 下列各组物质在水溶液中能够共存,而且加入石蕊显红色的是( )A、NaOH、CuSO4、H2SO4 B、NaCl、Na2SO4、NaHCO3 C、NaCl、Ba(NO3)2、HCl D、NH4NO3、NaOH、Na2SO419. 下列实验操作不能达到实验目的的是( )选项
实验目的
实验操作
A
除去CaCl2溶液中的少量盐酸
加入过量碳酸钙充分反应后过滤
B
除去CO2中少量的CO
点燃
C
鉴别固体(NH4)2SO4和K2SO4
分别取样,加熟石灰研磨,闻气味
D
除去Cu粉中少量的Fe粉
加入足量的稀盐酸充分反应、过滤、洗涤、烘干
A、A B、B C、C D、D二、多选题
-
20. 逻辑推理是一种重要的化学思维方法,下列说法中,正确的是( )A、若某雨水的pH<7,则该雨水一定呈酸性 B、催化剂可以改变化学反应的速率,则改变化学反应速率的物质一定是催化剂 C、将酚酞滴入碱性溶液后显红色,则能使酚酞变红色的溶液一定是碱性溶液 D、活泼金属加入稀盐酸能产生气体,则能与稀盐酸反应产生气体的固体一定是活泼金属
三、填空题
-
21. 请用物质的序号填空:请从①碘酒 ②烧碱 ③金刚石 ④盐酸 ⑤碳酸钙 ⑥葡萄糖,六种物质中选择正确的物质,用序号填空。(1)、人体胃液中主要的酸是。(2)、可用于消毒伤口的是。(3)、可作为人体重要能量来源的是。(4)、可用作补钙剂的是。(5)、可做钻探机钻头的是。(6)、炉具清洁剂里含有能去除油污的物质。22. 请用化学用语填空:(1)、2个汞原子。(2)、氯酸钾中氯元素化合价为+5。(3)、碱溶液中的阴离子。(4)、醋酸。23. 生活中处处有化学,回答下列问题:(1)、铁制品在(填“潮湿”或“干燥”)的空气中容易生锈:(2)、洗洁精清洗餐具去除油污时起作用:(3)、直饮水中可溶性钙、镁化合物的含量很低,它属于(填“硬水”或“软水”)。(4)、记录重要文献资料时,应使用碳素墨水,是因为。(5)、天然气属于(填“可再生”或“不可再生”)能源,其主要成分(甲烷)在空气中充分燃烧的化学方程式为。24. 元素周期表是学习和研究化学的重要工具。请分析下图中的信息并回答下列问题。
 (1)、原子序数为14的元素属于(填“金属”或“非金属”)元素,氮元素和磷元素的化学性质相似,是因为氮原子和磷原子的相同。(2)、R+结构示意图如右图所示,R元素位于元素周期表中第周期,它的化学性质与第三周期中的元素相似。
(1)、原子序数为14的元素属于(填“金属”或“非金属”)元素,氮元素和磷元素的化学性质相似,是因为氮原子和磷原子的相同。(2)、R+结构示意图如右图所示,R元素位于元素周期表中第周期,它的化学性质与第三周期中的元素相似。 (3)、结构决定性质,从原子结构示意图可以推测元素的化学性质。在元素周期表前18号元素中,最活泼的非金属元素是(填元素符号)。25. 下图为甲、乙、丙三种固体物质(不形成结晶水合物)在水中随温度变化的溶解度曲线,按要求填空。
(3)、结构决定性质,从原子结构示意图可以推测元素的化学性质。在元素周期表前18号元素中,最活泼的非金属元素是(填元素符号)。25. 下图为甲、乙、丙三种固体物质(不形成结晶水合物)在水中随温度变化的溶解度曲线,按要求填空。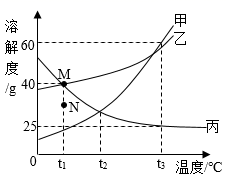 (1)、在℃时,甲和丙的溶解度相等。(2)、t1℃时,将乙溶液的状态由 M 点变为N 点,方法是。(3)、t3℃时,将40g 甲放入 50g 水中,充分溶解后所得溶液的质量为。(4)、t3℃时,将 125g 丙的饱和溶液降温至t1℃,应再加入g 丙才能恰好达到饱和状态。26. 北京第24届冬季奥林匹克运动会取得了巨大成功,北京也成为历史上首座“双奥之城”。
(1)、在℃时,甲和丙的溶解度相等。(2)、t1℃时,将乙溶液的状态由 M 点变为N 点,方法是。(3)、t3℃时,将40g 甲放入 50g 水中,充分溶解后所得溶液的质量为。(4)、t3℃时,将 125g 丙的饱和溶液降温至t1℃,应再加入g 丙才能恰好达到饱和状态。26. 北京第24届冬季奥林匹克运动会取得了巨大成功,北京也成为历史上首座“双奥之城”。 (1)、冬奥会速滑馆的冰面用目前最先进的二氧化碳跨临界直冷制冰技术制作。固态CO2能制冷的原因是。(2)、冬奥会火种灯内外灯罩之间设计了一个导流通道,能够让燃料在燃烧时不至于产生黑烟和异味,保持火种灯外观清洁、透亮。从促进燃料充分燃烧角度看,导流通道的作用是;灯体使用再生铝合金,主要利用其密度小,性好的特点。(3)、冰壶的材质主要是不含云母的花岗岩,在撞击时不会碎,也不易改变质量与外形。由此推断花岗岩具有的性质是。(4)、冰壶运动员穿的两只鞋的鞋底材质是不同的,蹬冰脚的鞋底为橡胶制成,滑行脚的鞋底为塑料制成。橡胶与塑料都属于(填“无机”或“有机”)材料。(5)、欲判断冰壶刷的材料是合成鬃还是马鬃,可采用的实验方法。
(1)、冬奥会速滑馆的冰面用目前最先进的二氧化碳跨临界直冷制冰技术制作。固态CO2能制冷的原因是。(2)、冬奥会火种灯内外灯罩之间设计了一个导流通道,能够让燃料在燃烧时不至于产生黑烟和异味,保持火种灯外观清洁、透亮。从促进燃料充分燃烧角度看,导流通道的作用是;灯体使用再生铝合金,主要利用其密度小,性好的特点。(3)、冰壶的材质主要是不含云母的花岗岩,在撞击时不会碎,也不易改变质量与外形。由此推断花岗岩具有的性质是。(4)、冰壶运动员穿的两只鞋的鞋底材质是不同的,蹬冰脚的鞋底为橡胶制成,滑行脚的鞋底为塑料制成。橡胶与塑料都属于(填“无机”或“有机”)材料。(5)、欲判断冰壶刷的材料是合成鬃还是马鬃,可采用的实验方法。四、综合题
-
27. 某工厂为实现“碳中和”目标,设计了一种“捕捉”CO2的减排方案,流程如图所示:
 (1)、分离器起的作用之一类似于过滤,实验室过滤操作中用来引流的玻璃仪器是。(2)、分离器中可能发生的化学反应有(用化学方程式表示,任写一个)(3)、反应器中发生的化学变化的基本反应类型为。(4)、上述流程中可循环利用的物质的化学式为。28. 请结合图回答问题:
(1)、分离器起的作用之一类似于过滤,实验室过滤操作中用来引流的玻璃仪器是。(2)、分离器中可能发生的化学反应有(用化学方程式表示,任写一个)(3)、反应器中发生的化学变化的基本反应类型为。(4)、上述流程中可循环利用的物质的化学式为。28. 请结合图回答问题: (1)、仪器名称:②。(2)、用高锰酸钾制取氧气,可选用的发生装置是(选填序号),该反应的化学方程式为。用E装置收集氧气完毕后,应先(选填“从水中取出导气管”或“熄灭酒精灯”)。(3)、实验室制取CO2 , 反应的化学方程式为 , 为方便控制反应的发生和停止,应选择的发生装置是(填序号),用该方法得到的 气体中会通常含有少量的水蒸气和(填名称)气体。(4)、 是一种可溶于水的气体,不能用排水法收集。老师说将装置E水槽中的水换成热水也可以收集 ,你认为其原因是。29. 某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。
(1)、仪器名称:②。(2)、用高锰酸钾制取氧气,可选用的发生装置是(选填序号),该反应的化学方程式为。用E装置收集氧气完毕后,应先(选填“从水中取出导气管”或“熄灭酒精灯”)。(3)、实验室制取CO2 , 反应的化学方程式为 , 为方便控制反应的发生和停止,应选择的发生装置是(填序号),用该方法得到的 气体中会通常含有少量的水蒸气和(填名称)气体。(4)、 是一种可溶于水的气体,不能用排水法收集。老师说将装置E水槽中的水换成热水也可以收集 ,你认为其原因是。29. 某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。【演示实验】将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。
【查阅资料】CaCl2溶液显中性。
【提出问题】实验中未观察到明显现象,部分同学产生了疑惑:反应后溶液中除了水还有哪些成分?
(1)、【猜想与假设】同学们猜想如下:猜想一:只有CaCl2猜想二:有CaCl2和HCl
猜想三: 猜想四:有CaCl2、HCl和Ca(OH)2
同学们讨论后一致认为猜想四不合理,理由是(用化学方程式解释)
(2)、【实验探究】为了验证猜想。甲小组设计了下列三个方案:实验方案
方案Ⅰ:滴加紫色石蕊试液
方案Ⅱ:加入铁粉
方案Ⅲ:滴加Na2CO3溶液
实验操作



实验现象
溶液呈紫色
产生白色沉淀
实验结论
猜想正确
猜想二正确
猜想三正确
(3)、【评价反思】乙小组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明猜想三正确,请你帮助他们说明原因:。(4)、【拓展迁移】丙小组同学认为,要验证猜想三成立,还可借助其他方案,为完成实验探究,下列物质中可选用的有(填序号)。①CuSO4溶液 ②BaCO3 ③酚酞溶液 ④FeCl3溶液 ⑤CO2
五、计算题
-
