黑龙江省牡丹江市2021-2022学年高一下学期开学考试化学试题
试卷更新日期:2022-06-09 类型:开学考试
一、选择题(本题包括20小题,每小题3分,共60分。每小题只有一个选项符合题意)。
-
1. 能用H++OH- = H2O表示的反应是( )A、氢氧化钡溶液与硫酸反应 B、氢氧化铜与稀硝酸反应 C、氢氧化钾与硫酸反应 D、氢氧化钠与醋酸反应2. 在下列溶液中能大量共存的无色透明离子组是( )A、K+、Na+、NO3-、MnO4- B、K+、Na+、Cl-、 SO42- C、K+、Na+、Br-、Cu2+ D、Na+、Ba2+、OH-、SO42-3. 下列离子方程式书写正确的是( )A、碳酸钙与盐酸反应 CO32-+2H+=CO2↑+H2O B、氢氧化钠和醋酸反应 OH-+H+=H2O C、硫酸和氯化钡溶液反应 Ba2++SO42-=BaSO4↓ D、铁钉放入硫酸铜溶液中 Fe+3Cu2+=2Fe3++3Cu4. 工业上冶炼钛的反应如下:TiCl4+2Mg Ti+2MgCl2。下列有关该反应的说法正确的是( )A、TiCl4是还原剂 B、Mg被氧化 C、TiCl4发生氧化反应 D、Mg得到电子5. 下列变化一定需要加入还原剂才能实现的是( )A、HCO3- →CO2 B、HCl→Cl2 C、KClO3→KCl D、MnO4- →Mn2+6. 除去Na2CO3固体中少量NaHCO3的最佳方法是 ( )A、加入适量盐酸 B、加入NaOH溶液 C、加热 D、配成溶液后通入CO27. 下列有关铝及其化合物的说法错误的是( )A、铁易生锈,而铝在空气中较稳定,所以铁比铝活泼 B、可用铝壶烧开水,不可用其长期存放食醋、碱水 C、氧化铝是一种较好的耐火材料,但不可用氧化铝坩埚熔化NaOH D、Al2O3能跟强酸、强碱溶液反应生成盐和水,所以它是两性氧化物8. 0oC,101KPa, 4.48L 某气体的质量为8g,则该气体的相对原子质量为( )A、40 B、40 g/mol C、160 D、160g/mol9. 将300mL 0.5mol/LNaOH溶液加水稀释到500mL,稀释后溶液中的NaOH的物质的量 浓度为( )A、0.3mol/L B、0.03mol/L C、 0.05mol/L D、0.04mol/L10. 下列有关铁与水反应的说法中正确的是( )A、在任何条件下,铁与水均能发生反应 B、在高温时,铁与水蒸气反应生成氢氧化铁和氢气 C、在高温时,铁与水蒸气反应生成氧化铁和氢气 D、在高温时,铁与水蒸气反应生成四氧化三铁和氢气11. 下列关于Fe2+和Fe3+的叙述中,错误的是( )A、Fe2+的水溶液为浅绿色 B、Fe3+的水溶液为黄色 C、Fe3+具有氧化性,Fe2+具有还原性 D、Fe3+溶液中滴入含SCN-的溶液,立即出现红色沉淀12. 证明某溶液中不含Fe3+而可能含有Fe2+ , 进行实验操作时最佳顺序为( )
①加入适量氯水 ②加入足量的KMnO4溶液 ③加入少量KSCN溶液.
A、③① B、③② C、①③ D、①②③13. 关于元素周期表的下列叙述,错误的是( )A、元素周期表揭示了化学元素间的内在联系,是化学发展史上的重要里程碑之一 B、在周期表中,把电子层数相同的元素排成一横行,称为一周期 C、元素周期表中,总共有18个纵行,18个族 D、第IA族的元素又称为碱金属元素(除了H),第VIIA族的元素又称为卤族元素14. 某元素原子最外层比次外层多5个电子,该元素的最高正化合价为( )A、+5 B、+6 C、+7 D、无最高正化合价15. 下列各组中化合物的性质比较,不正确的是( )A、酸性:HClO4>HBrO4>HIO4 B、稳定性:PH3>H2S> HCl C、碱性:NaOH>Mg(OH)2>Al(OH)3 D、非金属性:F>O>S16. 下列电子式正确的是( )A、 B、
B、 C、
C、 D、
D、 17. 关于元素周期表,下列叙述中不正确的是( )A、在元素周期表的氟氯硫磷砷附近可以寻找制备新型农药材料的元素 B、在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 C、在周期表的左下角可以寻找制备半导体材料的元素 D、在地球上元素的分布和它们在元素周期表中的位置有密切关系18. SO2有毒,但葡萄酒中都含有少量的SO2 , 以起到保鲜、杀菌和抗氧化的作用。下列说法不正确的是( )A、葡萄酒中的SO2对人体无害,因为它的含量很少 B、葡萄酒中的SO2具有抗氧化的作用,因为SO2具有较强的还原性 C、从红葡萄酒的颜色可判断出,其中的SO2没有漂白性 D、葡萄酒倒入酒杯摇一摇,可以减少其中SO2的含量19. 下列不属于可逆反应的是( )A、氯气与水反应生成盐酸与次氯酸 B、SO2的催化氧化 C、水电解生成H2和O2 , H2和O2点燃条件下生成H2O D、SO2溶于水和H2SO3分解20. 硫的氧化性不如氧气强,在下列叙述中不能说明这一事实的是( )A、S+O2=SO2 , O2是氧化剂、S是还原剂 B、S是淡黄色固体,O2是无色气体 C、氢硫酸放置在空气中易变浑浊(2H2S+O2=2S↓+2H2O) D、S和Cu反应只能生成Cu2S(硫化亚铜),而O2与Cu反应生成CuO
17. 关于元素周期表,下列叙述中不正确的是( )A、在元素周期表的氟氯硫磷砷附近可以寻找制备新型农药材料的元素 B、在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 C、在周期表的左下角可以寻找制备半导体材料的元素 D、在地球上元素的分布和它们在元素周期表中的位置有密切关系18. SO2有毒,但葡萄酒中都含有少量的SO2 , 以起到保鲜、杀菌和抗氧化的作用。下列说法不正确的是( )A、葡萄酒中的SO2对人体无害,因为它的含量很少 B、葡萄酒中的SO2具有抗氧化的作用,因为SO2具有较强的还原性 C、从红葡萄酒的颜色可判断出,其中的SO2没有漂白性 D、葡萄酒倒入酒杯摇一摇,可以减少其中SO2的含量19. 下列不属于可逆反应的是( )A、氯气与水反应生成盐酸与次氯酸 B、SO2的催化氧化 C、水电解生成H2和O2 , H2和O2点燃条件下生成H2O D、SO2溶于水和H2SO3分解20. 硫的氧化性不如氧气强,在下列叙述中不能说明这一事实的是( )A、S+O2=SO2 , O2是氧化剂、S是还原剂 B、S是淡黄色固体,O2是无色气体 C、氢硫酸放置在空气中易变浑浊(2H2S+O2=2S↓+2H2O) D、S和Cu反应只能生成Cu2S(硫化亚铜),而O2与Cu反应生成CuO二、非选择题
-
21. 用如图所示装置可检验混合气体中同时含有SO2和CO2。
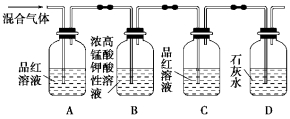 (1)、能够证明混合气体中含有SO2的实验现象是:;(2)、设计B、C的实验目的是:;(3)、写出B中发生反应的离子方程式:;(4)、能够证明混合气体中含有CO2的实验现象是: 。(5)、若将等体积的SO2和Cl2一起通入水中,写出所发生反应的化学方程式。22. 配制1 mol/L的CuSO4溶液500mL,需胆矾g;把称好的胆矾放入里,用适量蒸馏水使它完全溶解,把制得的溶液小心地注入容量瓶中,用适量蒸馏水洗涤烧杯2~3次,把每次的洗涤液都注入容量瓶中,然后慢慢地加入蒸馏水到液面距刻线处,改用滴加蒸馏水到液面与刻线相切;把瓶塞盖好,颠倒摇匀。从配好的溶液中取出10mL,此时溶液的物质的量浓度为。23. 实验室用如图所示方法制Fe(OH)2 , 但一般看不到白色的Fe(OH)2沉淀,原因是Fe(OH)2不稳定,极易被O2氧化生成Fe(OH)3。请回答:
(1)、能够证明混合气体中含有SO2的实验现象是:;(2)、设计B、C的实验目的是:;(3)、写出B中发生反应的离子方程式:;(4)、能够证明混合气体中含有CO2的实验现象是: 。(5)、若将等体积的SO2和Cl2一起通入水中,写出所发生反应的化学方程式。22. 配制1 mol/L的CuSO4溶液500mL,需胆矾g;把称好的胆矾放入里,用适量蒸馏水使它完全溶解,把制得的溶液小心地注入容量瓶中,用适量蒸馏水洗涤烧杯2~3次,把每次的洗涤液都注入容量瓶中,然后慢慢地加入蒸馏水到液面距刻线处,改用滴加蒸馏水到液面与刻线相切;把瓶塞盖好,颠倒摇匀。从配好的溶液中取出10mL,此时溶液的物质的量浓度为。23. 实验室用如图所示方法制Fe(OH)2 , 但一般看不到白色的Fe(OH)2沉淀,原因是Fe(OH)2不稳定,极易被O2氧化生成Fe(OH)3。请回答: (1)、向氯化亚铁溶液中滴加氢氧化钠溶液
(1)、向氯化亚铁溶液中滴加氢氧化钠溶液反应的离子方程式: ;现象是
(2)、Fe(OH)2被O2 氧化的化学方程式是:。(3)、实验室保存FeCl2溶液常常加入铁粉,其作用是(用离子方程式表示),检验FeCl2溶液是否变质,可向其中加入(填化学式)溶液,观察现象。24. 下表是元素周期表的一部分,回答下列关问题: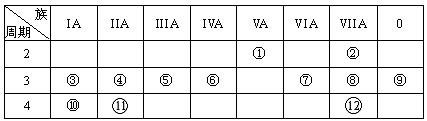 (1)、下列表述中能证明元素⑦与元素⑧非金属性强弱关系的是。
(1)、下列表述中能证明元素⑦与元素⑧非金属性强弱关系的是。a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
d. 元素⑧的氧化物的水化物酸性强于元素⑦的氧化物的水化物酸性
(2)、第三周期中,原子半径最大的元素是(填元素符号),简单离子半径最小的是(填化学式)。(3)、④与⑧可以形成(填离子或共价)化合物,请用电子式表示其形成过程:。