陕西省商洛市2022届高三第二次高考模拟检测试卷理科综合化学试题
试卷更新日期:2022-06-06 类型:高考模拟
一、单选题
-
1. 2022年3月5日《政府工作报告》中强调要“加强废旧物资循环利用”,下列北京冬奥会的各项做法中与此无关的是( )A、实现“水立方”变为“冰立方” B、采用光伏、风能产生绿电制备绿氢 C、“冰墩墩”填充循环再生聚酯纤维 D、收集消融的雪水用于景观绿化2. 下列装置能达到实验目的的是( )
 A、利用甲装置配制一定物质的量浓度的稀硫酸 B、利用乙装置制备并收集少量二氧化氮气体 C、利用丙装置由工业酒精制取无水酒精 D、利用丁装置从氯化镁溶液中获得无水3. 某有机物M是合成阿比朵尔的中间体,其结构简式如图所示,下列说法正确的是( )
A、利用甲装置配制一定物质的量浓度的稀硫酸 B、利用乙装置制备并收集少量二氧化氮气体 C、利用丙装置由工业酒精制取无水酒精 D、利用丁装置从氯化镁溶液中获得无水3. 某有机物M是合成阿比朵尔的中间体,其结构简式如图所示,下列说法正确的是( ) A、该有机物苯环上的一氯代物有4种 B、该有机物的分子式为C14H17NO4 C、分子中所有原子一定处于同一平面 D、该物质不能发生加成反应4. 短周期主族元素X、Y、Z、W的原子序数依次增大。元素X在常见化合物中均显负价,X、Y的最外层电子数之和与W的最外层电子数相等,Z的单质能与Y的最高价氧化物对应的水化物反应且有氢气生成。下列说法一定正确的是( )A、简单离子半径的大小顺序:W>Y>X B、Z的最高价氧化物对应的水化物是两性氢氧化物 C、X的最简单氢化物沸点高于W的最简单氢化物沸点 D、和均具有漂白性,但漂白原理不同5. 丙酮是最简单的脂肪酮,人们把它作为模型进行了大量的光化学反应研究。丙酮分子中存在如图1所示4种类型的化学键,即C=O、、、 , 丙酮在激光强度为时,在特定的时间间隔内这4种类型的化学键的键长变化如图2所示。
A、该有机物苯环上的一氯代物有4种 B、该有机物的分子式为C14H17NO4 C、分子中所有原子一定处于同一平面 D、该物质不能发生加成反应4. 短周期主族元素X、Y、Z、W的原子序数依次增大。元素X在常见化合物中均显负价,X、Y的最外层电子数之和与W的最外层电子数相等,Z的单质能与Y的最高价氧化物对应的水化物反应且有氢气生成。下列说法一定正确的是( )A、简单离子半径的大小顺序:W>Y>X B、Z的最高价氧化物对应的水化物是两性氢氧化物 C、X的最简单氢化物沸点高于W的最简单氢化物沸点 D、和均具有漂白性,但漂白原理不同5. 丙酮是最简单的脂肪酮,人们把它作为模型进行了大量的光化学反应研究。丙酮分子中存在如图1所示4种类型的化学键,即C=O、、、 , 丙酮在激光强度为时,在特定的时间间隔内这4种类型的化学键的键长变化如图2所示。
下列判断错误的是( )
A、I表示C-C键,在该条件下最易断裂 B、丙酮在该条件下的光解反应是吸热反应 C、丙酮在该条件下解离的第一步反应可表示为 D、丙酮在该条件下的光解反应中只有化学键的断裂6. 利用微生物除去废水中的乙酸钠和氯苯( ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( ) A、A极上的电极反应式为
A、A极上的电极反应式为 +e-=Cl-+
+e-=Cl-+ B、每除去1mol氯苯,同时产生11.2L(标准状况)
C、电子流向:B极→导线→A极→溶液→B极
D、该装置在高温环境中工作效率更高
7. 常温下,向10 mL0.1 mol·L-1丙烯酸(CH2=CHCOOH)溶液中滴加0.1 mol·L-1 NaOH溶液,溶液的酸度(AG)与NaOH溶液体积的关系如图所示。
B、每除去1mol氯苯,同时产生11.2L(标准状况)
C、电子流向:B极→导线→A极→溶液→B极
D、该装置在高温环境中工作效率更高
7. 常温下,向10 mL0.1 mol·L-1丙烯酸(CH2=CHCOOH)溶液中滴加0.1 mol·L-1 NaOH溶液,溶液的酸度(AG)与NaOH溶液体积的关系如图所示。
已知:AG=lg , 电离度=x 100%。
若忽略溶液混合时的体积变化,下列说法正确的是( )
A、b点对应的溶液中:c( Na+) >c(CH2=CHCOO-) >c(H+) >c(OH-) B、d点对应的溶液中:c(OH-) =c(H+) +c(CH2=CHCOO-) +c( CH2=CHCOOH) C、0.1 mol·L-1 CH2=CHCOOH溶液中丙烯酸的电离度近似等于10% D、若AG=0时V=x,则丙烯酸的电离常数为Ka=×10-7二、综合题
-
8. 硫化锂(Li2S)易潮解,在加热条件下易被空气中的氧化,是一种潜在的锂电池的电解质材料。实验室用粗锌(含少量铜、FeS)和稀硫酸反应制备 , 并用制得的去还原硫酸锂制备硫化锂,反应原理: , 实验装置如图所示。请回答下列问题:
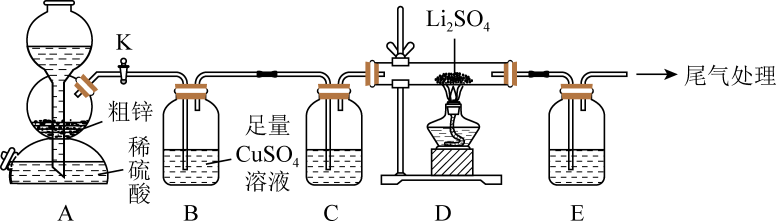 (1)、选择A装置实现随制随停,还适用于下列试剂制备对应气体的是(填标号)。
(1)、选择A装置实现随制随停,还适用于下列试剂制备对应气体的是(填标号)。a.70%硫酸、亚硫酸钠 b.:稀盐酸、大理石
c.:浓氨水、生石灰 d.:浓盐酸、
(2)、C和E装置中盛装的试剂相同,均可选择(填名称),E装置的作用是。(3)、B装置中发生反应的离子方程式为。(4)、得到的产品中往往含有一定量的杂质,某小组同学对产品中的杂质进行探究。①提出猜想:
猜想一:产品中含杂质
猜想二:产品中含杂质
猜想三:产品中含杂质S
依据所学知识,猜想三不成立,理由是。
②化学小组为验证猜想:
限选试剂:稀盐酸、稀硫酸、蒸馏水、品红溶液、双氧水、氯化钡溶液、硝酸钡溶液
实验
操作与现象
结论
I
取少量样品溶于水,
样品中不含
II
在实验I反应后的溶液中,
样品中含
(5)、测定产品纯度的方法:取wg样品加入足量稀硫酸,充分反应后,煮沸溶液,冷却后滴加酚酞溶液作指示剂,用NaOH标准溶液滴定,消耗NaOH标准溶液。①煮沸的目的是。
②样品的纯度为。
9. 铬酸铅俗称铬黄,是一种难溶于水的黄色固体,也是一种重要的黄色颜料,常用作橡胶、油墨、水彩、色纸等的着色剂。工业上用草酸泥渣(主要含草酸铅、硫酸铅)和铬矿渣(主要成分为 , 含有少量的、、)为原料制备铬酸铅,实现资源的回收再利用,其流程如下:
回答下列问题:
(1)、将铬矿渣“粉碎”的目的是;草酸泥渣“焙烧”后“水洗”的作用是。(2)、“滤渣II”的主要成分是(填化学式)。(3)、“氧化焙烧”时,被氧化的反应的化学方程式为。(4)、“一系列操作”包括、粉碎。(5)、为了使产品更纯,需将“含、的溶液”分离提纯,依据如图所示的溶解度信息,“含、的溶液”分离提纯的操作是。分离提纯后得到的固体的化学式为。 (6)、“焙烧”时加入碳酸钠是为了将硫酸铅转化为氧化铅(PbO),流程中加入碳酸钠的量为理论值的1.5倍,已知草酸泥渣中硫酸铅的含量为20.2%,则加入碳酸钠与草酸泥渣的质量之比为。10. 乙烷、乙烯均是有机合成中重要的原料,乙烯年产量的多少可体现一个国家石油化工发展水平的高低。回答下列问题:(1)、已知有关反应热化学方程式如下:
(6)、“焙烧”时加入碳酸钠是为了将硫酸铅转化为氧化铅(PbO),流程中加入碳酸钠的量为理论值的1.5倍,已知草酸泥渣中硫酸铅的含量为20.2%,则加入碳酸钠与草酸泥渣的质量之比为。10. 乙烷、乙烯均是有机合成中重要的原料,乙烯年产量的多少可体现一个国家石油化工发展水平的高低。回答下列问题:(1)、已知有关反应热化学方程式如下:①C2H6(g)C2H4(g)+H2(g) △H1=+137kJ·mol-1
②C2H4(g)+3O2(g)2CO2(g)+2H2O(l) △H2=-1411kJ·mol-1
欲利用反应①、②中的数据求C2H6(g)的燃烧热,还需要知道一种物质的燃烧热(用△H3表示),请写出该物质的燃烧热的热化学方程式。C2H6(g)的燃烧热(△H4)为(用含△H3的代数式表示)。
(2)、一定条件下向某刚性恒容密闭容器内充入一定量的C2H6(g),使其只发生反应①,测得不同温度,分别使用甲、乙两种催化剂的情况下,经过相同反应时间时乙烷的转化率随温度的变化情况如图1所示。
①温度低于1000K时,两种催化剂对该反应活化能影响较大的是(填“甲”或“乙”),使用该催化剂时,该转化反应适宜的温度是;使用催化剂甲时,当温度高于1000K时,C2H6的转化率减小的原因可能是(填标号)。
A.平衡向左移动
B.催化剂催化活性降低,导致反应速率减小
C.温度过高,乙烯与氢气发生反应
②乙烷的转化率随时间的变化关系如图2所示,在m点条件下,平衡时总压为2.1×105Pa,经过10min反应达到平衡状态,则0~10min内m点对应反应的v(C2H6)=Pa·min-1 , Kp为用气体分压表示的平衡常数,分压=总压×物质的量分数,则平衡常数Kp=Pa。
 (3)、利用电解法可将乙烷转化为乙酸、乙烯等多种产品,工作原理如图3所示。写出生成乙酸的电极反应式:。
(3)、利用电解法可将乙烷转化为乙酸、乙烯等多种产品,工作原理如图3所示。写出生成乙酸的电极反应式:。 11. 我国科学家最近开发的催化剂可实现NO还原制 , 为资源回收利用提供新思路。请回答下列问题:(1)、基态N原子价层电子排布图为。(2)、上述物质所含的第二周期元素中,第一电离能由大到小的顺序为(填元素符号,下同);电负性由小到大的顺序为。(3)、氨硼烷()是一种新型储氢材料。分子中B原子的杂化方式为。中的∠HNH(填“>”、“<”或“=”)中的∠HNH。(4)、已知(碳化硼),BN(氮化硼)的熔点依次为2550℃、3300℃,这两种物质的点存在差异的主要原因是。(5)、已知的晶胞结构如图1所示,该晶胞中含有的阳离子数为 , 阳离子的配位数为。
11. 我国科学家最近开发的催化剂可实现NO还原制 , 为资源回收利用提供新思路。请回答下列问题:(1)、基态N原子价层电子排布图为。(2)、上述物质所含的第二周期元素中,第一电离能由大到小的顺序为(填元素符号,下同);电负性由小到大的顺序为。(3)、氨硼烷()是一种新型储氢材料。分子中B原子的杂化方式为。中的∠HNH(填“>”、“<”或“=”)中的∠HNH。(4)、已知(碳化硼),BN(氮化硼)的熔点依次为2550℃、3300℃,这两种物质的点存在差异的主要原因是。(5)、已知的晶胞结构如图1所示,该晶胞中含有的阳离子数为 , 阳离子的配位数为。 (6)、钛晶体有两种晶胞结构(如图2和图3所示)。图2中晶胞的空间利用率(φ)为(用含π的式子表示);已知图3中晶胞底边长为anm,高为cnm,NA代表阿伏加德罗常数的值,则该晶体密度为(用含a、c、NA的代数式表示)。12. 有机物G是某药物的中间体,G的一种合成路线如下:
(6)、钛晶体有两种晶胞结构(如图2和图3所示)。图2中晶胞的空间利用率(φ)为(用含π的式子表示);已知图3中晶胞底边长为anm,高为cnm,NA代表阿伏加德罗常数的值,则该晶体密度为(用含a、c、NA的代数式表示)。12. 有机物G是某药物的中间体,G的一种合成路线如下:
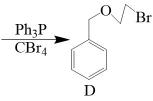




请回答下列问题:
(1)、依据官能团和碳的骨架分类,A属于;在核磁共振氢谱上G有组峰。(2)、反应A→B所需的试剂(填化学式)和条件分别为。(3)、F的分子式为 , 则F的结构简式为。F→G的反应类型是。(4)、B→C的化学方程式为。(5)、在C的同分异构体中,同时满足下列条件的结构有种(不考虑立体异构)。①分子中含有苯环;②1mol催化氧化后的产物能消耗4mol新制。
(6)、以甲苯和丙二酸二乙酯为原料合成 , 设计合成路线(无机试剂任选)。
, 设计合成路线(无机试剂任选)。