山东省日照市岚山区2022年中考一模化学试题
试卷更新日期:2022-06-01 类型:中考模拟
一、单选题
-
1. 2022年第24届冬奥会由北京市和张家口联合举办,此次冬奥会的理念之一是“绿色奥运”,下列做法与这一理念不相符的是( )A、发展公共交通,提倡绿色出行 B、增加使用太阳能、核能等新能源 C、改进燃煤技术,减少二氧化硫排放 D、改进燃煤锅炉烟囱,将废气排到高空2. 下列图示的实验操作正确的是( )A、取用粉末状药品
 B、检查装置气密性
B、检查装置气密性  C、溶解氯化钠
C、溶解氯化钠  D、制取氧气
D、制取氧气  3. 下列主题知识的归纳中,完全正确的是( )
3. 下列主题知识的归纳中,完全正确的是( )A.化学与健康
B.化学与环境
①适量的补充碘元素能预防甲状腺疾病
②用亚硝酸盐腌制蔬菜
③误食重金属盐,应喝大量的鲜榨果汁解毒
①使用无磷洗衣粉
②使用乙醇汽油能减少污染,节约石油资源
③使用新型可降解的塑料,减少“白色污染”
C.化学与安全
D.化学与生活
①档案材料失火,可用泡沫灭火器灭火
②炒菜时油锅着火可以用锅盖盖灭
③煤矿矿井要保持通风,严禁烟火
①用活性炭除去汽车内的异味
②用食盐水除去热水壶内壁的水垢
③用洗洁精和汽油都能除去衣服上的油污
A、A B、B C、C D、D4. 电解水实验装置如图所示,下列有关水的说法正确的是( )
A.实验过程中,
A、B两端产生气体的质量比为2:1 B、用肥皂水检验软水时,会产生大量浮渣 C、电解水时,可加入少量硫酸钠以增强导电性 D、用活性炭可将硬水软化5. 除去下列物质中的少量杂质,下列实验方案能达到目的的是( )选项
物质(括号内为杂质)
实验方案
A
MnO2(KCl)
先加足量水溶解,再过滤、洗涤、干燥
B
CO(CO2)
通过灼热的氧化铜
C
Fe2O3固体(CuO)
加入足量稀盐酸,过滤
D
NaOH溶液【Ca(OH)2】
加入过量的Na2CO3溶液,过滤
A、A B、B C、C D、D6. 抗击新冠肺炎疫情中,一种名为瑞德西韦(分子式:C27H35N6O8P)的新药枝寄予厚望,认为该新药或许会成为抗击新冠肺炎的“特效药”,下列说法正确的是( )A、瑞德西韦属于氧化物 B、瑞德西韦中氮元素与磷元素的质量比为14:31 C、瑞德西韦的相对分子质量是602 D、瑞德西韦由27个碳原子、35个氢原子、6个氮原子、8个氧原子和1个磷原子构成7. 节能减排、低碳出行是我们倡导的生活方式,“低碳”指的是尽量减少二氧化碳的排放。下列有关二氧化碳的说法正确的是()A、二氧化碳通入紫色石蕊溶液,溶液变为红色,说明二氧化碳具有酸性 B、二氧化碳的过度排放会加剧温室效应,因此应禁止使用化石燃料 C、二氧化碳和一氧化碳的组成元素相同,在一定条件下可以相互转化 D、进入久未开启的菜窖之前,必须做灯火试验,是因为二氧化碳有毒8. 2021年10月16日,神舟十三号载人飞船在酒泉卫星发射中心成功发射,于2022年4月16日成功抵达地面。神舟十三号的成功发射影显了中国航天的力量,在航天科技中会用到大量金属材料。下列有关金属材料的说法正确的是( )A、地壳中含量最高的金属元素是铁 B、钛和钛合金被广泛应用于火箭、导弹等 C、合金中一定只含金属元素 D、不锈钢的性能优良,所以钢是很纯的铁9. 在“宏观一微观一符号“之间建立联系,能帮助我们更好地认识物质的本质。如图表示某化学反应的微观过程,有关该反应的说法正确的是( ) A、该反应属于置换反应 B、甲物质中氮、氢元素的质量比为1:3 C、反应前后分子种类和数目不变 D、参加反应的甲、乙物质的分子个数比为4:510. 图像能直观体现化学中的各种变化,加深对化学知识的理解。下列图像能正确表示对应叙述的是( )A、
A、该反应属于置换反应 B、甲物质中氮、氢元素的质量比为1:3 C、反应前后分子种类和数目不变 D、参加反应的甲、乙物质的分子个数比为4:510. 图像能直观体现化学中的各种变化,加深对化学知识的理解。下列图像能正确表示对应叙述的是( )A、 在恒温条件下,将饱和氯化钠溶液蒸发适量水
B、
在恒温条件下,将饱和氯化钠溶液蒸发适量水
B、 将表面生锈的铁钉放入稀盐酸中
C、
将表面生锈的铁钉放入稀盐酸中
C、 加热一定质量的氯酸钾和二氧化锰的混合物
D、
加热一定质量的氯酸钾和二氧化锰的混合物
D、 向等质量的Zn和Mg中分别滴加等浓度等质量的稀盐酸
11. 某溶液中可能含有碳酸钾、硫酸钾中的一种或两种溶质,为测定其成分,进行如下实验:取一定量溶液于烧杯中,先加入过量氯化钡溶液,再加入稀硝酸,反应过程及产生沉淀的质量与所加溶液质量的关系如图所示。下列说法中正确的个数有( )
向等质量的Zn和Mg中分别滴加等浓度等质量的稀盐酸
11. 某溶液中可能含有碳酸钾、硫酸钾中的一种或两种溶质,为测定其成分,进行如下实验:取一定量溶液于烧杯中,先加入过量氯化钡溶液,再加入稀硝酸,反应过程及产生沉淀的质量与所加溶液质量的关系如图所示。下列说法中正确的个数有( )①该溶液中一定含有碳酸钾和硫酸钾
②反应进行到a点时,溶液中只含有一种溶质
③bc段上的任意一点 (c点除外) 都存在两种沉淀
④反应进行到c点时,溶液中只含有两种溶质
 A、1个 B、2个 C、3个 D、4个12. 现有Fe2O3和CuO的混合物mg,在高温条下用足量的CO还原,得到金属混合物2.4g。将生成的CO2气体用足量的澄清石灰水全部吸收后,产生白色沉淀5.0g,则m的数值为( )A、3.2 B、3.8 C、4.6 D、7.4
A、1个 B、2个 C、3个 D、4个12. 现有Fe2O3和CuO的混合物mg,在高温条下用足量的CO还原,得到金属混合物2.4g。将生成的CO2气体用足量的澄清石灰水全部吸收后,产生白色沉淀5.0g,则m的数值为( )A、3.2 B、3.8 C、4.6 D、7.4二、填空题
-
13. “见著知微,见微知著”是化学思维方法。下图中A、B、C、D是四种粒子的结构示意图。

请回答下列问题:
(1)、图中A、B、C、D属于种元素的粒子。(2)、D中x=。(3)、据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如图所示,请回答:该元素在元素周期表中位于第周期,其化学性质与哪种微粒性质相似(填字母),金属锶在化学反应中易(填“失去”或“得到”)电子,形成的离子是(填写离子符号) (4)、锶元素与C形成化合物的化学式是。14. 溶液与人们的生产生活密切相关。(1)、实验室用氯化钠固体配制100g溶质质量分数为8%的氯化钠溶液,下列说法中错误的是。
(4)、锶元素与C形成化合物的化学式是。14. 溶液与人们的生产生活密切相关。(1)、实验室用氯化钠固体配制100g溶质质量分数为8%的氯化钠溶液,下列说法中错误的是。A 实验的步骤为计算、称量、量取、溶解
B 量取水时,用规格为100mL的量筒
C 若用量筒量取水时俯视凹液面的最低处,则配制溶液的质量分数小于8%
D 溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解
(2)、硝酸钾、氯化钾的溶解度曲线如图1所示。
P点的含义是。
(3)、当温度时,氯化钾的溶解度大于硝酸钾的溶解度。(4)、t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定形成饱和溶液的是 , 其溶液的溶质质量分数为(结果精确到0.1%)。(5)、图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为 , 下列有关说法错误的是。A ①与②的溶质质量可能相等
B ②与③的溶质质量分数一定相等
C 等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D 等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾
三、综合题
-
15. 下图是中学常见物质的转换关系图。其中A、B常温下都为无色液体,且组成元素相同,A、B、X、Y、E都为氧化物,X、E都为黑色固体,Y可用作干燥剂,F是大理石的主要成分,I为蓝色沉淀,L为不溶于稀硝酸的白色沉淀。请回答:
 (1)、X在反应①中起作用。(2)、写出反应⑥的化学方程式。(3)、写出Y的化学式 , L的化学式。(4)、写出G在空气中变质发生反应的化学方程式。16. 电子工业上制造铜电路板,常用30%的FeCl3溶液腐蚀镀铜电路板上的铜箔(Cu),以下是某兴趣小组设计的处理该生产过程中产生废液的流程图。据图回答下列问题:
(1)、X在反应①中起作用。(2)、写出反应⑥的化学方程式。(3)、写出Y的化学式 , L的化学式。(4)、写出G在空气中变质发生反应的化学方程式。16. 电子工业上制造铜电路板,常用30%的FeCl3溶液腐蚀镀铜电路板上的铜箔(Cu),以下是某兴趣小组设计的处理该生产过程中产生废液的流程图。据图回答下列问题:查阅资料: ;
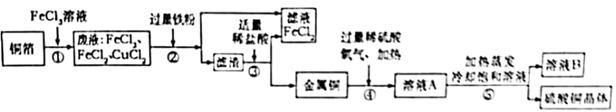 (1)、步骤①所得的废液中只含有FeCl3、CuCl2、FeCl2三种溶质,据此可判断步骤①中铜与FeCl3反应生成的两种产物是(写化学式)。(2)、步骤②中加入的铁粉与氯化铜发生反应的化学方程式是。步骤②还需要进行的实验操作是。(3)、步骤③加入适量稀盐酸充分反应,当观察到现象时,说明滤渣中只剩下铜。(4)、步骤②③所得FeCl2可与一种气体单质发生化合反应生成FeCl3 , 实现循环使用。根据质量守恒定律可推测该单质是。(5)、溶液B中含有的溶质是。17. 下图是实验室制备CO2 , 并验证CO2性质的实验装置图,请回答下列问题,
(1)、步骤①所得的废液中只含有FeCl3、CuCl2、FeCl2三种溶质,据此可判断步骤①中铜与FeCl3反应生成的两种产物是(写化学式)。(2)、步骤②中加入的铁粉与氯化铜发生反应的化学方程式是。步骤②还需要进行的实验操作是。(3)、步骤③加入适量稀盐酸充分反应,当观察到现象时,说明滤渣中只剩下铜。(4)、步骤②③所得FeCl2可与一种气体单质发生化合反应生成FeCl3 , 实现循环使用。根据质量守恒定律可推测该单质是。(5)、溶液B中含有的溶质是。17. 下图是实验室制备CO2 , 并验证CO2性质的实验装置图,请回答下列问题, (1)、写出标号仪器的名称:①。(2)、在检查装置A的气密性操作时,当关闭活塞M和N,向长颈漏斗中注水,观察到的现象,说明装置不漏气。(3)、关闭活塞N,打开活塞M,向长颈漏斗中加入稀盐酸,则A中发生的化学反应方程式是。装置C处观察到的现象是。(4)、关闭活塞M,打开活塞N,用A、D、E、F制取纯净干燥的CO2气体,装置D的作用是。装置E中盛装 , 可用于除去CO2气体中的水分。当观察到 , 说明F中已收集满CO2。18. 小兰用图示装置验证CO2能与NaOH发生化学反应。推注射器活塞向充满CO2的集气瓶(甲)中注入过量的NaOH溶液,振荡集气瓶后打开止水夹。(不考虑微溶物)
(1)、写出标号仪器的名称:①。(2)、在检查装置A的气密性操作时,当关闭活塞M和N,向长颈漏斗中注水,观察到的现象,说明装置不漏气。(3)、关闭活塞N,打开活塞M,向长颈漏斗中加入稀盐酸,则A中发生的化学反应方程式是。装置C处观察到的现象是。(4)、关闭活塞M,打开活塞N,用A、D、E、F制取纯净干燥的CO2气体,装置D的作用是。装置E中盛装 , 可用于除去CO2气体中的水分。当观察到 , 说明F中已收集满CO2。18. 小兰用图示装置验证CO2能与NaOH发生化学反应。推注射器活塞向充满CO2的集气瓶(甲)中注入过量的NaOH溶液,振荡集气瓶后打开止水夹。(不考虑微溶物) (1)、向容器甲中注入NaOH溶液后,打开止水夹后可以观察到现象证明CO2能与NaOH发生化学反应。(2)、反应后将甲中混合物过滤,得到白色沉淀和无色滤液。欲探究无色滤液中的溶质成分,小兰分析得出无色滤液中一定含(填化学式)(3)、【提出问题】无色滤液中还含有哪些溶质
(1)、向容器甲中注入NaOH溶液后,打开止水夹后可以观察到现象证明CO2能与NaOH发生化学反应。(2)、反应后将甲中混合物过滤,得到白色沉淀和无色滤液。欲探究无色滤液中的溶质成分,小兰分析得出无色滤液中一定含(填化学式)(3)、【提出问题】无色滤液中还含有哪些溶质【做出猜想】①Na2CO3;②CaCl2;③CaCl2和Na2CO3;④无其他溶质
小兰认为猜想一定不正确。(填序号)
(4)、【进行实验】实验步骤
实验现象
实验结论
Ⅰ.取少量滤液于试管中,滴加少量稀盐酸
无明显现象
猜想④成立
Ⅱ.
无明显现象
(5)、【实验交流】小梅认为上述实验结论不正确,理由是(用化学方程式表示)
四、计算题
-
19. 请根据如图所示的实验过程和提供的数据,解答下列问题。
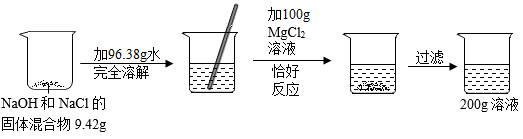 (1)、实验过程中,产生沉淀的质量为g。(2)、最终所得溶液中溶质的质量分数为多少? (写出计算过程)
(1)、实验过程中,产生沉淀的质量为g。(2)、最终所得溶液中溶质的质量分数为多少? (写出计算过程)