山东省临沂市兰山区2022年中考一模化学试题
试卷更新日期:2022-05-27 类型:中考模拟
一、单选题
-
1. 下列变化过程中,仅发生物理变化的是( )A、实验室制取氧气 B、硝酸钡溶液与稀硫酸混合 C、钢铁熔化 D、食物腐烂2. 下列物质中不属于盐的是( )A、小苏打 B、生石灰 C、氯化钾 D、硫酸钙3. 下列实验操作正确的是( )A、氢气验纯
 B、二氧化碳验满
B、二氧化碳验满 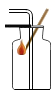 C、浓硫酸稀释
C、浓硫酸稀释 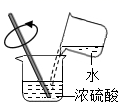 D、滴加液体
D、滴加液体 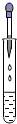 4. 下列化学用语书写正确的是( )A、干冰:CO B、2个氦气分子:2He2 C、乙醇:C2H5OH D、氯化铝:AlCl25. 防止金属锈蚀是科研人员研究的重要课题。小明发现金属铜制作的眼镜架,时间久了表面形成一层绿色的锈渍,其化学成分是碱式碳酸铜[Cu2(OH)2CO3]。该锈渍是通过化合反应生成的,反应物除金属铜、二氧化碳、水外,应还有( )A、氮气 B、氧气 C、二氧化硫 D、二氧化氮6. 一般来说,化学反应前后有元素化合价变化的反应属于氧化还原反应,则下列化学反应一定不属于氧化还原反应的是( )A、氧化铜和稀盐酸反应: B、铁与硫酸铜溶液反应: C、碳在足量氧气中充分燃烧: D、一氧化碳与氧化铜反应:7. 化学与我们的生活、生产密切相关。下列有关说法错误的是( )A、炒菜时油锅中的油着火,可用锅盖盖灭 B、为了身体健康,提倡使用一次性碗筷 C、减少雾霾,提倡公交出行 D、水体污染,会直接影响人体健康8. 下列实验现象正确的是( )A、硫在氧气中燃烧,发出微弱的淡蓝色火焰 B、向硫酸铜溶液中滴加氢氧化钠溶液产生白色沉淀 C、白磷在空气中燃烧,产生大量白雾 D、氢氧化钠暴露在空气中,表面形成溶液9. 构建化学基本观念是学好化学的基础。下列对化学基本观念的认识错误的是( )A、元素观:过氧化氢和水都是由氢元素和氧元素组成的 B、结构观:过氧化氢和水的化学性质不同是因为两者的分子构成不同 C、微粒观:一个过氧化氢分子是由一个氢分子和一个氧分子构成的 D、转化观:过氧化氢在一定条件下可以转化为水10. 据报道,地塞米松是一百个被证明能减少新冠肺炎死亡病例的药物。地塞米松是糖皮质类激素,其药理作用主要是抗炎、抗毒、抗过敏、抗风湿,临床使用较广泛,地塞米松的化学式为C22H29FO5 , 下列关于地塞米松的叙述正确的是( )A、地塞米松属于氧化物 B、地塞米松的相对分子质量是372 C、每个地塞米松分子由57个原子构成 D、地塞米松中氢、氧元素的质量之比为29:511. 宏观辨识与微观探析是化学学科的核心素养之一。下列对宏观事实的微观解释错误的是( )
4. 下列化学用语书写正确的是( )A、干冰:CO B、2个氦气分子:2He2 C、乙醇:C2H5OH D、氯化铝:AlCl25. 防止金属锈蚀是科研人员研究的重要课题。小明发现金属铜制作的眼镜架,时间久了表面形成一层绿色的锈渍,其化学成分是碱式碳酸铜[Cu2(OH)2CO3]。该锈渍是通过化合反应生成的,反应物除金属铜、二氧化碳、水外,应还有( )A、氮气 B、氧气 C、二氧化硫 D、二氧化氮6. 一般来说,化学反应前后有元素化合价变化的反应属于氧化还原反应,则下列化学反应一定不属于氧化还原反应的是( )A、氧化铜和稀盐酸反应: B、铁与硫酸铜溶液反应: C、碳在足量氧气中充分燃烧: D、一氧化碳与氧化铜反应:7. 化学与我们的生活、生产密切相关。下列有关说法错误的是( )A、炒菜时油锅中的油着火,可用锅盖盖灭 B、为了身体健康,提倡使用一次性碗筷 C、减少雾霾,提倡公交出行 D、水体污染,会直接影响人体健康8. 下列实验现象正确的是( )A、硫在氧气中燃烧,发出微弱的淡蓝色火焰 B、向硫酸铜溶液中滴加氢氧化钠溶液产生白色沉淀 C、白磷在空气中燃烧,产生大量白雾 D、氢氧化钠暴露在空气中,表面形成溶液9. 构建化学基本观念是学好化学的基础。下列对化学基本观念的认识错误的是( )A、元素观:过氧化氢和水都是由氢元素和氧元素组成的 B、结构观:过氧化氢和水的化学性质不同是因为两者的分子构成不同 C、微粒观:一个过氧化氢分子是由一个氢分子和一个氧分子构成的 D、转化观:过氧化氢在一定条件下可以转化为水10. 据报道,地塞米松是一百个被证明能减少新冠肺炎死亡病例的药物。地塞米松是糖皮质类激素,其药理作用主要是抗炎、抗毒、抗过敏、抗风湿,临床使用较广泛,地塞米松的化学式为C22H29FO5 , 下列关于地塞米松的叙述正确的是( )A、地塞米松属于氧化物 B、地塞米松的相对分子质量是372 C、每个地塞米松分子由57个原子构成 D、地塞米松中氢、氧元素的质量之比为29:511. 宏观辨识与微观探析是化学学科的核心素养之一。下列对宏观事实的微观解释错误的是( )选项
宏观事实
微观解释
A
氧气经压缩可以储存在钢瓶中
压强增大,分子间的间隔变小
B
水电解生成氢气和氧气
化学反应前后原子的种类改变
C
一氧化碳和二氧化碳化学性质不同
构成二者的分子不同
D
分子的质量和体积都很小
1滴水中大约有1.67×1021个水分子
A、A B、B C、C D、D12. 人们摄入的各种食物为生命活动提供物质基础和能量,下列说法正确的是( )A、维生素可以从蔬菜、水果等食物中获得 B、人体内缺钙会引起贫血症 C、霉变食物加热后即可食用 D、钠与锌元素都是人体所需的常量元素13. 将下列各组物质放入足量的水中,充分搅拌后,得到无色溶液的是( )A、氯化亚铁 B、硫酸钡 C、硫酸铜 D、氢氧化钙14. 材料研制与化学科学的发展密切相关。下列说法错误的是( )A、加快研发可降解塑料,解决由聚乙烯等塑料制品造成的“白色污染”问题 B、从远古的稻草增强黏土到如今钢筋混凝土、碳纤维等都应是复合材料 C、用于航天工业的钛合金具有耐高温、耐腐蚀、强度高等性能,属于金属材料 D、合成纤维、棉纤维和羊毛纤维,均是以石油为原料合成的有机高分子材料15. 兴趣小组按如图流程进行实验(每步均充分反应),反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,无明显现象,下列说法错误的是( ) A、滤液中的溶质一定有FeCl2、ZnCl2和CuCl2 B、滤渣中一定有Cu,一定没有Fe和Zn C、两支试管混合后,固体总质量一定增加 D、由实验可判断出铁、铜、锌的活动性顺序16. 检验、鉴别、除杂与分离是研究及获得物质的重要方法。下列实验方案不合理的是( )
A、滤液中的溶质一定有FeCl2、ZnCl2和CuCl2 B、滤渣中一定有Cu,一定没有Fe和Zn C、两支试管混合后,固体总质量一定增加 D、由实验可判断出铁、铜、锌的活动性顺序16. 检验、鉴别、除杂与分离是研究及获得物质的重要方法。下列实验方案不合理的是( )选项
实验目的
实验方案
A
检验氧气、二氧化碳
用带火星的木条分别伸入集气瓶
B
分离CaCO3和CaCl2
用水溶解、过滤、蒸发、烘干
C
除去H2中混有的少量水分
通过盛氢氧化钠固体的干燥管
D
鉴别Cu和Fe2O3
观察颜色
A、A B、B C、C D、D17. 逻辑推理是一种重要的化学思维方法,下列推理正确的是( )A、金刚石与石墨都是由碳元素组成的,所以它们的性质相同 B、化合物由不同种元素组成,所以不同种元素组成的纯净物一定是化合物 C、中和反应生成盐和水,所以凡是生成盐和水的反应都是中和反应 D、有机物是含有碳元素的化合物,所以含有碳元素的化合物一定是有机物18. 下列图象与对应的叙述相符合的是( )A、 a是充分加热一定质量的碳酸氢铵
B、
a是充分加热一定质量的碳酸氢铵
B、 b向一定量的氢氧化钠溶液中不断加水,溶液的pH变化
C、
b向一定量的氢氧化钠溶液中不断加水,溶液的pH变化
C、 c是将等质量的Mg和Fe、分别与溶质质量分数相同的足量稀硫酸反应
D、
c是将等质量的Mg和Fe、分别与溶质质量分数相同的足量稀硫酸反应
D、 d是向一定质量的盐酸和MgCl2的混合溶液中,逐滴加入NaOH溶液
d是向一定质量的盐酸和MgCl2的混合溶液中,逐滴加入NaOH溶液
二、填空题
-
19. 化学与我们的生活、生产、科技密切相关。(1)、厨房中常用的食材有大米、面粉、食用油、鸡蛋、青菜等,其中富含蛋白质的食材是。(2)、厨房中有洗菜用的塑料盆、装垃圾的塑料袋,切菜用的不锈钢刀等,其中不锈钢刀属于(填“有机合成材料”或“合金”)。(3)、防疫期间,人们常用84消毒液【主要成分为次氯酸钠(NaClO)】对生活场所进行杀菌、消毒。工业制备NaClO的反应原理为 ,则X的化学式为。(4)、海水中蕴藏着丰富的化学资源,海水中含量最多的阴离子是(填离子符号)。20. 下表是元素周期表的一部分。请回答下列问题:
 (1)、若锂元素在周期表中的位置可表示为“第2周期IA族”,则地壳中含量最高的金属元素在周期表中的位置可表示为 , 该金属元素与“第2周期ⅥA族”元素组成化合物的化学式是。(2)、X2-与Ar的核外电子排布相同,则x与钠形成化合物的化学式是。(3)、周期表中A元素的原子在化学变化中容易(填“得”或“失”)电子形成化合物。(4)、图1是硒元素周期表中的一部分,图2是硒原子的结构示意图,则硒原子的核外电子数是 , 最外层电子数n= , 则硒元素在周期表的位置是(填“C、D”中一项)。
(1)、若锂元素在周期表中的位置可表示为“第2周期IA族”,则地壳中含量最高的金属元素在周期表中的位置可表示为 , 该金属元素与“第2周期ⅥA族”元素组成化合物的化学式是。(2)、X2-与Ar的核外电子排布相同,则x与钠形成化合物的化学式是。(3)、周期表中A元素的原子在化学变化中容易(填“得”或“失”)电子形成化合物。(4)、图1是硒元素周期表中的一部分,图2是硒原子的结构示意图,则硒原子的核外电子数是 , 最外层电子数n= , 则硒元素在周期表的位置是(填“C、D”中一项)。
 21. 我国是世界上第一个在海域成功试采可燃冰的国家,可燃冰主要含甲烷水合物,用作燃料时反应的微观示意图如图,据图示回答下列有关问题:
21. 我国是世界上第一个在海域成功试采可燃冰的国家,可燃冰主要含甲烷水合物,用作燃料时反应的微观示意图如图,据图示回答下列有关问题: (1)、甲烷是最简单的(填“无机物”或“有机物”);(2)、据上图所示,说明在化学反应中,可分而不可分。(3)、该反应的化学方程式是。22. 为探究硝酸钾的溶解性,进行了如图实验(见图I),结合KNO3溶解度曲线(见图Ⅱ)判断,回答下列问题。
(1)、甲烷是最简单的(填“无机物”或“有机物”);(2)、据上图所示,说明在化学反应中,可分而不可分。(3)、该反应的化学方程式是。22. 为探究硝酸钾的溶解性,进行了如图实验(见图I),结合KNO3溶解度曲线(见图Ⅱ)判断,回答下列问题。
 (1)、溶液①、③一定是所处温度下的不饱和溶液的是(填数字序号)。(2)、溶液②、④的浓度(填“相等”或“不相等”)。(3)、30℃时145.8g硝酸钾的饱和溶液降温至20℃会有g硝酸钾结晶析出。(4)、20℃时溶液②中硝酸钾溶液的浓度是(精确到1%)。(5)、据图所示,要使硝酸钾溶液中硝酸钾结晶析出,通常采用的方法。23. 水是生命之源,是人类最宝贵的自然资源。(1)、生活中通常采用的方法降低水的硬度,同时还能杀菌、消毒。(2)、下列做法会造成水体污染的是 (填字母序号)。A、工业废水经处理达标后排放 B、用洗衣水冲马桶 C、随意丢弃废旧电池24. 已知硝酸铵的化学式是:NH4NO3 , 据此回答下列问题:(1)、一个硝酸铵分子中是由个原子构成;硝酸铵的相对分子质量是。(2)、硝酸铵中氮元素的质量分数是。
(1)、溶液①、③一定是所处温度下的不饱和溶液的是(填数字序号)。(2)、溶液②、④的浓度(填“相等”或“不相等”)。(3)、30℃时145.8g硝酸钾的饱和溶液降温至20℃会有g硝酸钾结晶析出。(4)、20℃时溶液②中硝酸钾溶液的浓度是(精确到1%)。(5)、据图所示,要使硝酸钾溶液中硝酸钾结晶析出,通常采用的方法。23. 水是生命之源,是人类最宝贵的自然资源。(1)、生活中通常采用的方法降低水的硬度,同时还能杀菌、消毒。(2)、下列做法会造成水体污染的是 (填字母序号)。A、工业废水经处理达标后排放 B、用洗衣水冲马桶 C、随意丢弃废旧电池24. 已知硝酸铵的化学式是:NH4NO3 , 据此回答下列问题:(1)、一个硝酸铵分子中是由个原子构成;硝酸铵的相对分子质量是。(2)、硝酸铵中氮元素的质量分数是。三、综合题
-
25. 小明同学在实验操作考核中,要完成的题目是“二氧化碳的制取、收集和验满”。
 (1)、如图所示是实验桌上摆放好的该实验所需的用品,小明同学发现其中缺少了一种实验仪器和一种药品,请你写出所缺仪器的名称;所缺药品是。(2)、写出制取二氧化碳气体反应的化学方程式:。26. 实验室常用如图所示装置来制取气体。
(1)、如图所示是实验桌上摆放好的该实验所需的用品,小明同学发现其中缺少了一种实验仪器和一种药品,请你写出所缺仪器的名称;所缺药品是。(2)、写出制取二氧化碳气体反应的化学方程式:。26. 实验室常用如图所示装置来制取气体。
 (1)、实验室用过氧化氢分解制取氧气,选用的发生装置是(填字母序号)。(2)、若用C装置收集二氧化碳气体,气体应从(填“a”或“b”)端进入。(3)、实验室里用装置D制取氢气,其反应的化学方程式是。27. 通过对初中化学的学习,某化学兴趣小组对金属钠的性质开展了探究活动。
(1)、实验室用过氧化氢分解制取氧气,选用的发生装置是(填字母序号)。(2)、若用C装置收集二氧化碳气体,气体应从(填“a”或“b”)端进入。(3)、实验室里用装置D制取氢气,其反应的化学方程式是。27. 通过对初中化学的学习,某化学兴趣小组对金属钠的性质开展了探究活动。【查阅资料】
①钠贮存在煤油中,Na2O2是淡黄色固体
②
③
④CaCl2溶液pH=7,Na2CO3溶液的pH>7
【实验探究】
(1)、实验一:在盛有水的烧杯中滴入几滴酚酞溶液,把一块绿豆大小的金属钠(用滤纸吸干表面的煤油后,用刀切去表面的外皮)投入烧杯中。观察到钠浮在水面上,熔化成闪亮的小球且在水面上迅速游动,发出“嘶嘶”的响声,反应后溶液呈红色。①从实验现象可知,钠的物理性质有:A.固体;B.硬度小;C.密度比水小;D。
②烧杯中的溶质除酚酞外还含有(填化学式)。
③取少量烧杯中的溶液于试管中,然后向试管中滴加某溶液至红色恰好消失(无其它现象),则滴加的是(填化学式)溶液。
(2)、实验二:另取一小块钠(如实验一处理)放在石棉网上灼烧,金属钠燃烧并产生黄色火焰,最后生成淡黄色固体(填化学式)。将淡黄色固体露置于空气中,一段时间后变为白色粉末。同学们依据查阅资料、经过讨论,认为该白色粉末可能是:I .NaOH;Ⅱ.Na2CO3;Ⅲ.NaOH、Na2CO3
为确定该白色粉末的成分,又进行如下实验:
实验步骤
实验现象
实验结论
①取少量白色粉末于试管中,加水充分溶解,滴加过量的溶液,振荡
产生白色沉淀
综合实验现象判断,此白色粉末是Na2CO3 , 发生反应的化学方程式
②静止后,向上层清液中滴加少量溶液
无明显现象
【实验结论】固体同时与气体和水分反应时,固体与气体会先发生反应。
28. 北京冬奥会开幕式精妙绝伦、美轮美奂。如图所示“五环”中相交两环中的物质间能够发生化学反应,其中A、B、C、D分别是NaOH、Fe、CuO、CuSO4中的一种,C溶液能使紫色石蕊溶液变蓝,D是氧化物。 (1)、B的化学式是。(2)、发生中和反应反应的化学方程式是:。29.(1)、在通常情况下,燃烧需要三个条件:;氧气(或空气);达到燃烧所需的最低温度(也叫着火点)。(2)、下面是探究燃烧条件的实验,请你根据实验图示和资料信息回答有关问题。
(1)、B的化学式是。(2)、发生中和反应反应的化学方程式是:。29.(1)、在通常情况下,燃烧需要三个条件:;氧气(或空气);达到燃烧所需的最低温度(也叫着火点)。(2)、下面是探究燃烧条件的实验,请你根据实验图示和资料信息回答有关问题。资料信息:白磷和红磷的着火点分别是40℃、240℃。

①铜片上的红磷不燃烧,是因为。
②烧杯中水的作用一方面 , 另一方面。
(3)、为了防止失火造成生命财产的损害,加油站等场所常贴有下列图标,其中表示“禁止吸烟”的是 (填字母序号)。 30. 某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下图:
30. 某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下图:
资料1:垃圾焚烧产生的烟气中含有SO2等有害气体,CaSO3是白色沉淀。
资料2:铁锈的主要成分是Fe2O3 , FeSO4容易被空气中的O2氧化。
回答下列问题:
(1)、将所得FeSO4溶液在氮气环境中蒸发浓缩、降温结晶、过滤,得到FeSO4晶体,其中氮气的作用是。(2)、政府倡导垃圾分类,其好处是(任写一点):。(3)、石灰浆吸收SO2(性质与CO2相似)的化学反应方程式为。(4)、稀硫酸溶解生锈的铁制品(主要含铁,还有氧化铁等)生成硫酸亚铁的过程中会同时发生复分解反应、置换反应和化合反应,写出发生化合反应的化学反应方程式。四、计算题
-
31. 某种铁合金中含有不溶于酸的杂质。取该合金样品粉末22.8g,分四次向其中加入稀硫酸共200g。反应过程的有关数据记录如表。
次序
第1次
第2次
第3次
第4次
加入稀硫酸的质量/g
50
50
50
50
产生氢气的质量/g
0.2
a
0.2
0.1
(1)、a=。(2)、计算稀硫酸中溶质的质量分数(请写出计算过程,计算结果精确到0.1%)。