山东省济宁市兖州区2022年中考二模化学试题
试卷更新日期:2022-05-27 类型:中考模拟
一、单选题
-
1. 下列物质的用途由化学性质决定的是( )A、干冰用于食品保鲜 B、活性炭作除味剂 C、生石灰干燥剂 D、汽油清洗油污2. 下列物质归类正确的是( )A、氧化铜、水、过氧化氢、氧气 氧化物 B、氯化钠、碳酸钾、硝酸银、硫酸铵 盐 C、烧碱、纯碱、熟石灰、生石灰 碱 D、甲烷、醋酸、乙醇、碳酸氢钠 有机物3. 化学源于生活,服务于生活,以下说法不合理的是( )A、煤燃烧产生的SO2排放是形成酸雨的原因之一,应禁止化石燃料的使用 B、长期饮用硬水不利于身体健康,可以用肥皂水区分硬水与软水 C、在潮湿的空气中铁易生锈,可以在铁制护栏表面涂刷油漆 D、用灼烧的方法可以鉴别棉线和羊毛线4. 下列各组离子在溶液中能大量共存的是( )A、Na+、H+、Cl﹣、OH﹣ B、Ag+、K+、Cl﹣、 C、Na+、H+、NO3﹣、 D、H+、Mg2+、 、Cl﹣5. 下列关于硫酸的认识,正确的是( )A、组成:硫酸溶液中H+和SO 的数目相同 B、性质:能与CO2、SO3等非金属氧化物反应 C、用途:可用于实验室制备CuSO4等硫酸盐 D、生产:含硫酸废水用CaCl2处理后直接排放6. 下列实验方案正确的是( )
序号
实验目的
实验方案
A
鉴别NH4Cl和KCl两种白色固体肥料
加入熟石灰研磨后闻气味
B
鉴别CO2和N2
将燃着的木条分别伸入气体中,观察现象
C
除去CO2中混有的少量CO
将气体通过灼热铜丝网
D
除去氢氧化钠溶液中的碳酸钠
加入过量的石灰水,充分反应后过滤
A、A B、B C、C D、D7. 我国科研人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图。下列说法正确的是( ) A、甲的相对分子质量为6 B、一个丙分子中含有4个氢原子 C、参加反应的甲与乙的质量比为3∶1 D、氢元素的化合价在反应前后没有发生改变8. 现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是( )
A、甲的相对分子质量为6 B、一个丙分子中含有4个氢原子 C、参加反应的甲与乙的质量比为3∶1 D、氢元素的化合价在反应前后没有发生改变8. 现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是( )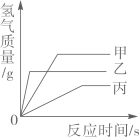 A、完全反应所需时间:丙>甲>乙 B、生成氢气的质量:甲>乙>丙 C、相对原子质量:乙>丙>甲 D、消耗硫酸的质量:甲>乙>丙9. A、B、C三种固体物质的溶解度曲线如图所示,下列问题说法错误的是( )
A、完全反应所需时间:丙>甲>乙 B、生成氢气的质量:甲>乙>丙 C、相对原子质量:乙>丙>甲 D、消耗硫酸的质量:甲>乙>丙9. A、B、C三种固体物质的溶解度曲线如图所示,下列问题说法错误的是( ) A、t1℃时,A,B,C三种物质中溶解度最大的是B B、t1℃时,C的饱和溶液的溶质质量分数为25% C、t1℃时,在盛有100克水的烧杯中,加入50克B物质,充分溶解后,得到溶液的质量为140g D、将t1℃的A,B,C三种饱和溶液分别升温至t2℃,所得溶液中溶质质量分数由大到小的顺序是B>A>C10. 稀盐酸与氢氧化钠溶液反应时溶液pH的变化如图所示。下列说法正确的是( )
A、t1℃时,A,B,C三种物质中溶解度最大的是B B、t1℃时,C的饱和溶液的溶质质量分数为25% C、t1℃时,在盛有100克水的烧杯中,加入50克B物质,充分溶解后,得到溶液的质量为140g D、将t1℃的A,B,C三种饱和溶液分别升温至t2℃,所得溶液中溶质质量分数由大到小的顺序是B>A>C10. 稀盐酸与氢氧化钠溶液反应时溶液pH的变化如图所示。下列说法正确的是( ) A、该图所对应操作是将氢氧化钠溶液滴入稀盐酸中 B、n点表示的溶液中的微粒只有Na+和Cl- C、P点所示溶液中的溶质为NaOH D、该反应的基本类型是中和反应
A、该图所对应操作是将氢氧化钠溶液滴入稀盐酸中 B、n点表示的溶液中的微粒只有Na+和Cl- C、P点所示溶液中的溶质为NaOH D、该反应的基本类型是中和反应二、填空题
-
11. 化学基础与常识(1)、保持水的化学性质的最小粒子是(用符号表示,下同):(2)、NH4NO3水溶液中大量存在的阳离子是。(3)、碳单质可用于冶金工业,是利用了它的性;12. 分类、类比、推理是学习化学的常用方法。(1)、随着科学研究的进展,化学实验的方法也从定性到定量发生了质的转变。若按实验方法分类,应将实验D和(填字母)分为一类,依据是。
 (2)、①观察所给粒子排列规律,将合适的化学符号填入空白:O2-、F-、、Na+、Mg2+。
(2)、①观察所给粒子排列规律,将合适的化学符号填入空白:O2-、F-、、Na+、Mg2+。②类比金属单质间的置换反应,某些非金属单质间也能发生置换反应,如Cl2比Br2活泼,能与HBr发生反应:Cl2+2HBr=2HCl+Br2已知Cl2比N2活泼,则Cl2与NH3在一定条件下发生反应的化学方程式为。
13. CO2是一种酸性氧化物。为探究CO2和NaOH发生化学反应,某同学选用了下列两种装置进行实验,都证明了CO2和NaOH确实发生了化学反应。请回答下列问题: (1)、选择装置I时,可观察到的实验现象为:。(2)、选择装置Ⅱ时,可观察到烧杯内的水沿着导管倒流入锥形瓶中,产生该实验现象的原因是:。(3)、CO2和NaOH溶液反应的化学方程式为。14. 葡萄糖经过肠壁吸收进入血液称为血糖,为人体组织提供能量。已知葡萄糖的化学式为C6H12O6。(1)、一个葡萄糖分子由个原子构成;(2)、葡萄糖中碳元素的质量分数为。
(1)、选择装置I时,可观察到的实验现象为:。(2)、选择装置Ⅱ时,可观察到烧杯内的水沿着导管倒流入锥形瓶中,产生该实验现象的原因是:。(3)、CO2和NaOH溶液反应的化学方程式为。14. 葡萄糖经过肠壁吸收进入血液称为血糖,为人体组织提供能量。已知葡萄糖的化学式为C6H12O6。(1)、一个葡萄糖分子由个原子构成;(2)、葡萄糖中碳元素的质量分数为。三、综合题
-
15. 某品牌电器的废旧电路板中还有Fe、Cu、Ag、Ni(镍,银白色金属)等金属,如下图是某车间回收部分金属的工艺流程,已知 。

回答下列问题。
(1)、滤渣③中含有的金属是。(2)、根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱顺序是NiFe(填“>”或“<”)。(3)、滤液③中加入足量铁粉的主要目的是 , 固体A除主要含有铜外,还含有一定量的铁,为了进一步提纯铜,可以向固体A中加入适量的稀硫酸,发生反应的化学方程式为。(4)、相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点是。16. 有一包白色固体样品,可能含氢氧化钠、硝酸钠、碳酸钠、硫酸钠、氯化钡中的一种或几种。小金同学为探究其成分完成了以下实验:①取少量白色固体溶于水,得到无色溶液,等分为两份;
②往一份无色溶液中加入稀硫酸,产生沉淀质量与所加稀硫酸质量关系如图所示;

③往另一份无色溶液中通入适量的CO2 , 产生白色沉淀。请回答:(用化学式填空)
(1)、仅根据②推测原样品中一定不存在的物质是;(2)、原样品的所有可能组成是 。17. 请回答下列问题。(1)、在实验室中,我们常用如图所示装置制取和收集某些气体。
①写出a仪器的名称:。
②实验室制取二氧化碳时,你选择的发生装置为 , 化学反应方程式为。
③经查阅资料,Na2O2(过氧化钠)通常情况下为淡黄色固体,能与水发生剧烈反应产生氧气。小明在实验室用Na2O2制取氧气时发生装置选择了B而没有选择C,你认为他选择的理由是。若用F装置收集氧气,进气端应选择端(用“b”或“c”填空)。
(2)、某化学兴趣小组用实验室常用药品(或溶液)对“NaOH溶液与稀盐酸是否恰好完全反应”进行探究。【实验探究】
方案I:某同学先向试管中加入约2 mLNaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。
①实验结论。
②从微观的角度分析,该反应的实质是。
③在滴入稀盐酸的过程中,若观察到有少量气泡出现,请分析产生气泡的可能原因。
方案Ⅱ:
实验步骤
实验现象
结论
取2 mLNaOH溶液于试管中,滴入一定量的稀盐酸,振荡后加入镁条
若
稀盐酸过量
若没有明显现象
NaOH溶液与稀盐酸恰好完全反应
(3)、【实验反思】①另有同学提出方案Ⅱ不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是。
②除以上方案外,下列哪些物质单独使用,也能证明“NaOH溶液与稀盐酸是否恰好完全反应”(填序号)。
A.铜片 B.pH试纸 C.氯化铜 D.紫色石蕊试液
四、计算题
-
18. 在锥形瓶中加入80.0g质量分数为10%的硫酸铜溶液,塞好橡胶塞。将几根铁钉用砂纸打磨干净后在天平上称得质量为56.0g,再将盛有硫酸铜溶液的锥形瓶和铁钉一起放在天平上称量,记录所称得质量m1 . 将上述铁钉浸到硫酸铜溶液中,待反应一段时间后溶液颜色改变时,将盛有硫酸铜溶液和锥形瓶放在天平上称量,记录所称的质量为m2。(1)、m1m2(填“>”或“=”或“<”)。(2)、锥形瓶的质量为(用含m1或m2的代数式表示)。(3)、若硫酸铜反应完全,求此时所得溶液的质量(写出计算结果)。