江苏省宿迁市泗阳县2022年中考二模化学试题
试卷更新日期:2022-05-27 类型:中考模拟
一、单选题
-
1. 争奇斗艳的物质世界充满了无穷的变化,下列变化中属于物理变化( )A、氧炔焰焊接金属 B、菠萝榨汁 C、石灰浆抹墙后变潮湿 D、铜器表面变绿2. 2022年北京冬奥会将于2月4日开幕,下列做法从微观角度解释不合理的是( )A、运动场上用水造冰——温度降低,分子停止运动 B、开幕式上舞台云雾——干冰升华,分子间隔发生改变 C、奥运村中日常消毒——消毒液挥发,分子在不断运动 D、天然气公交车出行——天然气燃烧,分子种类发生改变3. 下列关于“物质-分类-用途”的说法正确的是( )A、汞—非金属—用作温度计 B、纯碱—碱—制玻璃 C、消石灰—盐—作建筑材料 D、乙醇—有机物—作溶剂4. 化学是一门以实验为基础的学科,用下图能达到实验目的的是( )A、
 干燥CO2
B、
干燥CO2
B、 监控O2流速
C、
监控O2流速
C、 检验CO2
D、
检验CO2
D、 收集O2
5. 氧气是空气的主要成分之一,有关氧气说法错误的是( )A、液氧用于火箭发射,是由于氧气具有助燃性 B、用加热高锰酸钾的方法可以制取氧气 C、鱼类能在水中生活,证明氧气易溶于水 D、铁丝能在氧气中燃烧,火星四溅,产生黑色固体6. 下列对某一主题的知识归纳,有错误的是( )
收集O2
5. 氧气是空气的主要成分之一,有关氧气说法错误的是( )A、液氧用于火箭发射,是由于氧气具有助燃性 B、用加热高锰酸钾的方法可以制取氧气 C、鱼类能在水中生活,证明氧气易溶于水 D、铁丝能在氧气中燃烧,火星四溅,产生黑色固体6. 下列对某一主题的知识归纳,有错误的是( )A.化学与能源
B.化学与健康
①石油、煤、天然气都是不可再生能源
②太阳能、风能、氢能属于新能源
①糖类、油脂—组成元素完全相同
②碘、锌、硒—都是人体必需的微量元素
C.化学与生活
D.化学与安全
①喝汽水打嗝—气体溶解度随温度升高而增大
②木柴架空燃烧更旺—原理是增大了氧气的浓度
①重金属中毒—喝鲜牛奶、豆浆等解毒
②煤气泄漏—关闭气阀、严禁烟火
A、A B、B C、C D、D7. 下列各组物质在给定pH的溶液中能大量共存并形成无色溶液的是( )A、pH为3:FeCl3、NaOH、NaCl B、pH为10:BaCl2、Na2CO3、CuCl2 C、pH为5:BaCl2、NaHCO3、K2SO4 D、pH为1:NH4Cl、Na2SO4、HNO38. 如图1是甲、乙、丙三种固体物质的溶解度曲线,图2是对某物质的饱和溶液进行实验时的变化情况,下列描述正确的是( ) A、t1℃时,乙溶液和丙溶液的溶质质量分数一定相等 B、t3℃时,50g水中加入30g甲形成80g 溶液 C、将t3℃时甲、丙两种物质的饱和溶液降温至t2℃,两种溶液中溶质的质量分数:甲>丙 D、如图2滴入水后,饱和溶液变浑浊,则该饱和溶液的溶质是甲9. 下列实验方案,操作能达到实验目的的是( )
A、t1℃时,乙溶液和丙溶液的溶质质量分数一定相等 B、t3℃时,50g水中加入30g甲形成80g 溶液 C、将t3℃时甲、丙两种物质的饱和溶液降温至t2℃,两种溶液中溶质的质量分数:甲>丙 D、如图2滴入水后,饱和溶液变浑浊,则该饱和溶液的溶质是甲9. 下列实验方案,操作能达到实验目的的是( )选项
实验目的
实验操作
A
检验某未知溶液是否有
加入氯化钡溶液有白色沉淀,再加稀硝酸,沉淀不消失
B
鉴别NH4NO3和尿素
分别取少量固体与研钵中,加熟石灰研磨
C
除去部分变质的NaOH中的杂质
加水溶解,滴加适量的CaCl2溶液
D
分离CaCO3、CuCl2、NaCl
依次加入:水、NaOH、稀硫酸
A、A B、B C、C D、D10. 已知溶液A中含NaCl、Na2SO4、Mg(NO3)2、CuCl2中的一种或几种,溶液B中含NaOH、Ba(NO3)2中的一种或两种。小宝同学对两组溶液的成分进行了如下探究:Ⅰ.取一定量的A、B混合,产生白色沉淀,过滤,得沉淀C和无色溶液D;
Ⅱ.向沉淀C中滴加过量的稀盐酸,沉淀部分溶解,得溶液E结合以上探究过程,下列说法正确的是( )
A、由步骤1可知,溶液A中一定不含CuCl2 B、溶液B中只有一种溶质 C、白色沉淀C是纯净物 D、无色溶液D中一定含有Na+、Cl-、二、填空题
-
11. 化学与科技、生产、生活密切相关。(1)、西红柿炖牛肉味道鲜美,营养丰富。牛肉中富含的营养素是;西红柿中含维生素C,缺少维生素C会引起。(2)、智能发热抗寒服是用石墨烯电热薄膜技术制作而成。石墨烯是碳的纳米单质,石墨烯(C)与氧化铜反应生成一种单质和一种能使澄清石灰水变浑浊的气体,请写出该化学方程式。(3)、“嫦娥四号”探测到月慢中含橄榄石(主要成分Mg2SiO4),Mg2SiO4中硅元素的化合价是 , 写出其中所含金属离子的符号是。(4)、西藏旅游时“高原缺氧”中的“氧”是指(填“氧分子”、“氧元素”或“氧原子”)。
三、综合题
-
12. 人类文明的发展和社会的进步与材料密切相关。请根据相关信息回答下列问题:(1)、解码智慧冬奥:
①2022年北京冬奥会,硫化镉发电玻璃成为绿色和科技办奥交汇的创新点。如图是碲原子的结构示意图


则碲元素在元素周期表中位于第周期,属于元素(填“金属”或“非金属”),其相对原子质量是。
②氢能“黑科技”亮相北京冬奥会。冬奥会“飞扬”火矩科技亮点之一是采用氢气作为燃料,其优点是(写一点)
③冬奥会国家速滑馆“冰丝带”采用面向未来的单层双向正交马鞍形索网结构,减少屋顶所用钢材2800吨。金属资源储量有限,钢铁生锈是世界面临的难题。铁生锈的主要条件是铁与同时接触。
(2)、近年来,我国高铁建设飞速发展,建造高铁需要大量的钢铁。下图为模拟炼铁的装置,写出a中发生反应的化学方程式;描述b处反应的现象。 13. 我国化学家侯德榜发明了侯氏制碱法,为世界制碱工业技术发展作出杰出贡献。侯氏制碱法中重要的一步是向饱和食盐水中先后通入足量的氨气(极易溶于水)和二氧化碳制NaHCO3 , 某兴趣小组在实验室模拟该过程,结合具体步骤回答问题:
13. 我国化学家侯德榜发明了侯氏制碱法,为世界制碱工业技术发展作出杰出贡献。侯氏制碱法中重要的一步是向饱和食盐水中先后通入足量的氨气(极易溶于水)和二氧化碳制NaHCO3 , 某兴趣小组在实验室模拟该过程,结合具体步骤回答问题:
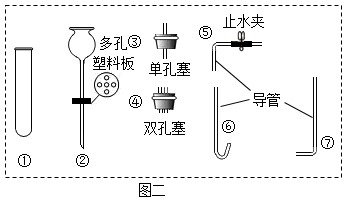 (1)、制备氨气。实验室常选择加热熟石灰和氯化铵固体混合物的方法制备氨气。制取氨气的发生装置可选图一中的装置。收集时能用图D方法的依据是:。(2)、制备二氧化碳气体。实验室常用稀盐酸和(填名称)反应制备二氧化碳,其化学方程式为:。选择图二中的可组装一套能控制反应发生和停止的制取二氧化碳的发生装置,其中用于添加液体药品的仪器名称是。(3)、配制饱和食盐水。步骤为:计算、称量、。该步骤需要用到的仪器有:。(4)、向饱和食盐水中先后通入足量的氨气和二氧化碳制备NaHCO3的化学方程式为: ,实验中,要先通氨气后通二氧化碳的原因是。14. 某化学兴趣小组的一个实验操作考题是:用碳酸钠溶液鉴别稀盐酸、食盐水和澄清石灰水。(1)、【进行实验】
(1)、制备氨气。实验室常选择加热熟石灰和氯化铵固体混合物的方法制备氨气。制取氨气的发生装置可选图一中的装置。收集时能用图D方法的依据是:。(2)、制备二氧化碳气体。实验室常用稀盐酸和(填名称)反应制备二氧化碳,其化学方程式为:。选择图二中的可组装一套能控制反应发生和停止的制取二氧化碳的发生装置,其中用于添加液体药品的仪器名称是。(3)、配制饱和食盐水。步骤为:计算、称量、。该步骤需要用到的仪器有:。(4)、向饱和食盐水中先后通入足量的氨气和二氧化碳制备NaHCO3的化学方程式为: ,实验中,要先通氨气后通二氧化碳的原因是。14. 某化学兴趣小组的一个实验操作考题是:用碳酸钠溶液鉴别稀盐酸、食盐水和澄清石灰水。(1)、【进行实验】实验步骤
实验现象
实验结论
分别用a、b、c三支试管取样,各加入一定量碳酸钠溶液
a中
a中物质是稀盐酸
b中无明显现象
b中物质是食盐水
c中
c中物质是澄清石灰水
把c试管反应后的物质进行过滤,得到滤液。
(2)、【提出问题】滤液中溶质的成分是什么?猜想一:NaOH和Na2CO3;
猜想二:NaOH;
猜想三:。
提示:Ca(OH)2微溶于水。
(3)、【实验过程】为证明猜想一是否正确,进行了如下实验:实验步骤
实验现象
实验结论
取一定量滤液于试管中,加入一种盐溶液(写溶质化学式)。
有白色沉淀
猜想一正确
写出上述有白色沉淀生成的化学方程式。
(4)、同学们还对a试管反应后废液的酸碱性感兴趣,决定用pH试纸测定其pH值用pH试纸测定a试管反应后废液酸碱性的过程
测定结果
pH=3
(5)、【反思与交流】a试管中的废液显(填“酸性”、“碱性”、“中性”),从环保、经济、操作简便等方面考虑,应向废液加入(写化学式)后再排放。15. 某工厂废液中含有氯化钠、氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如图所示:
请回答下列问题:
(1)、工厂废液中加入过量A反应的化学方程式为。(2)、用化学式表示固体甲的成分。(3)、加入过量B发生反应的基本类型是。(4)、完成步骤④的化学方程式: 。四、计算题
-
16. 某化学兴趣小组的同学为测定假黄金(铜锌合金)中锌的质量,取20克假黄金置于烧杯中,取120克稀盐酸,分6次加入,充分反应,实验数据如下:
实验次序
1
2
3
4
5
6
加入稀盐酸的质量/g
20
20
20
20
20
20
剩余固体的质量/g
18.7
m
16.1
14.8
13.5
13.5
请回答:
(1)、表中m=。(2)、假黄金(铜锌合金)中锌的质量分数是。(3)、所用稀盐酸中溶质的质量分数是?(写出计算过程)
-