广东省梅州市2022年中考一模化学试题
试卷更新日期:2022-05-27 类型:中考模拟
一、单选题
-
1. 下列梅州市非物质文化遗产制作过程涉及化学变化的是( )A、五华石雕 B、客家酿酒 C、蕉岭竹编 D、埔寨纸花2. 垃圾分类是新时尚。饮用后的空矿泉水瓶应投入( )A、
 B、
B、 C、
C、 D、
D、 3. 下列科学家与其贡献对应正确的是( )A、拉瓦锡一原子论 B、道尔顿—元素周期表 C、张青莲一提取青蒿素 D、侯德榜一侯氏制碱法4. 新的一天从营养丰富的早餐开始。下列食物富含蛋白质的是( )A、鸡蛋 B、白粥 C、苹果 D、馒头5. 下列属于复合肥料的是( )A、NH4Cl B、CO(NH2)2 C、Ca(H2PO4)2 D、KNO36. 下列说法错误的是( )A、铁在潮湿的空气中容易生锈 B、食品包装中充O2以防腐 C、SO2是空气主要污染物 D、金属的活动性:Zn>Fe>Cu7. 化学使生活更美好。下列做法合理的是( )A、用甲醛保鲜食品 B、用水浇灭炒菜时锅里油着火 C、用洗清精洗涤餐具上的油污 D、用浓硫酸作食品干燥剂8. 实验室某四个试剂橱已存放如下药品,实验员新购进一些苏打,应将它放进( )
3. 下列科学家与其贡献对应正确的是( )A、拉瓦锡一原子论 B、道尔顿—元素周期表 C、张青莲一提取青蒿素 D、侯德榜一侯氏制碱法4. 新的一天从营养丰富的早餐开始。下列食物富含蛋白质的是( )A、鸡蛋 B、白粥 C、苹果 D、馒头5. 下列属于复合肥料的是( )A、NH4Cl B、CO(NH2)2 C、Ca(H2PO4)2 D、KNO36. 下列说法错误的是( )A、铁在潮湿的空气中容易生锈 B、食品包装中充O2以防腐 C、SO2是空气主要污染物 D、金属的活动性:Zn>Fe>Cu7. 化学使生活更美好。下列做法合理的是( )A、用甲醛保鲜食品 B、用水浇灭炒菜时锅里油着火 C、用洗清精洗涤餐具上的油污 D、用浓硫酸作食品干燥剂8. 实验室某四个试剂橱已存放如下药品,实验员新购进一些苏打,应将它放进( )橱名
甲
乙
丙
丁
试剂
盐酸、硫酸
烧碱、苛性钾
食盐、氯化钡
酒精、汽油
A、甲 B、乙 C、丙 D、丁9. 我国载人航天工程使用了液氢、煤油、新型镁铝合金等物质。下列说法错误的是( )A、液氢和煤油都属于可再生能源 B、可通过石油加热炼制得到煤油 C、可用锌和稀硫酸反应制取氢气 D、镁铝合金的硬度比镁、铝的大10. 敦煌壁画色彩艳丽,其蓝色源于石青【Cu3(OH)2(CO3)2】。石青中铜元素的化合价是( )A、+1 B、+2 C、+3 D、+411. 铷原子钟为我国北斗导航卫星系统提供精确的时间。结合图,下列说法正确的是( )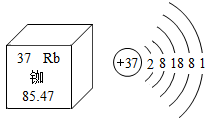 A、铷元素属于非金属元素 B、铷原子的质子数等于中子数 C、铷元素的化学性质与钠元素相似 D、铷元素的相对原子质量为85.47g12. 欲配制质量分数为10%的NaCl溶液,下列有关操作正确的是( )A、取固体
A、铷元素属于非金属元素 B、铷原子的质子数等于中子数 C、铷元素的化学性质与钠元素相似 D、铷元素的相对原子质量为85.47g12. 欲配制质量分数为10%的NaCl溶液,下列有关操作正确的是( )A、取固体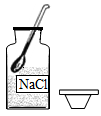 B、称固体
B、称固体 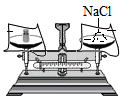 C、量取水
C、量取水 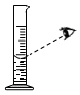 D、溶解
D、溶解  13. 梅州金柚是国家地理标志产品,富含维生素C(化学式为C6H8O6)。下列有关维生素C的说法正确的是( )A、是有机化合物 B、碳元素和氧元素质量比为1:1 C、由20个原子构成 D、碳元素的质量分数最大14. 如图为物质M的溶解度曲线图,下列有关说法正确的是( )
13. 梅州金柚是国家地理标志产品,富含维生素C(化学式为C6H8O6)。下列有关维生素C的说法正确的是( )A、是有机化合物 B、碳元素和氧元素质量比为1:1 C、由20个原子构成 D、碳元素的质量分数最大14. 如图为物质M的溶解度曲线图,下列有关说法正确的是( ) A、t1℃时,M的饱和溶液的溶质质量分数为20% B、t2℃a点溶液中溶质与溶剂的质量比为3:7 C、将b点的M溶液降低温度至t1℃,溶液恰好饱和 D、t2℃→t1℃时,M的饱和溶液析出晶体10g15. 下列除去杂质所选用的方法正确的是( )
A、t1℃时,M的饱和溶液的溶质质量分数为20% B、t2℃a点溶液中溶质与溶剂的质量比为3:7 C、将b点的M溶液降低温度至t1℃,溶液恰好饱和 D、t2℃→t1℃时,M的饱和溶液析出晶体10g15. 下列除去杂质所选用的方法正确的是( )选项
物质(括号内为杂质)
除杂方法
A
CH4(CO)
点燃
B
KCl固体(MnO2固体)
加足量水搅拌,过滤,蒸发
C
NaOH溶液(Na2CO3)
加入适量稀盐酸
D
铜粉(锌粉)
加入适量的硫酸亚铁溶液
A、A B、B C、C D、D二、填空题
-
16. 第24届冬奥会在北京圆满落幕,北京作为双奥之城不断向世界展示绿色奥运理念。(1)、冬奥火炬“飞扬”采用氢气做燃料。
①冬奥火炬燃烧时实现“零排放”的原因是。
②将氢气存储在高压燃料罐中,分子间间隔变(选填“大”或“小”)。火炬传递结束后,采用关闭燃料阀门的方法熄灭火炬,其中蕴含的灭火原理是。
③冬奥火炬外壳制作需先“织”好碳纤维外壳“骨架”,然后向里注入特殊树脂,固化成型,再经过打磨、喷漆、镭雕等环节制成。火炬的外壳材料属于材料(填“金属”或“复合”)。
(2)、本次冬奥会使用二氧化碳作为制冷剂。此措施减少的碳排放总量相当于种植超过120万棵树。若大气中二氧化碳排放过多会导致;固体二氧化碳俗称。(3)、奥运选手参加开幕式均需佩戴口罩,以阻挡飞沫、病毒等物质,此原理相当于化学实验操作中的。17. 我国纪念2022年“世界水日”“中国水周”活动主题为“推进地下水超采综合治理复苏河湖生态环境”。请回答下列与水有关的问题。(1)、生活中可用检验硬水和软水,可用的方法降低水的硬度。(2)、自来水厂常利用活性炭的性,除去水中的色素和异味。(3)、图1为电解水的实验装置图。电解时,水中需加入少量的NaOH,电解后溶液的pH(选填“增大”或“变小”)。你认为生活中可采收节约用水的措施是(写一种)。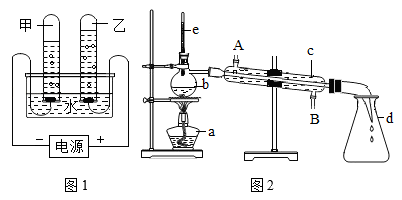 (4)、在实验室可用如图2装置制取蒸馏水。冷水从(填“A”成“B”)进入c仪器,在b中加入少许碎瓷片的作用是。
(4)、在实验室可用如图2装置制取蒸馏水。冷水从(填“A”成“B”)进入c仪器,在b中加入少许碎瓷片的作用是。三、综合题
-
18. 根据图中的实验装置回答。
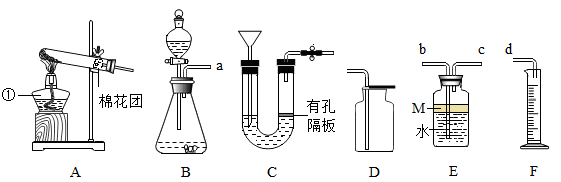 (1)、写出仪器①的名称。(2)、实验室用A装置制取O2 , 该反应的化学方程式为;用D装置收集O2时,验满的方法是。(3)、关于CO2:
(1)、写出仪器①的名称。(2)、实验室用A装置制取O2 , 该反应的化学方程式为;用D装置收集O2时,验满的方法是。(3)、关于CO2:①若用C装置制取CO2 , 优点是。
②若用B、E、F装置组合测定生成CO2的体积,则装置接口顺序为a→→→d(填b、c顺序),为防止CO2溶于水,M物质可以是。
(4)、若B装置中的反应过于剧烈,从安全角度考虑,可以采取的措施有(多选,填字母序号)。a、用容积较小的锥形瓶
b、减慢液体的滴加速度
c、加热反应物
d、用水稀释液体反应物
19. 将一小块银白色的金属钠放置在空气中会发生下例变化:【提出问题】常温下钠与氧气反应,产物有哪些?
【查阅资料】钠的氧化物有氧化钠和过氧化钠(Na2O2)两种,氧化钠与水发生反应的化学方程式如下:
(1)、过氧化钠也能与水反应,化学方程式为 ,X的化学式为;从过氧化钠与水反应的产物可推测,过氧化钠可用于潜水艇的(填“供氧剂”或“供氢剂”)(2)、【提出猜想】常温下钠与氧气反应的产物可能是:猜想I:Na2O猜想Ⅱ:猜想Ⅲ:Na2O和Na2O2。
【实验探究一】
实验操作
实验现象
实验结论
取少量常温下钠与氧气反应的产物于试管中并加入足量蒸馏水
固体溶解,不产生气泡
猜想正确
(3)、【继续探究】钠在空气中放置一段时间后得到白色固体的成分是什么?【提出猜想】猜想一:Na2CO3猜想二:Na2CO3和NaOH。
【实验探究二】
实验操作
实现现象
实验结论
a.取少量白色固体于试管中并加入足量
产生白色沉淀
猜想二正确
b.将上述沉淀过滤,取少量滤液于试管中并加入
(4)、类比氧化铁与盐酸的反应,与出氧化钠与盐酸反应的化学方程式。20. 我国力争2030年前实现“碳达峰”,2060年前实现“碳中和”。图是某厂为实现该目标设计的利用氢氧化钠溶液“捕集”一氧化碳的主要技术流程。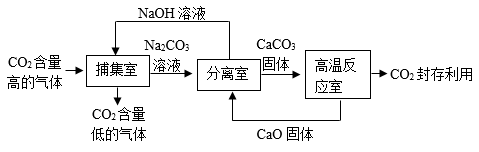 (1)、捕集室中发生反应的化学方程式为 , 捕集室中采用喷淋方式加入NaOH溶液,其优点是。(2)、整个设计流程中,可循环利用的物质是、(写化学式)。(3)、分离室发生的反应为 和(用化学方程式表示)。(4)、高温反应室发生的反应属于反应(填基本反应类型)。(5)、CO2与H2在催化条件下反应生成甲醇,其微观示意图如图所示。请在图框中补画齐全分子的模型与数目。
(1)、捕集室中发生反应的化学方程式为 , 捕集室中采用喷淋方式加入NaOH溶液,其优点是。(2)、整个设计流程中,可循环利用的物质是、(写化学式)。(3)、分离室发生的反应为 和(用化学方程式表示)。(4)、高温反应室发生的反应属于反应(填基本反应类型)。(5)、CO2与H2在催化条件下反应生成甲醇,其微观示意图如图所示。请在图框中补画齐全分子的模型与数目。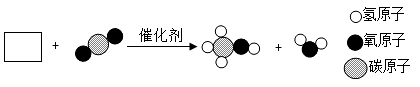 21. 某校化学研究小组利用数字化技术对初中化学常见的实验进行深究活动,请回答:
21. 某校化学研究小组利用数字化技术对初中化学常见的实验进行深究活动,请回答: (1)、为比较块状碳酸钙和碳酸钙粉末与稀盐酸反应的速率,进行了如图1”所示实验,并用压强传感器测得锥形瓶内气压变化情况如图2所示。
(1)、为比较块状碳酸钙和碳酸钙粉末与稀盐酸反应的速率,进行了如图1”所示实验,并用压强传感器测得锥形瓶内气压变化情况如图2所示。①C数值为。曲线(选填“I”或“Ⅱ”)表示的是碳酸钙粉末与稀盐酸反应的气压变化。
②对比分析如图2中(选填“a”、“b”、“c”或“d”)两点实验数据,可比较出两锥形瓶内的反应速率快慢。
(2)、研究小组称取了mg大理石样品,将100g稀盐酸逐滴滴入样品中,实验过程中剩余固体与加入稀盐酸的质量关系如图3(假设杂质不反应,也不溶于水)①大理石样品m的值是。
②计算反应结束时生成二氧化碳的质量(写出计算过程)。