浙江省温州市环大罗山联盟2021-2022学年高二下学期期中联考化学试题
试卷更新日期:2022-05-19 类型:期中考试
一、单选题
-
1. 下列分析方法中不是现代化学测定有机物结构的是:( )A、燃烧法 B、红外光谱法 C、紫外光谱法 D、核磁共振谱法2. 为验证某有机物属于烃的含氧衍生物,下列方法正确的是( )A、验证其完全燃烧后的产物只有H2O和CO2 B、测定其燃烧产物中H2O和CO2的物质的量之比 C、测定其完全燃烧时消耗有机物的物质的量分别与生成的H2O和CO2的物质的量之比 D、测定该试样的质量及试样完全燃烧后生成的H2O和CO2的质量3. 下列分子式只表示一种物质的是( )A、C3H8 B、C3H7Cl C、C2H6O D、C4H104. 下列表示错误的是( )A、丙烯酸的结构简式: B、2-丁醇的键线式:
 C、羟基的电子式:
C、羟基的电子式:  D、二甲醚的球棍模型:
D、二甲醚的球棍模型:  5. 下列关于物质用途的说法正确的是( )A、甲醛的水溶液可用于防腐 B、丙三醇可用于配制汽车防冻液 C、卤代烃不可用作灭火剂 D、酚类化合物有毒,不能用于杀菌消毒6. 下列关于有机反应类型的判断错误的是( )A、 取代反应 B、 氧化反应 C、 加成反应 D、HOCH2CH2CH2OH
5. 下列关于物质用途的说法正确的是( )A、甲醛的水溶液可用于防腐 B、丙三醇可用于配制汽车防冻液 C、卤代烃不可用作灭火剂 D、酚类化合物有毒,不能用于杀菌消毒6. 下列关于有机反应类型的判断错误的是( )A、 取代反应 B、 氧化反应 C、 加成反应 D、HOCH2CH2CH2OH +H2O 消去反应
7. 下列说法错误的是( )A、苯的同系物都能使高锰酸钾褪色 B、 乙烷在光照条件下最多能与 发生取代反应 C、石油的催化裂化是为了提高汽油等轻质油品质 D、煤的直接或间接液化可获得甲醇等含氧有机物8. 下列说法正确的是( )A、足球烯和纳米碳管互为同分异构体 B、2-甲基丙烷和正戊烷互为同系物 C、 、 互为同素异形体 D、 和 互为同位素9. 下列说法错误的是( )A、萘(
+H2O 消去反应
7. 下列说法错误的是( )A、苯的同系物都能使高锰酸钾褪色 B、 乙烷在光照条件下最多能与 发生取代反应 C、石油的催化裂化是为了提高汽油等轻质油品质 D、煤的直接或间接液化可获得甲醇等含氧有机物8. 下列说法正确的是( )A、足球烯和纳米碳管互为同分异构体 B、2-甲基丙烷和正戊烷互为同系物 C、 、 互为同素异形体 D、 和 互为同位素9. 下列说法错误的是( )A、萘( )不是苯的同系物,其一氯代物有2种
B、棉花、麻的主要成分是纤维素,蚕丝的主要成分是蛋白质
C、石油的常压蒸馏可以得到润滑油、石蜡、沥青等馏分
D、煤气化生成的可燃性气体中的 和 再经过催化合成可以转变为液体燃料
10. 我国女药学家屠呦呦因四十多年前发现了青蒿素,有效降低疟疾患者的死亡率,从而获得2015年诺贝尔生理学或医学奖.青蒿素的分子结构如图所示,下列有关青蒿素的有关说法正确的是( )
)不是苯的同系物,其一氯代物有2种
B、棉花、麻的主要成分是纤维素,蚕丝的主要成分是蛋白质
C、石油的常压蒸馏可以得到润滑油、石蜡、沥青等馏分
D、煤气化生成的可燃性气体中的 和 再经过催化合成可以转变为液体燃料
10. 我国女药学家屠呦呦因四十多年前发现了青蒿素,有效降低疟疾患者的死亡率,从而获得2015年诺贝尔生理学或医学奖.青蒿素的分子结构如图所示,下列有关青蒿素的有关说法正确的是( ) A、分子中所有碳原子可能处于同一平面上 B、分子中含氧官能团只有酯基 C、青蒿素的化学式是C15H22O5 D、青蒿素属于烃类有机物11. 下列说法正确的是( )A、主链上有5个碳原子的庚烷( )共有五种 B、烷烃的通式为 ,随 值增大,碳元素的质量分数逐渐减小 C、乙烯与溴发生加成反应的产物为溴乙烷 D、 苯恰好与 氢气加成,说明一个苯分子中有三个碳碳双键12. 有关
A、分子中所有碳原子可能处于同一平面上 B、分子中含氧官能团只有酯基 C、青蒿素的化学式是C15H22O5 D、青蒿素属于烃类有机物11. 下列说法正确的是( )A、主链上有5个碳原子的庚烷( )共有五种 B、烷烃的通式为 ,随 值增大,碳元素的质量分数逐渐减小 C、乙烯与溴发生加成反应的产物为溴乙烷 D、 苯恰好与 氢气加成,说明一个苯分子中有三个碳碳双键12. 有关 的说法正确的是( ) A、该物质在酸性条件下发生水解,其含苯环部分的水解产物所有碳原子一定在同一平面上 B、该物质中不含有手性碳原子 C、与足量NaOH溶液完全反应,可生成丙三醇 D、该物质在浓硫酸或NaOH水溶液条件下均可发生消去反应13. 下列能达到鉴别或提纯目的的是( )A、溴苯中混有溴,加入 溶液,用汽油萃取 B、酸性 溶液既可鉴别乙烷和乙烯,又可除去乙烷中少量的乙烯 C、乙烷中有乙烯,通入氢气在一定条件下反应,使乙烯转化为乙烷 D、己烷中溶有溴单质,可加足量氢氧化钠溶液,完全反应后分液14. 将“试剂”分别加入①、②两只试管中,不能完成“实验目的”的是( )
的说法正确的是( ) A、该物质在酸性条件下发生水解,其含苯环部分的水解产物所有碳原子一定在同一平面上 B、该物质中不含有手性碳原子 C、与足量NaOH溶液完全反应,可生成丙三醇 D、该物质在浓硫酸或NaOH水溶液条件下均可发生消去反应13. 下列能达到鉴别或提纯目的的是( )A、溴苯中混有溴,加入 溶液,用汽油萃取 B、酸性 溶液既可鉴别乙烷和乙烯,又可除去乙烷中少量的乙烯 C、乙烷中有乙烯,通入氢气在一定条件下反应,使乙烯转化为乙烷 D、己烷中溶有溴单质,可加足量氢氧化钠溶液,完全反应后分液14. 将“试剂”分别加入①、②两只试管中,不能完成“实验目的”的是( )实验目的
试剂
试管中的物质
A
醋酸的酸性强于苯酚
碳酸氢钠溶液
①醋酸②苯酚溶液
B
羟基对苯环的活性有影响
饱和溴水
①苯②苯酚溶液
C
甲基对苯环的活性有影响
酸性高锰酸钾溶液
①苯②甲苯
D
乙醇羟基中的氢原子不如水分子中的氢原子活泼
金属钠
①水②乙醇
A、A B、B C、C D、D15. 下列关于有机物的说法中,正确的一组是( )①“乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
②汽油、柴油和植物油都是碳氢化合物,完全燃烧只生成 和
③石油的分馏、煤的气化和液化都是物理变化
④淀粉和纤维素水解的最终产物都是葡萄糖
⑤将ag铜丝灼烧成黑色后趁热插入乙醇中,铜丝变红,再次称量质量等于ag
⑥除去甲烷中混有的少量乙烯,可将混合气体通过盛有溴水的洗气瓶
A、①③⑤⑥ B、④⑤⑥ C、③④⑤ D、②③④⑥16. CPAE是蜂胶的主要活性成分,它可由咖啡酸合成,其合成过程如下。下列说法错误的是( ) A、1mol CPAE与足量的NaOH溶液反应,最多消耗3mol NaOH B、可用金属Na检测上述反应结束后是否残留苯乙醇 C、与苯乙醇互为同分异构体的酚类物质共有9种 D、咖啡酸可发生聚合反应,并且其分子中含有3种官能团17. 下列说法错误的是( )A、葡萄糖和蔗糖都属于还原性糖 B、氨基酸是两性化合物 C、酶的催化作用在高温、强酸、强碱、重金属盐作用下易失效 D、DNA由两条平行盘绕的多聚核苷酸组成,两条链上的碱基通过氢键作用结合成碱基对18. 下列说法错误的是( )A、乙醛、甲酸、葡萄糖分别加入足量的新制 悬浊液并加热,均能产生砖红色沉淀 B、蛋白质的一级结构决定蛋白质的性质和功能 C、酚醛树脂、锦纶、核糖核酸、腺嘌呤都是有机高分子化合物 D、聚合物(
A、1mol CPAE与足量的NaOH溶液反应,最多消耗3mol NaOH B、可用金属Na检测上述反应结束后是否残留苯乙醇 C、与苯乙醇互为同分异构体的酚类物质共有9种 D、咖啡酸可发生聚合反应,并且其分子中含有3种官能团17. 下列说法错误的是( )A、葡萄糖和蔗糖都属于还原性糖 B、氨基酸是两性化合物 C、酶的催化作用在高温、强酸、强碱、重金属盐作用下易失效 D、DNA由两条平行盘绕的多聚核苷酸组成,两条链上的碱基通过氢键作用结合成碱基对18. 下列说法错误的是( )A、乙醛、甲酸、葡萄糖分别加入足量的新制 悬浊液并加热,均能产生砖红色沉淀 B、蛋白质的一级结构决定蛋白质的性质和功能 C、酚醛树脂、锦纶、核糖核酸、腺嘌呤都是有机高分子化合物 D、聚合物( )可由单体 和 加聚制得
19. 下表中实验操作能达到实验目的的是( )
)可由单体 和 加聚制得
19. 下表中实验操作能达到实验目的的是( )实验操作
实验目的
A
向溴乙烷中滴加少量硝酸银溶液
检验溴离子的存在
B
向待测液中分别加入酸性高锰酸钾溶液
鉴别苯、甲苯
C
向 的 溶液中滴加3-4滴 的氢氧化钠溶液,再向其中加入 乙醛,加热
检验醛基
D
向淀粉水解液中加入少量新制氢氧化铜悬浊液,煮沸
检验葡萄糖的存在
A、A B、B C、C D、D20. 下列实验装置图正确的是( )A、实验室制备及收集乙烯 B、石油分馏
B、石油分馏  C、实验室制硝基苯
C、实验室制硝基苯  D、实验室制乙酸乙酯
D、实验室制乙酸乙酯  21. 阿魏酸在食品、医药等方面有着广泛的用途。一种合成阿魏酸的反应可表示为:
21. 阿魏酸在食品、医药等方面有着广泛的用途。一种合成阿魏酸的反应可表示为:
下列说法正确的是( )
A、可用酸性 溶液检测上述反应是否有阿魏酸生成 B、香兰素、阿魏酸均可与 、 、 溶液反应 C、通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 D、与香兰素互为同分异构体,分子中有4种不同化学环境的氢且能发生银镜反应的酚类化合物共有3种22. 下列说法错误的是( )A、 氰基丙烯酸异丁酯的结构简式为 ,它的分子式是
B、等质量的甲烷、乙烯、乙醇分别充分燃烧,所耗用氧气的量依次减少
C、能与 溶液反应且分子式为 的有机物不一定是乙酸
D、
,它的分子式是
B、等质量的甲烷、乙烯、乙醇分别充分燃烧,所耗用氧气的量依次减少
C、能与 溶液反应且分子式为 的有机物不一定是乙酸
D、 是加成反应
23. 有关
是加成反应
23. 有关 的说法错误的是( ) A、分子中至少有8个碳原子共平面 B、分子中含1个手性碳原子 C、 该有机物最多能与 反应 D、酸性条件下加热水解有 生成24. 已二酸是一种重要的化工原料,科学家在现有工业路线基础上,提出了一条“绿色”合成路线:
的说法错误的是( ) A、分子中至少有8个碳原子共平面 B、分子中含1个手性碳原子 C、 该有机物最多能与 反应 D、酸性条件下加热水解有 生成24. 已二酸是一种重要的化工原料,科学家在现有工业路线基础上,提出了一条“绿色”合成路线: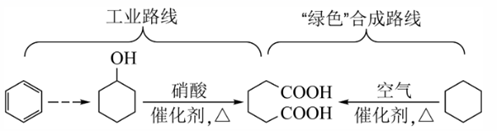
下列说法正确的是( )
A、苯与溴水混合,充分振荡后静置,下层溶液呈橙红色 B、环己醇与乙醇互为同系物 C、已二酸与 溶液反应有 生成 D、环己烷分子中所有碳原子共平面25. 我国科研人员使用催化剂CoGa3实现了H2还原肉桂醛生成肉桂醇,反应机理的示意图如下。下列说法错误的是( ) A、肉桂醛分子中存在顺反异构现象 B、苯丙醛分子中有5种不同化学环境的氢原子 C、还原反应过程发生了极性共价键和非极性共价键的断裂 D、该催化剂实现了选择性还原肉桂醛中的醛基
A、肉桂醛分子中存在顺反异构现象 B、苯丙醛分子中有5种不同化学环境的氢原子 C、还原反应过程发生了极性共价键和非极性共价键的断裂 D、该催化剂实现了选择性还原肉桂醛中的醛基二、填空题
-
26. 回答下列问题:(1)、
 的名称是: , 若该有机物是由炔烃加成而来,则该炔烃可能的结构有种。 (2)、氯乙烷的沸点(12℃)介于乙烷(-89℃)和乙醇(79℃)之间,其原因是。27. 将6.1g某有机物A(仅含C、H、O元素)样品置于燃烧器中充分燃烧,将燃烧产物依次通过浓硫酸和碱石灰,待燃烧产物被完全吸收后测得前者增重2.7g,后者增重15.4g,请回答:(1)、该有机物的实验式。(2)、若该有机物A的相对分子量为122,属于芳香族化合物,其核磁共振氢谱上有4组峰,且峰面积之比为1∶2∶2∶1,能与金属钠反应产生氢气,也能和新制加热后产生砖红色沉淀,该有机物的结构简式是 , 请写出该有机物与足量新制加热后反应的化学方程式。(3)、有机物A的某种同分异构体B,可用作食品防腐剂,能和碳酸氢钠溶液反应产生气泡。B是无色结晶,熔点122℃,沸点249℃,在水中溶解度如下图:
的名称是: , 若该有机物是由炔烃加成而来,则该炔烃可能的结构有种。 (2)、氯乙烷的沸点(12℃)介于乙烷(-89℃)和乙醇(79℃)之间,其原因是。27. 将6.1g某有机物A(仅含C、H、O元素)样品置于燃烧器中充分燃烧,将燃烧产物依次通过浓硫酸和碱石灰,待燃烧产物被完全吸收后测得前者增重2.7g,后者增重15.4g,请回答:(1)、该有机物的实验式。(2)、若该有机物A的相对分子量为122,属于芳香族化合物,其核磁共振氢谱上有4组峰,且峰面积之比为1∶2∶2∶1,能与金属钠反应产生氢气,也能和新制加热后产生砖红色沉淀,该有机物的结构简式是 , 请写出该有机物与足量新制加热后反应的化学方程式。(3)、有机物A的某种同分异构体B,可用作食品防腐剂,能和碳酸氢钠溶液反应产生气泡。B是无色结晶,熔点122℃,沸点249℃,在水中溶解度如下图:温度/℃
25
50
75
溶解度/g
0.34
0.85
2.2
B中混有KCl固体和泥沙,若要提纯B,在下列选项中选取合适的操作并正确排序。
①热水溶解 ②趁热过滤 ③过滤 ④冷却结晶 ⑤蒸发结晶 ⑥蒸馏 ⑦洗涤 ⑧干燥
三、综合题
-
28. 以气体 A 为原料的合成如图所示:

已知: 是生产塑料的合成树脂, 的产量是一个国家石油化工发展水平的重要标志。
(1)、写出 的电子式;②反应类型为。(2)、写出碳化钙与水反应制取 的化学方程式。(3)、实验室用该反应制取 时,可用饱和食盐水代替水,目的是。(4)、写出③、④反应方程式:③④。(5)、 还可以用石蜡油制取,工业上由石油获得汽油、煤油、石蜡油等成分的方法是。(6)、下列说法正确的是_______A、气体 的高分子聚合物可用于制备导电高分子材料 B、③反应的三元取代说明了苯环活化了甲基 C、可用间二甲苯是否存在不同结构来证明苯环的特殊的大 键 D、联苯 不属于苯的同系物,其二溴代物有17种
E、 的同分异构体
不属于苯的同系物,其二溴代物有17种
E、 的同分异构体  与 按物质的量之比 发生加成反应,生成产物有10种(不考虑立体异构)
29. 甲苯是重要的有机合成原料,以甲苯为原料合成抗肿瘤药物氟他胺X和某种抗疟疾药物的中间体Y的路线如下:
与 按物质的量之比 发生加成反应,生成产物有10种(不考虑立体异构)
29. 甲苯是重要的有机合成原料,以甲苯为原料合成抗肿瘤药物氟他胺X和某种抗疟疾药物的中间体Y的路线如下: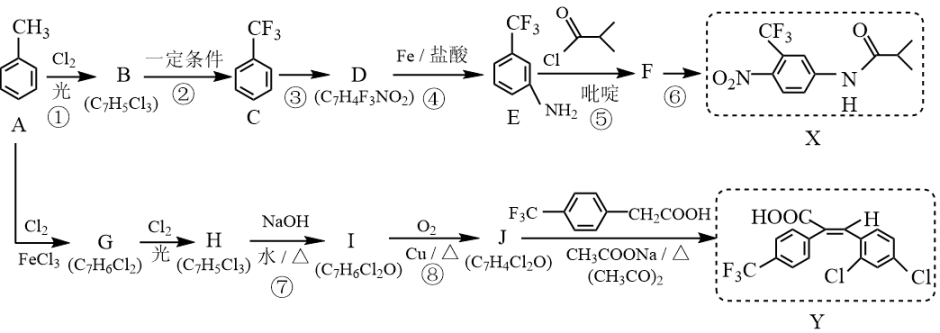
已知:①

②


③
请回答
(1)、E中官能团名称。(2)、下列说法正确的是____。A、B和H属于同一种物质 B、X分子中所有C原子和N原子可能在同一平面上 C、已知吡啶是一种有机碱,在反应⑤中可以吸收生成的HCl,提高转化率 D、反应③④⑤⑥都是取代反应,⑧是氧化反应(3)、F的结构简式是。(4)、完成J→Y的化学方程式。(5)、以丙炔为原料设计合成 的合成路线 (用流程图表示,无机试剂、有机溶剂任选)。 (6)、M是J的同系物,组成比J多一个 , 写出符合下列要求的M的所有的同分异构体
的合成路线 (用流程图表示,无机试剂、有机溶剂任选)。 (6)、M是J的同系物,组成比J多一个 , 写出符合下列要求的M的所有的同分异构体①能与溶液发生显色反应 ②苯环上只有一种氢
30. 正丁醚常用作有机合成反应的溶剂,某实验小组利用如下装置(夹持和加热装置均省略)合成正丁醚,其反应原理如下:反应物和产物的相关数据如下表:
化合物名称
密度( )
熔点(℃)
沸点(℃)
相对分子质量
水中溶解性
正丁醇
0.810
-89.8
118.0
74
微溶
正丁醚
0.769
-95.3
142.0
130
不溶于水
备注:正丁醚微溶于饱和氯化钙溶液
实验步骤:
①将 正丁醇、 浓硫酸加入两口烧瓶中,再加入几粒碎瓷片,摇匀;
②装好分水器和温度计;
③控制反应温度在 之间,回流 ;
④将分水器中的下层水层从下口放出,上层液体倒回两口烧瓶 中;
⑤将反应液冷却到室温后倒入盛有 水的分液漏斗中,经过分离、洗涤后再分离提纯,收集称重得正丁醚 。
回答下列问题:
 (1)、实验中冷凝管的进水口为(填“ ”或“ ”)。(2)、实验中,温度过高则发生分子内脱水生成烃类化合物,写出生成烃类化合物反应的化学方程式:。(3)、步骤⑤中,分液漏斗内的有机层是从分液漏斗(填“上口”或“下口”)放出(或倒出)。(4)、有机层粗产物需依次用水洗、氢氧化钠溶液洗涤、水洗和饱和氯化钙溶液洗涤。用氢氧化钠溶液洗涤的目的是。(5)、洗涤完成后,通过以下操作分离提纯产物,正确的操作顺序是(填标号)。
(1)、实验中冷凝管的进水口为(填“ ”或“ ”)。(2)、实验中,温度过高则发生分子内脱水生成烃类化合物,写出生成烃类化合物反应的化学方程式:。(3)、步骤⑤中,分液漏斗内的有机层是从分液漏斗(填“上口”或“下口”)放出(或倒出)。(4)、有机层粗产物需依次用水洗、氢氧化钠溶液洗涤、水洗和饱和氯化钙溶液洗涤。用氢氧化钠溶液洗涤的目的是。(5)、洗涤完成后,通过以下操作分离提纯产物,正确的操作顺序是(填标号)。
A.蒸馏 B.加入无水 C.过滤(6)、本实验所得正丁醚的产率为(小数点后保留两位数字)。