江苏省南京市建邺区2022年中考一模化学试题
试卷更新日期:2022-05-18 类型:中考模拟
一、单选题
-
1. 下列用品主要由合成材料制成的是( )A、纯棉卫衣 B、木质小尺 C、涤纶书包 D、钢制圆规2. 把少量下列物质分别放入足量水中,充分搅拌,不能形成溶液的是( )A、硫酸铵 B、小苏打 C、豆油 D、酒精3. 下列物质中,能用作磷肥的是( )A、K2SO4 B、CO(NH2)2 C、NH4NO3 D、Ca(H2PO4)24. 下列所贴的警示标志与存放的物质不相符的是( )A、火碱
 B、硫磺
B、硫磺  C、甲醛
C、甲醛  D、浓硫酸
D、浓硫酸  5. 下列物所与颜色对应正确的是( )A、高锰酸钾—黑色 B、金—红色 C、氯化铁溶液一浅绿色 D、液氧一淡蓝色6. 下列叙述正确的是( )A、用活性炭可将硬水软化 B、沙漠地区的铁制品绣蚀较慢 C、天然气是可再生能源 D、汽油可作除去油污的乳化剂7. 下图是五种微粒的结构示意图,下列说法错误的是( )
5. 下列物所与颜色对应正确的是( )A、高锰酸钾—黑色 B、金—红色 C、氯化铁溶液一浅绿色 D、液氧一淡蓝色6. 下列叙述正确的是( )A、用活性炭可将硬水软化 B、沙漠地区的铁制品绣蚀较慢 C、天然气是可再生能源 D、汽油可作除去油污的乳化剂7. 下图是五种微粒的结构示意图,下列说法错误的是( )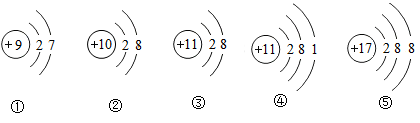 A、③④属于同一种元素 B、①②④表示的是原子,③⑤表示的是离子 C、②③⑤是相对稳定的结构 D、①④对应元素组成化合物的化学式为NaF28. 下列各组数据比较,其中正确的是( )A、熔点:锡>钨 B、地壳中元素含量:铝<硅 C、硬度:纯铁>生铁 D、人体中元素含量:氧<碳9. 将下列气体通入酚酞溶液中,能使酚酞溶液变红的是( )A、NH3 B、N2 C、CO2 D、SO210. 打火机中的液化气主要成分为丙烷(C3H8)和丁烷(C4H10),下列说法正确的是( )A、丙烷比丁烷少1个碳原子 B、丙烷和丁烷都属于有机高分子化合物 C、丙烷的相对分子质量比丁烷的相对分子质量小14g D、丙烷中碳元素的质量分数比丁烷中碳元素的质量分数小11. 下列对宏观事实的微观解释错误的是( )
A、③④属于同一种元素 B、①②④表示的是原子,③⑤表示的是离子 C、②③⑤是相对稳定的结构 D、①④对应元素组成化合物的化学式为NaF28. 下列各组数据比较,其中正确的是( )A、熔点:锡>钨 B、地壳中元素含量:铝<硅 C、硬度:纯铁>生铁 D、人体中元素含量:氧<碳9. 将下列气体通入酚酞溶液中,能使酚酞溶液变红的是( )A、NH3 B、N2 C、CO2 D、SO210. 打火机中的液化气主要成分为丙烷(C3H8)和丁烷(C4H10),下列说法正确的是( )A、丙烷比丁烷少1个碳原子 B、丙烷和丁烷都属于有机高分子化合物 C、丙烷的相对分子质量比丁烷的相对分子质量小14g D、丙烷中碳元素的质量分数比丁烷中碳元素的质量分数小11. 下列对宏观事实的微观解释错误的是( )选项
事实
解释
A
水银温度计放入热水中,水银柱升高
受热后原子之间的间隔变大
B
金刚石硬度很大,石墨却很软
构成两种物质的原子不同
C
蔗糖溶液不导电
溶液中没有自由移动的带电粒子
D
化学反应前后各物质质量总和不变
反应前后原子的种类、数目、质量均不改变
A、A B、B C、C D、D12. 甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。下列说法错误的是( ) A、t2℃时,甲、乙的溶解度相等 B、t1℃时,甲的饱和溶液中溶质与溶剂的质量之比为1:5 C、t3℃时,分别将甲、乙固体溶于水,配成两种物质的饱和溶液各100g,所需甲的质量小于乙的质量 D、甲中含有少量的乙,可采用冷却热的饱和溶液的方法提纯甲13. 除去下列物质中的少量杂质(括号内为杂质)拟定实验方案可行的是( )A、H2气体(HCl气体)——依次通过足量的碳酸氢钠溶液和浓硫酸 B、NaCl固体(泥沙)——加水充分溶解、过滤、洗涤、干燥 C、KCl溶液(MgCl2)——加入过量的KOH溶液,过滤 D、CaCl2溶液(HCl)——加入过量的碳酸钙,过滤14. 用氯离子传感器采集数据,向一定体积、一定浓度的氯化钠溶液中慢慢加入等体积、一定浓度的硝酸银溶液,恰好完全反应。实验数据如图所示。下列说法错误的是( )
A、t2℃时,甲、乙的溶解度相等 B、t1℃时,甲的饱和溶液中溶质与溶剂的质量之比为1:5 C、t3℃时,分别将甲、乙固体溶于水,配成两种物质的饱和溶液各100g,所需甲的质量小于乙的质量 D、甲中含有少量的乙,可采用冷却热的饱和溶液的方法提纯甲13. 除去下列物质中的少量杂质(括号内为杂质)拟定实验方案可行的是( )A、H2气体(HCl气体)——依次通过足量的碳酸氢钠溶液和浓硫酸 B、NaCl固体(泥沙)——加水充分溶解、过滤、洗涤、干燥 C、KCl溶液(MgCl2)——加入过量的KOH溶液,过滤 D、CaCl2溶液(HCl)——加入过量的碳酸钙,过滤14. 用氯离子传感器采集数据,向一定体积、一定浓度的氯化钠溶液中慢慢加入等体积、一定浓度的硝酸银溶液,恰好完全反应。实验数据如图所示。下列说法错误的是( )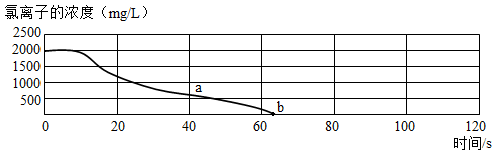 A、b点时溶液不导电 B、a点溶液中的离子为Na+、Cl-、 C、反应时观察到有白色沉淀生成 D、该反应的基本反应类型为复分解反应15. 利用气体压强的变化是完成实验的重要手段,以下各图装置气密性均良好。下列说法错误的是( )A、
A、b点时溶液不导电 B、a点溶液中的离子为Na+、Cl-、 C、反应时观察到有白色沉淀生成 D、该反应的基本反应类型为复分解反应15. 利用气体压强的变化是完成实验的重要手段,以下各图装置气密性均良好。下列说法错误的是( )A、 图①红磷燃烧过程中弹簧夹未夹紧,则测得空气中氧气的体积分数偏大
B、
图①红磷燃烧过程中弹簧夹未夹紧,则测得空气中氧气的体积分数偏大
B、 图②加入氧化钙后,石灰水中溶质质量减小,会导致玻璃弯管左侧液面降低
C、
图②加入氧化钙后,石灰水中溶质质量减小,会导致玻璃弯管左侧液面降低
C、 图③滴入浓硫酸后,气球胀大,说明氢氧化钠和硫酸反应放热
D、
图③滴入浓硫酸后,气球胀大,说明氢氧化钠和硫酸反应放热
D、 图④通入CO2后,碳酸钠溶液变浑浊,说明氯化钙溶液与碳酸钠溶液发生
图④通入CO2后,碳酸钠溶液变浑浊,说明氯化钙溶液与碳酸钠溶液发生
二、填空题
-
16. 化学与人类生活密切相关。(1)、Ⅰ、下表列出的是每100g某品种西瓜的主要营养素数据。
营养素
水分
蛋白质
油脂
X
维生素
钙、铁、锌等
质量
92.5g
0.7g
0.2g
6.1g
6.8mg
17.1mg
“X”是指六大基本营养素中的。
(2)、“钙、铁、锌”中属于人体必需的微量元素的是。(填元素符号)(3)、Ⅱ、在日常生活中,各种塑料制品已被广泛应用。请指出使用塑料的利与弊(各写出一条)。
①利:。
②弊:。
(4)、Ⅲ、燃烧是人类最早利用的化学反应之一。如图实验可用来验证可燃物燃烧的条件。

a.将一定量的白磷浸入80℃热水中,白磷不燃烧。
b.将一定量的红磷浸入80℃热水中,红磷不燃烧。
c.升高右侧漏斗至红磷露出水面,红磷不燃烧。
d.升高左侧漏斗至白磷露出水面,白磷燃烧。
①c中红磷不燃烧的原因是。
②对比a和d,可验证可燃物燃烧的条件是。
(5)、实验小组同学欲鉴别一氧化碳和甲烷两种气体,请设计实验并完成下表。实验操作
实验现象及结论
任写一个有关反应的化学方程式
。
。
。
三、综合题
-
17. 实验室常用溶质质量分数为6%的H2O2溶液(MnO2作催化剂)制取氧气。(1)、配制质量分数为6%的H2O2溶液。
①计算:配制150g质量分数为6%的H2O2溶液,需要质量分数为30%(密度为1.1g/cm3)的H2O2溶液体积为mL(计算结果保留一位小数),水为g。
②量取:用量筒量取所需H2O2溶液和水,倒入烧杯中。用量筒量取液体时,视线应与。
③混匀:…。
(2)、制取氧气(可能用到的部分装置如图)。
①实验室用氯酸钾(MnO2作催化剂)制取干燥的氧气,选择的发生装置和收集装置为(填字母),反应的化学方程式为。
②实验室用发生装置B制取氧气的化学方程式为。
(3)、实验反思。①若其他操作正确,量取水时俯视读数,则配制的H2O2溶液溶质质量分数6%(填“>”、“<”或“=”)。
②若用E装置收集一瓶(容积为200mL)体积分数为80%的氧气,预先应用量筒量取mL的水加入该集气瓶中(不考虑水蒸气的影响)。
18. 2020年12月,“嫦娥五号”返回器携带的月球土壤样品,对于科学探测月球的金属资源方面意义很大。(1)、月球上存在天然的铁、铝等金属颗粒而地球上没有,原因是。(2)、为验证铜、锌、银三种金属的活动性顺序,两位同学设计了不同方案。
①小明设计了如图所示方案。根据现象,得出铜、锌、银三种金属的活动性由强到弱的顺序为。发生反应的化学方程式为。
②小芳选择了光亮的铜丝、溶液和溶液(均写化学式)也验证出铜、锌、银三种金属的活动性顺序。
(3)、镁和镁合金广泛应用于航空航天等领域。写出镁与盐酸反应的化学方程式,并计算若得到0.4g的氢气,理论上最少消耗铁的质量是多少?19. 以煤粉灰(主要成分为Al2O3、SiO2及少量Fe2O3等)为原料制取Al2O3的部分工艺流程如图:
【资料】
①SiO2既不溶于水也不溶于酸。
②煅烧时发生的反应为: 。
(1)、“酸浸”步骤中盐酸与Fe2O3发生反应的化学方程式为。“酸浸”时温度不宜过高的原因是。(2)、滤渣的主要成分是(写名称)。(3)、“除铁”时发生的反应为 ,则X的化学式为。(4)、流程中可循环利用的物质为(写化学式)。20. 图中A~J是初中化学常见的物质。A可供给动植物呼吸:B、E、I属于氧化物,且E中两种元素的质量比为4:1:G是蓝色固体:J俗称熟石灰。图中“一”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物、生成物和反应条件已略去。 (1)、C的化学式为。(2)、写出D与E反应的化学方程式。(3)、写出F与G反应的化学方程式。(4)、写出H→I反应的化学方程式。21. 化学兴趣小组为测定碱式碳酸亚铁【xFeCO3·yFe(OH)2】的组成,在老师的指导下设计了如图实验装置,进行了相关的探究(实验中每一步的吸收都是完全的)。
(1)、C的化学式为。(2)、写出D与E反应的化学方程式。(3)、写出F与G反应的化学方程式。(4)、写出H→I反应的化学方程式。21. 化学兴趣小组为测定碱式碳酸亚铁【xFeCO3·yFe(OH)2】的组成,在老师的指导下设计了如图实验装置,进行了相关的探究(实验中每一步的吸收都是完全的)。
【查阅资料】
①碱式碳酸亚铁受热完全分解生成氧化亚铁、二氧化碳和水。
②氧化亚铁不稳定,在空气中加热会被氧化成四氧化三铁。
(1)、【实验步骤】①检查装置气密性后,称取4.83g碱式碳酸亚铁粉末放在装置B中,连接仪器。
②打开弹簧夹K,鼓入一段时间空气,称量装置C、D、E的质量。
③关闭弹簧夹K,加热装置B,直至观察到装置C中 , 再打开弹簧夹K,缓缓通入空气一段时间,这样操作的目的是。
④再次称量装置C、D、E的质量。
(2)、【实验数据】装置C/g
装置D/g
装置E/g
加热前
200.00
180.00
180.00
加热后
200.27
181.32
180.00
【实验结论】
在xFeCO3·yFe(OH)2 , x:y=。
(3)、【交流反思】①写出装置A中发生反应的化学方程式为。
②实验结束后,装置B中残留固体可能有氧化亚铁、四氯化三铁。
①残留固体可能有四氧化三铁的原因是(用化学方程式表示)。
②称得残留固体的质量为3.36g,通过计算得出残留固体为。
-