福建省三明市2022年九年级第二次教学质量监测化学试题
试卷更新日期:2022-05-18 类型:中考模拟
一、单选题
-
1. 今年世界卫生日的主题为“我们的地球,我们的健康”。下列做法错误的是( )A、垃圾分类回收 B、废电池集中填埋 C、污水处理达标后排放 D、使用光降解塑料2. 维持人类生命和健康的下列基本营养素中,不能提供能量的是( )A、油脂 B、糖类 C、蛋白质 D、维生素3. 下列有关水的说法正确的是( )A、水和冰由不同的分子构成 B、长期饮用蒸馏水,有利于身体健康 C、生活中通过煮沸可以降低水的硬度 D、天然水经自来水厂净化处理后成为纯净物4. 下列检查装置气密性的操作,错误的是( )A、
 B、
B、 C、
C、 D、
D、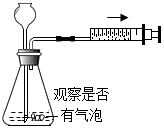 5. 下列说法正确的是( )A、稀盐酸和稀硫酸化学性质相似,原因是溶液中都含有氢离子 B、气体容易被压缩,原因是气体分子的质量和体积都很小 C、金刚石和石墨都由碳原子构成,是同一种物质 D、保持氯化钠化学性质的微粒是氯化钠分子6. 下图是铁及其化合物的“价一类”二维图。下列说法错误的是( )
5. 下列说法正确的是( )A、稀盐酸和稀硫酸化学性质相似,原因是溶液中都含有氢离子 B、气体容易被压缩,原因是气体分子的质量和体积都很小 C、金刚石和石墨都由碳原子构成,是同一种物质 D、保持氯化钠化学性质的微粒是氯化钠分子6. 下图是铁及其化合物的“价一类”二维图。下列说法错误的是( ) A、a对应的物质类别是单质 B、b与稀盐酸反应时,溶液由无色逐渐变为黄色 C、c不溶于水,也不与稀硫酸反应 D、 对应的点为e点7. 如图所示,将适量液体x加入到烧瓶中,气球不会逐渐膨胀的是( )
A、a对应的物质类别是单质 B、b与稀盐酸反应时,溶液由无色逐渐变为黄色 C、c不溶于水,也不与稀硫酸反应 D、 对应的点为e点7. 如图所示,将适量液体x加入到烧瓶中,气球不会逐渐膨胀的是( )
液体X
固体Y
A
稀盐酸
铜
B
稀盐酸
小苏打
C
水
氧氧化钠
D
水
生石灰
A、A B、B C、C D、D8. 疗新冠肺炎的中药“连花清瘟胶囊”中含有薄荷脑(C10H20O)。下列有关薄荷脑的说法错误的是( )A、属于有机物 B、氢元素的质量分数最大 C、一个分子中有31个原子 D、由碳、氢、氧三种元素组成9. 下列实验操作能够达到目的的是( )选项
实验目的
实验操作
A
测定某废水的酸碱度
取样,将待测液滴在用水润湿的pH试纸上
B
比较Fe、Cu、Ag的金属活动性
溶液中将将Fe和Cu分别放入AgNO3
C
检验CO2中混有HCl
将气体通入紫色石蕊试液中
D
鉴别稀盐酸和稀硫酸
取样,滴加氯化钡溶液
A、A B、B C、C D、D10. 兴趣小组将一块铝箔加入盛有100 g稀盐酸的烧杯中,反应停止时,有剩余,产生氢气质量和反应时间关系如图所示。下列分析错误的是( ) A、该铝箔表面有氧化铝 B、反应停止时,烧杯中剩余溶液的质量为99.8 g C、t1~t2时间段,氢气生成速率加快与温度升高有关 D、t2~t3时间段,氢气生成速率变慢是因为盐酸浓度变小
A、该铝箔表面有氧化铝 B、反应停止时,烧杯中剩余溶液的质量为99.8 g C、t1~t2时间段,氢气生成速率加快与温度升高有关 D、t2~t3时间段,氢气生成速率变慢是因为盐酸浓度变小二、填空题
-
11. “化”说能源。(1)、木柴是使用最早、最广泛的生物能源。木柴劈成小块更易燃烧的原因是。(2)、燃油燃油是古代重要的能源。唐宋时期的夹瓷盏是省油的灯,其结构如图所示:

①下层盏的水能减缓油的挥发从微观的角度解释其原因是。
②夹瓷盏省油的另一个原因是其盏身为陶瓷。陶瓷属于。
A.无机非金属材料 B.金属材料 C.合成材料 D.复合材料
(3)、化石燃料是现代重要的能源,包括煤、、天然气等。化石燃料燃烧会产生大量的二氧化碳,为实现“碳达峰”,科学家将CO2和H2在一定条件下反应,方程式为2CO2+6H2 X+4H2O,X是一种重要的化工原料,化学式为。(4)、新能源2022年北京冬季奥运会使用以氢氧燃料电池为动力的汽车。氢氧燃料电池中发生反应的化学方程式为。
12. 化学中的宏—微—符。根据下图回答问题。
 (1)、锶的相对原子质量为 , 属于元素(填“金属”或“非金属”)。(2)、氯离子中,x的数值是;氯元素位于元素周期表第周期。(3)、离子符号为Sr2+牙膏中添加的氯化锶有抗过敏作用,其化学式为。(4)、溶液中发生图3所示的反应,化学方程式为 , 反应前后,溶液中离子数目(填“增加”“减少”或“不变”)。13. 中国化学史上的辉煌。(1)、《天工开物·燔石》中烧石成灰”:每煤饼一层垒石一层,铺薪其底、灼火燔之。
(1)、锶的相对原子质量为 , 属于元素(填“金属”或“非金属”)。(2)、氯离子中,x的数值是;氯元素位于元素周期表第周期。(3)、离子符号为Sr2+牙膏中添加的氯化锶有抗过敏作用,其化学式为。(4)、溶液中发生图3所示的反应,化学方程式为 , 反应前后,溶液中离子数目(填“增加”“减少”或“不变”)。13. 中国化学史上的辉煌。(1)、《天工开物·燔石》中烧石成灰”:每煤饼一层垒石一层,铺薪其底、灼火燔之。
①“烧石成灰”,“灰”的主要成分是(填化学式)。
②“烧石成灰”的过程中,将热能转换为。
③“铺薪其底”,木材对煤饼燃烧的作用是。
(2)、《梦溪笔谈》中记载;信州铅山县有苦泉,流以为洞。挹其水熬之,则成胆矾。烹胆矾则成铜;熬胆矾铁釜,久之亦化为铜。①“挹其水熬之,则成胆矾”。该步骤相当于化学操作中的。
②“烹胆矾则成铜”,胆矾加热的化学方程式为 ,CuSO4·5H2O的相对分子质量为。
③“熬胆矾铁釜,久之亦化为铜”。“铁釜化为铜”的化学方程式为。
14. 硝酸钾不同温度时的溶解度如下、某兴趣小组同学将一定量的硝酸钾固体加入盛有100 g水的烧杯中,级慢升温和充分溶解,不同温度下烧杯中溶液的质量如下图所示:
温度/℃
0
20
40
60
80
90
100
溶解度/g
13.3
31.6
63.9
110
169
X
246
(1)、溶解度表中X值的范围为 。(2)、a点对应的溶液质量为。(3)、b点对应的溶液的溶质质量分数为(列式即可)。(4)、使d点对应的溶液变成饱和溶液,至少需要加入硝酸钾的质量为。(5)、溶液温度从60℃升温至80℃时,溶液中溶质的质量分数(填“变大”“不变”或“变小”)。三、综合题
-
15. 某食品包装袋中“双吸剂”上的标答如图所示,兴趣小组同学取适量“双吸剂”样品研碎,按照下图流程进行实验。回答问题。

 (1)、操作1和操作2的名称是。(2)、无色溶液中的溶质是。(3)、生成可燃性气体的反应属于(填反应类型)。(4)、Cl2与浅绿色溶液发生化合反应,反应的化学方程式为。(5)、根据实验,“双吸剂”除了铁粉、生石灰,还可能有填物质名称)。(6)、“双吸剂”的工作原理主要是利用铁能与和等物质发生反应。16. 实验室用H2O2溶液和MnO2制取氧气的部分装置如图1。
(1)、操作1和操作2的名称是。(2)、无色溶液中的溶质是。(3)、生成可燃性气体的反应属于(填反应类型)。(4)、Cl2与浅绿色溶液发生化合反应,反应的化学方程式为。(5)、根据实验,“双吸剂”除了铁粉、生石灰,还可能有填物质名称)。(6)、“双吸剂”的工作原理主要是利用铁能与和等物质发生反应。16. 实验室用H2O2溶液和MnO2制取氧气的部分装置如图1。 (1)、仪器①的名称是。(2)、该反应的化学方程式为;收集较纯净的氧气,应选择的装置是(填字母)。(3)、用图2所示装置除去氧气中混有的水蒸气,瓶中的试剂是 , 气体应从(填“a”或“b”)端通入。(4)、不同质量分数的H2O2溶液中加入等量的MnO2、实验现象如下表:
(1)、仪器①的名称是。(2)、该反应的化学方程式为;收集较纯净的氧气,应选择的装置是(填字母)。(3)、用图2所示装置除去氧气中混有的水蒸气,瓶中的试剂是 , 气体应从(填“a”或“b”)端通入。(4)、不同质量分数的H2O2溶液中加入等量的MnO2、实验现象如下表:H2O2的质量分数
实验现象
15%
反应速度快,短时间内产生大量气泡
10%
反应比较平缓,导管口气流均匀、连续
5%
反应平缓,导管口气流均匀、连续
3%
反应缓慢,产生气泡的速率慢
①根据上表,用H2O2溶液制取氧气时,质量分数在范围较好。
②市售的H2O2溶液质量分数为30%,配制成6%,30%的H2O2溶液与水的质量比为。
17. 小某兴趣小组用图1所示装置试验石灰水的导电性、观察到灯泡发光;有同学发现通电一段时间后,两个石墨电极附近有气泡产生,且与正极相连的石墨附近产生大量白色浑浊。兴趣小组对此展开探究。 (1)、灯泡发光,说明石灰水能导电。氢氧化钙在水中解离出的阳离子是(写微粒符号)。(2)、与负极相连的石墨附近产生的气体是。(3)、白色浑浊产生的原因。
(1)、灯泡发光,说明石灰水能导电。氢氧化钙在水中解离出的阳离子是(写微粒符号)。(2)、与负极相连的石墨附近产生的气体是。(3)、白色浑浊产生的原因。猜想一:溶液温度升高导致氢氧化钙析出。
猜想二:水减少导致氢氧化钙析出。
猜想三:与正极相莲的石墨附近产生的气体与反应,生成的气体和石灰水反应生成碳酸钙。最后一个反应的化学方程式为。
(4)、另取三份相同的饱和石灰水,测定其温度和质量,进行以下实验探究。【实验1】一份重复导电性实验。测定溶液产生大量白色浑浊时的温度和质量。
【实验2】一份加热升高且同温度,未观察到明显的白色浑浊。
【实验3】一份恒温蒸发相同质量的水,观察到产生少量白色浑浊。
【实验4】实验装置如图2所示;检查装置气密性,加入实验1中的浑浊液,开启传感器,然后注入足量的稀盐酸。广口瓶中二氧化碳的含量随时间变化的曲线如图3所示。

分析与结论:
①白色浑浊物中含有氢氧化钙。氢氧化钙析出的主要原因是。
②图3曲线中,二氧化碳含量在开始阶段降低的原因是;根据图中曲线,说明白色浑浊物中。
(5)、实验拓展:若通电相同时间,减少白色浑浊物产生的措施有:(写一条)。四、计算题
-
18. 某兴趣小组将6 g的干燥鸡蛋壳捣碎,放在烧杯中,然后向其中滴加足量的稀盐酸(鸡蛋壳中的其他成分不溶于水,也不与稀盐酸反应),生成2.2 g二氧化碳,反应的化学方程式为 。求该鸡蛋壳中CaCO3的质量分数(保留一位小数)。