辽宁省抚顺市抚顺县2021-2022学年九年级下学期教学质量检测化学试题
试卷更新日期:2022-05-16 类型:中考模拟
一、单选题
-
1. 在抗击新冠疫情中,下列措施包含化学变化的是( )A、喷药消毒 B、开窗通风 C、经常洗手 D、佩戴口罩2. 下列不属于化石燃料的是()A、天然气 B、石油 C、煤 D、乙醇3. 下列物质属于氧化物的是( )A、O3 B、SO3 C、CaSO4 D、Cu(OH)24. 下列“液体”为纯净物的是( )A、蒸馏水 B、胃液 C、波尔多液 D、“84”消毒液5. 下列图示实验操作中,正确的是( )A、
 倾倒液体
B、
倾倒液体
B、 稀释浓硫酸
C、
稀释浓硫酸
C、 过滤
D、
过滤
D、 称量氢氧化钠固体
6. 下列做法不符合食品安全的是( )A、用食盐腌制蔬菜 B、用小苏打焙制糕点 C、用甲醛溶液保鲜海产品 D、用干冰来冷藏食品7. 为建设天蓝地绿水净的美丽中国,下列做法不合理的是( )A、工业三废处理后排放 B、施用大量农药减少植物病虫害 C、合成新型洗涤剂减少氮磷排放 D、研发易降解材料减少白色污染8. 从分子、原子角度认识物质是化学的基本特征。下列说法正确的是( )A、分子由原子构成,分子比原子大 B、水遇冷凝结成冰,水分子停止了运动 C、原子是变化中的最小粒子,不可再分 D、分子中原子的重新组合是化学变化的基础9. 下列实验现象描述正确的是( )A、硫在氧气中燃烧,产生淡蓝色火焰 B、高温条件下,碳与二氧化碳反应吸收热量 C、铜丝插入硫酸铝溶液中,溶液由无色变为蓝色 D、打开盛有浓盐酸的试剂瓶塞,在瓶口有白色烟雾生成10. 科学家成功地将二氧化碳转化为乙烯,反应前后分子种类变化的微观示意图如下。下列说法错误的是( )
称量氢氧化钠固体
6. 下列做法不符合食品安全的是( )A、用食盐腌制蔬菜 B、用小苏打焙制糕点 C、用甲醛溶液保鲜海产品 D、用干冰来冷藏食品7. 为建设天蓝地绿水净的美丽中国,下列做法不合理的是( )A、工业三废处理后排放 B、施用大量农药减少植物病虫害 C、合成新型洗涤剂减少氮磷排放 D、研发易降解材料减少白色污染8. 从分子、原子角度认识物质是化学的基本特征。下列说法正确的是( )A、分子由原子构成,分子比原子大 B、水遇冷凝结成冰,水分子停止了运动 C、原子是变化中的最小粒子,不可再分 D、分子中原子的重新组合是化学变化的基础9. 下列实验现象描述正确的是( )A、硫在氧气中燃烧,产生淡蓝色火焰 B、高温条件下,碳与二氧化碳反应吸收热量 C、铜丝插入硫酸铝溶液中,溶液由无色变为蓝色 D、打开盛有浓盐酸的试剂瓶塞,在瓶口有白色烟雾生成10. 科学家成功地将二氧化碳转化为乙烯,反应前后分子种类变化的微观示意图如下。下列说法错误的是( )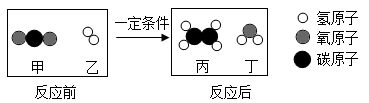 A、乙烯的化学式为C2H4 B、甲和丁均为氧化物 C、生成丙和丁的分子个数比为1:1 D、参加反应的甲与乙的质量比为22:311. 下列各组物质在溶液中能大量共存且形成无色溶液的是( )A、BaCl2 Na2SO4 B、MgSO4 NaCl C、FeCl3 NaNO3 D、KOH HCl12. 下列鉴别方法不可行的是( )A、用熟石灰鉴别化肥氯化铵和硝酸铵 B、用稀硫酸鉴别氧化铜粉末和木炭粉末 C、用灼烧闻气味的方法鉴别棉纤维和合成纤维 D、不另加试剂就能鉴别出硫酸铜、氢氧化钠、氯化钠的三种溶液13. 向溶质为硝酸银的溶液中加入一定质量的铜粉和锌粉。充分反应后过滤,得到滤渣和滤液。下列判断错误的是( )A、若滤液为无色,滤渣中一定含有铜和银 B、若滤液为蓝色,滤渣中一定含有银,可能含有铜 C、向滤渣中加入稀盐酸若有气泡产生,滤液中一定只含有硝酸锌 D、向滤渣中加入稀盐酸若没有气泡产生,滤液中一定含有硝酸锌和硝酸铜14. 下列选项中,符合化学学科核心素养的是( )A、探究与创新:用铁丝代替红磷测定空气中氧气的体积分数 B、变化与守恒:化学变化前后,催化剂的性质和质量都不发生改变 C、宏观与微观:化学反应前后,原子种类、质量与元素种类、质量均不变 D、模型与推理:金刚石和石墨中碳原子排列方式不同,所以它们的化学性质不同15. 为达到实验目的,下列实验方案不可行的是( )
A、乙烯的化学式为C2H4 B、甲和丁均为氧化物 C、生成丙和丁的分子个数比为1:1 D、参加反应的甲与乙的质量比为22:311. 下列各组物质在溶液中能大量共存且形成无色溶液的是( )A、BaCl2 Na2SO4 B、MgSO4 NaCl C、FeCl3 NaNO3 D、KOH HCl12. 下列鉴别方法不可行的是( )A、用熟石灰鉴别化肥氯化铵和硝酸铵 B、用稀硫酸鉴别氧化铜粉末和木炭粉末 C、用灼烧闻气味的方法鉴别棉纤维和合成纤维 D、不另加试剂就能鉴别出硫酸铜、氢氧化钠、氯化钠的三种溶液13. 向溶质为硝酸银的溶液中加入一定质量的铜粉和锌粉。充分反应后过滤,得到滤渣和滤液。下列判断错误的是( )A、若滤液为无色,滤渣中一定含有铜和银 B、若滤液为蓝色,滤渣中一定含有银,可能含有铜 C、向滤渣中加入稀盐酸若有气泡产生,滤液中一定只含有硝酸锌 D、向滤渣中加入稀盐酸若没有气泡产生,滤液中一定含有硝酸锌和硝酸铜14. 下列选项中,符合化学学科核心素养的是( )A、探究与创新:用铁丝代替红磷测定空气中氧气的体积分数 B、变化与守恒:化学变化前后,催化剂的性质和质量都不发生改变 C、宏观与微观:化学反应前后,原子种类、质量与元素种类、质量均不变 D、模型与推理:金刚石和石墨中碳原子排列方式不同,所以它们的化学性质不同15. 为达到实验目的,下列实验方案不可行的是( )选项
目的
实验方案
A
制备
用生石灰、水、碳酸钠为原料制备烧碱
B
净化
经沉淀、过滤、吸附、消毒操作,可将河水净化为自来水
C
除杂
除去氯化钠固体中少量的氢氧化钠固体,加入过量的稀盐酸、蒸发
D
检验
检验氢氧化钠溶液与稀硫酸是否反应,可向反应后溶液中加入氯化钡溶液
A、A B、B C、C D、D二、填空题
-
16. 请用化学用语填空:(1)、2个氟原子;(2)、氯酸钾中氯元素化合价;(3)、碱溶液中的阴离子;(4)、醋酸。17. 紫薯中富含淀粉、蛋白质、维生素、锌、铁、钙等,营养丰富。(1)、紫薯中维生素(选填“A”、“B”或“C”)可预防坏血病。(2)、除淀粉外,紫薯中含有的能给人体供能的营养素是。(3)、紫薯中的元素可有效预防佝偻病。(4)、紫薯种植常需施用复合肥。现有硝酸铵、硝酸钾、氯化钾三种化肥,其中属于复合肥的是。(5)、紫薯生长过程中离不开水,农田灌溉时将大水漫灌改成滴灌或喷灌,其目的是。18. 图1是元素周期表中铟元素的信息,图2是铟原子的结构示意图,回答下列问题:
 (1)、铟元素的原子核外共有个电子层。(2)、在化学反应中,铟原子容易(填“失去”或“得到”)电子形成铟离子,铟离子的化学符号为。(3)、图2中X的数值是。19. 下图是氯化钠和硝酸钾在不同温度下的溶解度,请回答问题:
(1)、铟元素的原子核外共有个电子层。(2)、在化学反应中,铟原子容易(填“失去”或“得到”)电子形成铟离子,铟离子的化学符号为。(3)、图2中X的数值是。19. 下图是氯化钠和硝酸钾在不同温度下的溶解度,请回答问题:温度/℃
0
10
20
30
40
50
溶解度/g
NaCl
35.7
35.8
36.0
36.3
36.6
37.0
KNO3
13.3
20.9
31.6
45.8
63.9
85.5
(1)、20℃时,把20 g氯化钠加入50 g水中充分溶解,所得溶液质量为。(2)、分别将50℃时硝酸钾和氯化钠的饱和溶液降温到0℃,析出晶体的质量关系为硝酸钾氯化钠 (填“<”、“>”或“无法确定”)。(3)、20℃对某固体的溶液进行恒温蒸发,实验过程如下图,请回答问题。
①该固体是(填“氯化钠”或“硝酸钾”)
②溶液乙为(填“不饱和溶液”、“饱和溶液”或“无法确定”)。
③甲~丁溶液溶质的质量分数大小关系为。
A.甲<乙<丙=丁 B.甲<乙<丙<丁 C.甲<乙<丁<丙
20. 能源利用和环境保护问题一直受到社会高度关注。(1)、国家提倡使用电动汽车,多地出台电动汽车不限行措施,电动汽车和燃油汽车相比,其优点是(答一点)。(2)、目前我市部分公交线路已引进了以天然气为燃料的公交车。天然气的主要成分是甲烷,请写出甲烷充分燃烧的化学方程式。(3)、下列做法无助于全球能源可持续发展的是____。A、使用节能灯泡 B、用秸秆制秸秆燃气 C、加大石油进口,减少国内原油开采 D、大力开发利用风能,替代化石燃料21. “对比实验”是科学探究常用的方法,根据以下实验回答问题。 (1)、实验一中开可乐的瓶盖,观察到大量气泡冒出,说明气体的溶解度与有关。(2)、实验二中产生浮渣更多的是(填“硬水”或“软水”)。(3)、实验三中观察到木条燃烧,玻璃棒不燃烧,说明燃烧应具备的条件是。(4)、实验四中观察到高锰酸钾溶于水形成紫红色溶液,而碘几乎不溶于水,说明物质的溶解性与有关。
(1)、实验一中开可乐的瓶盖,观察到大量气泡冒出,说明气体的溶解度与有关。(2)、实验二中产生浮渣更多的是(填“硬水”或“软水”)。(3)、实验三中观察到木条燃烧,玻璃棒不燃烧,说明燃烧应具备的条件是。(4)、实验四中观察到高锰酸钾溶于水形成紫红色溶液,而碘几乎不溶于水,说明物质的溶解性与有关。三、综合题
-
22. 共享单车可实现绿色出行。
 (1)、在如图中所标示的共享单车各部件中,属于金属材料的是。(填序号)(2)、防止自行车链条生锈的有效措施是。(3)、自行车有些零件选用了铝合金材料,其优点是质量轻、硬度大和。(4)、废弃的生锈铁制品可以制取氯化铁,用于工业废水的处理,由部分锈蚀的铁制品制备氯化铁晶体的主要过程如图所示。
(1)、在如图中所标示的共享单车各部件中,属于金属材料的是。(填序号)(2)、防止自行车链条生锈的有效措施是。(3)、自行车有些零件选用了铝合金材料,其优点是质量轻、硬度大和。(4)、废弃的生锈铁制品可以制取氯化铁,用于工业废水的处理,由部分锈蚀的铁制品制备氯化铁晶体的主要过程如图所示。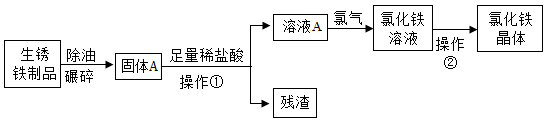
①操作1是。
②操作2中需要用玻璃棒搅拌的目的是。
③固体A与稀盐酸发生置换反应的化学方程式为。
23. A~E是五种不同类别的物质,已知A是紫红色固体,D俗称火碱。且A、B、C中含有相同元素,它们之间的关系如图所示(部分反应物,生成物及反应条件已略去),图中“一”表示相连的两种物质之间可以发生反应,“→"表示物质间可以相互转化。 (1)、A的化学式是;(2)、D的一种用途是;(3)、E的物质类别为(填“酸”、“盐”或“氧化物”);(4)、若B由三种元素组成,写出C→B反应的化学方程式。24. 根据下列仪器回答有关问题。
(1)、A的化学式是;(2)、D的一种用途是;(3)、E的物质类别为(填“酸”、“盐”或“氧化物”);(4)、若B由三种元素组成,写出C→B反应的化学方程式。24. 根据下列仪器回答有关问题。
 (1)、组装一套二氧化碳的发生和收集装置,应选择上述仪器中的(填序号),检验二氧化碳的实验操作是。(2)、实验室用高锰酸钾制取氧气,还需补充的一种仪器是(填仪器名称),反应的化学方程式为 , 若用排水法收集氧气,集满氧气的现象为。25. 某化学活动小组在探究碳酸钠的化学性质时,做了如下实验
(1)、组装一套二氧化碳的发生和收集装置,应选择上述仪器中的(填序号),检验二氧化碳的实验操作是。(2)、实验室用高锰酸钾制取氧气,还需补充的一种仪器是(填仪器名称),反应的化学方程式为 , 若用排水法收集氧气,集满氧气的现象为。25. 某化学活动小组在探究碳酸钠的化学性质时,做了如下实验 (1)、实验一:探究碳酸钠溶液的酸碱性,观察到试管中溶液变为红色,可得出的结论是:碳酸钠溶液显性。
(1)、实验一:探究碳酸钠溶液的酸碱性,观察到试管中溶液变为红色,可得出的结论是:碳酸钠溶液显性。实验二:探究碳酸钠溶液分别与氯化钙溶液和氢氧化钙溶液的反应,此时两支试管中观察到的现象是 , 反应的化学方程式为(写一个)。
(2)、实验后,同学们将实验二中两支试管里的物质倒入同一个洁净的小烧杯中,充分反应后,静置一会儿,发现烧杯中白色固体明显增多。过滤后,同学们对滤液中的溶质展开了探究。【提出问题】滤液的溶质都有哪些物质?
【猜想与假设】
A同学:滤波中的溶质含有氯化钠、氢氧化钠、碳酸钠
B同学:滤液中的溶质含有氯化钠、氢氧化钠、氢氧化钙
C同学:滤液中的溶质含有氯化钠、氯化钙
同学们经过认真的思考后,认为C同学的猜想是错误的,原因是。
(3)、【探究及结论】经改正后同学们进行了如下实验,取滤液于试管中,向其中滴加足量的(试剂名称),观察到有气泡生成,由此同学们得出结论:A同学的猜想成立。
(4)、【实验拓展】若要验证滤液中的氢氧化钠存在,可向滤液中加入的试剂组合是____。
A、氢氧化钙溶液 B、酚酞溶液 C、氯化钙溶液(5)、【归纳与总结】结合此探究过程,同学们认识到在分析化学反应后所得物质的成分时,不仅要考虑生成物,还要考虑。
四、计算题