天津市西青区2022年中考一模化学试题
试卷更新日期:2022-05-16 类型:中考模拟
一、单选题
-
1. 下列成语涉及化学变化的是( )A、滴水成冰 B、木已成舟 C、风吹草动 D、钻木取火2. 空气中含量最多且化学性质不活泼的气体是()A、O2 B、CO2 C、N2 D、Ne3. “庄稼一枝花,全靠肥当家。”下列属于复合肥料的是( )A、NH4HCO3 B、KCl C、(NH4)2HPO4 D、CO(NH2)24. 下列实验操作中正确的是( )A、
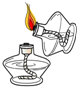 点燃酒精灯
B、
点燃酒精灯
B、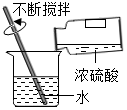 稀释浓硫酸
C、
稀释浓硫酸
C、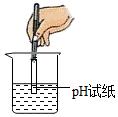 测溶液的pH
D、
测溶液的pH
D、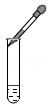 滴加液体
5. 大气平流层中的臭氧(O3)能吸收大部分紫外线,保护地球生物,臭氧属于( )A、纯净物 B、混合物 C、氧化物 D、化合物6. 下列说法错误的是( )A、液化石油气压缩到钢瓶中一分子体积变小 B、品红在静置的水中会扩散一分子在不停的运动 C、金刚石和石墨物理性质差异很大一碳原子排列方式不同 D、氢气在氯气中燃烧生成氯化氢一在化学变化中分子可以再分7. 2021年4月16日,我国自主研发出超流氦大型低温制冷装备,打破了发达国家的技术垄断,液氦是制造超低温的“神器”。根据图中信息判断,下列关于氦的说法正确的是( )
滴加液体
5. 大气平流层中的臭氧(O3)能吸收大部分紫外线,保护地球生物,臭氧属于( )A、纯净物 B、混合物 C、氧化物 D、化合物6. 下列说法错误的是( )A、液化石油气压缩到钢瓶中一分子体积变小 B、品红在静置的水中会扩散一分子在不停的运动 C、金刚石和石墨物理性质差异很大一碳原子排列方式不同 D、氢气在氯气中燃烧生成氯化氢一在化学变化中分子可以再分7. 2021年4月16日,我国自主研发出超流氦大型低温制冷装备,打破了发达国家的技术垄断,液氦是制造超低温的“神器”。根据图中信息判断,下列关于氦的说法正确的是( ) A、氦属于金属元素 B、氦原子容易失去电子 C、氦的相对原子质量是4.003g D、氦原子核内有2个质子8. 下列有关实验现象的描述正确的是( )A、硫在氧气中燃烧发出微弱的淡蓝色火焰 B、将打磨光亮的铝丝插入到硫酸铜溶液中,铝丝表面有铜析出 C、打开盛有浓盐酸的试剂瓶,瓶口出现白雾 D、铁丝在氧气中燃烧生成四氧化三铁9. 下列有关“一定”的说法正确的是( )A、生成盐和水的反应一定是酸碱中和反应 B、原子一定是由质子、中子和电子构成 C、化学反应前后分子种类一定不变 D、由同种元素组成的纯净物一定是单质10. 在反应X+2Y=R+2M中已知X和Y的相对分子质量之比为1:2,当1.6gX与Y恰好完全反应时,生成4.4gR,则在此反应中Y与M的质量比为( )A、1:1 B、16:9 C、9:22 D、9:1611. 归纳总结是学习化学的基本方法,下列知识点归纳完全正确的是( )
A、氦属于金属元素 B、氦原子容易失去电子 C、氦的相对原子质量是4.003g D、氦原子核内有2个质子8. 下列有关实验现象的描述正确的是( )A、硫在氧气中燃烧发出微弱的淡蓝色火焰 B、将打磨光亮的铝丝插入到硫酸铜溶液中,铝丝表面有铜析出 C、打开盛有浓盐酸的试剂瓶,瓶口出现白雾 D、铁丝在氧气中燃烧生成四氧化三铁9. 下列有关“一定”的说法正确的是( )A、生成盐和水的反应一定是酸碱中和反应 B、原子一定是由质子、中子和电子构成 C、化学反应前后分子种类一定不变 D、由同种元素组成的纯净物一定是单质10. 在反应X+2Y=R+2M中已知X和Y的相对分子质量之比为1:2,当1.6gX与Y恰好完全反应时,生成4.4gR,则在此反应中Y与M的质量比为( )A、1:1 B、16:9 C、9:22 D、9:1611. 归纳总结是学习化学的基本方法,下列知识点归纳完全正确的是( )A.化学与健康
B.化学与环境
①人体缺乏维生素A会引起夜盲症
②禁止食用甲醛溶液浸泡过的海产品
③食用霉变的花生对人体有害
①焚烧秸秆不会造成环境污染
②使用脱硫煤可有效解决酸雨问题
③工业废水未经处理就排放会造成水污染
C.化学与农业
D.化学与生活
①可用铁桶配制农药波尔多液
②农业上采用喷灌和滴灌可节约用水
③过量使用化学肥料会造成土壤污染
①用碳素墨水书写档案
②蚊虫叮咬涂肥皂水可以减轻痛痒
③涤纶、羊毛、腈纶都属于合成纤维
A、A B、B C、C D、D12. 下列图像能正确反映其对应关系的是( )A、 电解水生成氢气和氧气的质量与反应时间的关系
B、
电解水生成氢气和氧气的质量与反应时间的关系
B、 加热一定量高锰酸钾固体制氧气,剩余固体中锰元素的质量分数与反应时间的关系
C、
加热一定量高锰酸钾固体制氧气,剩余固体中锰元素的质量分数与反应时间的关系
C、 向氢氧化钠溶液中不断加水,溶液pH与加入水的质量关系
D、
向氢氧化钠溶液中不断加水,溶液pH与加入水的质量关系
D、 相同质量的Mg、Fe分别与足量的稀盐酸反应,产生氢气的质量与反应时间的关系
相同质量的Mg、Fe分别与足量的稀盐酸反应,产生氢气的质量与反应时间的关系
二、多选题
-
13. 下列实验方案设计正确的是( )
选项
实验目的
实验方案
A
除去KCl溶液中含有的少量KNO3
加适量硝酸银溶液,过滤
B
除去CO2中含有的少量CO
通过足量灼热的氧化铜
C
鉴别CuCl2、NaCl、NaOH和H2SO4溶液
不需要外加试剂就可以鉴别
D
检验NaOH溶液中是否含有Ca(OH)2
滴入氯化铁溶液,观察现象
A、A B、B C、C D、D14. 甲、乙、丙、丁四种物质的相互反应关系如图所示,下列选项符合对应关系的是( )
选项
A
B
C
D
甲
HCl
CO2
Ca(OH)2
Fe
乙
Ca(OH)2
NaOH
Na2CO3
HCl
丙
K2CO3
CaCl2
H2SO4
CuSO4
丁
H2SO4
AgNO3
BaCl2
NaOH
A、A B、B C、C D、D15. 利用气体压强的变化是完成实验的重要手段。以下各图装置气密性均良好。下列正确的是( )A、 向广口瓶中滴入稀盐酸后,气球变大,说明氢氧化钠和盐酸反应放热
B、
向广口瓶中滴入稀盐酸后,气球变大,说明氢氧化钠和盐酸反应放热
B、 向试管中加入氧化钙后,石灰水中溶质质量减小,玻璃弯管左侧液面降低
C、
向试管中加入氧化钙后,石灰水中溶质质量减小,玻璃弯管左侧液面降低
C、 过量红磷燃烧熄灭并冷却至室温后,打开弹簧夹,观察到集气瓶水面上升1/5
D、
过量红磷燃烧熄灭并冷却至室温后,打开弹簧夹,观察到集气瓶水面上升1/5
D、 氢氧化钡溶液变浑浊,说明通入的二氧化碳与氢氧化钡发生了反应
氢氧化钡溶液变浑浊,说明通入的二氧化碳与氢氧化钡发生了反应
三、填空题
-
16. 化学在生产、生活中有着广泛应用。现有①熟石灰 ②活性炭 ③干冰 ④氯化钠,选择适当的物质填空(填序号),(1)、可作厨房调味品的是。(2)、可作冰箱除味剂的是。(3)、可改良酸性土壤的是。(4)、可用于人工降雨的是。17. 生活中处处有化学,回答下列问题:(1)、加铁酱油中铁元素属于人体所需的(填“常量”或“微量”)元素;(2)、铁制品在(填“潮湿”或“干燥”)的空气中容易生锈:(3)、洗洁精清洗餐具去除油污时起作用:(4)、生活中通过可以降低水的硬度:(5)、在厨房中,天然气属于(填“可再生”或“不可再生”)能源,其主要成分(甲烷)在空气中充分燃烧的化学方程式为。(6)、油锅起火,迅速用锅盖盖灭,其主要灭火原理是____。A、降低温度至食用油的着火点以下 B、清除可燃物 C、隔绝空气(7)、84消毒液中的有效成分为次氯酸钠(化学式为NaClO),其中Cl元素的化合价为。18. 在宏观、微观和符号之间建立联系是化学特有的思维方式。根据电解水的实验,回答下列问题:
 (1)、从宏观上观察:如图所示,试管a中气体名称为;由产物可知,水是由组成;(2)、从微观上分析:每个水分子是由构成;(3)、从符号上表示:电解水的化学方程式为。19. 根据下列粒子的结构示意图,回答下列问题:
(1)、从宏观上观察:如图所示,试管a中气体名称为;由产物可知,水是由组成;(2)、从微观上分析:每个水分子是由构成;(3)、从符号上表示:电解水的化学方程式为。19. 根据下列粒子的结构示意图,回答下列问题: (1)、属于同一种元素的是(填字母,下同):不同种元素最本质的区别是不同;(2)、A~E中具有相对稳定结构的原子是。(3)、D和E元素形成化合物的化学式为(用字母表示):(4)、F元素原子中x的值是。20. 写出下列反应的化学方程式。(1)、硫在氧气中燃烧。(2)、铜与硝酸银溶液反应。(3)、碳酸氢钠与稀盐酸反应。21. 甲、乙、丙三种物质的溶解度曲线如下图所示,回答下列问题:
(1)、属于同一种元素的是(填字母,下同):不同种元素最本质的区别是不同;(2)、A~E中具有相对稳定结构的原子是。(3)、D和E元素形成化合物的化学式为(用字母表示):(4)、F元素原子中x的值是。20. 写出下列反应的化学方程式。(1)、硫在氧气中燃烧。(2)、铜与硝酸银溶液反应。(3)、碳酸氢钠与稀盐酸反应。21. 甲、乙、丙三种物质的溶解度曲线如下图所示,回答下列问题: (1)、温度为℃时,甲、乙两物质溶解度相同;(2)、20℃时,甲、乙、丙三种物质溶解度由大到小的顺序。(3)、50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液的质量由大到小的顺序为。22. 金属材料与人类的生产和生活密切相关。请回答:(1)、下列用品中,主要利用金属导电性的是____(填字母);A、铂金饰品 B、铁锅 C、铝导线(2)、将一定量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。滤液呈蓝色,则滤渣中可能含有的物质是(写出化学式,下同)。滤液中一定含有的溶质是。(3)、A、B、C、D、E、F均含同一种元素,它们之间的转化关系如下图(部分物质已略去)。A是目前世界年产量最高的金属:D属于氧化物,氧元素质量分数为30%,B的化学式为 , D→E的化学方程式为 , C→F反应的化学方程式为 , 则X的化学式为。
(1)、温度为℃时,甲、乙两物质溶解度相同;(2)、20℃时,甲、乙、丙三种物质溶解度由大到小的顺序。(3)、50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液的质量由大到小的顺序为。22. 金属材料与人类的生产和生活密切相关。请回答:(1)、下列用品中,主要利用金属导电性的是____(填字母);A、铂金饰品 B、铁锅 C、铝导线(2)、将一定量的铁粉加入到Al(NO3)3、Cu(NO3)2、AgNO3三种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。滤液呈蓝色,则滤渣中可能含有的物质是(写出化学式,下同)。滤液中一定含有的溶质是。(3)、A、B、C、D、E、F均含同一种元素,它们之间的转化关系如下图(部分物质已略去)。A是目前世界年产量最高的金属:D属于氧化物,氧元素质量分数为30%,B的化学式为 , D→E的化学方程式为 , C→F反应的化学方程式为 , 则X的化学式为。 23. 有一固体混合物,可能含有K2CO3、K2SO4、CuSO4、CaCl2、KNO3等物质中的一种或几种。将混合物溶于水,得无色溶液,当滴入硝酸钡溶液时,有白色沉淀产生,再加足量的稀硝酸沉淀部分溶解,则该混合物一定含有 , 一定不含有 , 可能含有。24. 请你根据所学知识并结合下图所示装置回答下列问题:
23. 有一固体混合物,可能含有K2CO3、K2SO4、CuSO4、CaCl2、KNO3等物质中的一种或几种。将混合物溶于水,得无色溶液,当滴入硝酸钡溶液时,有白色沉淀产生,再加足量的稀硝酸沉淀部分溶解,则该混合物一定含有 , 一定不含有 , 可能含有。24. 请你根据所学知识并结合下图所示装置回答下列问题: (1)、装置E中仪器a的名称是。(2)、实验室用高锰酸钾制取氧气的化学方程式为;实验室用装置B制氧气时,该反应的化学方程式为。(3)、实验室制取氢气选用A~E中的装置组合是或。(4)、实验室制取二氧化碳的化学方程式为;若用F装置收集二氧化碳气体应从(填“m”或“n”)端通入。
(1)、装置E中仪器a的名称是。(2)、实验室用高锰酸钾制取氧气的化学方程式为;实验室用装置B制氧气时,该反应的化学方程式为。(3)、实验室制取氢气选用A~E中的装置组合是或。(4)、实验室制取二氧化碳的化学方程式为;若用F装置收集二氧化碳气体应从(填“m”或“n”)端通入。四、计算题