天津市河东区2022年中考一模化学试题
试卷更新日期:2022-05-16 类型:中考模拟
一、单选题
-
1. 中华传统文化博大精深,下列成语中涉及化学变化的是( )A、木已成舟 B、滴水成冰 C、火上浇油 D、聚沙成塔2. 2022年北京冬奥会秉持“科技冬奥”的理念,其中国家速滑馆“冰丝带”采用了CO2直冷制冰技术,碳排放值趋近于零,减少碳排放可以防止下列哪一情况的发生( )A、空气污染 B、酸雨 C、温室效应 D、雾霾3. 下列物质属于纯净物的是( )A、海水 B、水泥砂浆 C、水银 D、汽水4. 规范的实验操作是科研成功的前提,下列图示实验操作中正确的是( )A、
 B、
B、 C、
C、 D、
D、 5. 下图为常见几种水果的近似pH值,其中酸性最强的是( )A、
5. 下图为常见几种水果的近似pH值,其中酸性最强的是( )A、 西瓜pH=6.6
B、
西瓜pH=6.6
B、 葡萄 pH=5.1
C、
葡萄 pH=5.1
C、 柠檬 pH=2.3
D、
柠檬 pH=2.3
D、 桔子 pH=3.6
6. 北京冬奥会上品种丰富的美味佳肴是为运动员们特殊的营养需求制作的。以下是为运动员准备的一份晚餐:香肠、炖牛肉、米饭、红烧鱼、鸡蛋汤,这份晚餐还需要的营养素是( )A、糖类 B、油脂 C、蛋白质 D、维生素7. 高铁酸钠(Na2FeO4)是一种“绿色环保高效”的饮用水消毒剂.高铁酸钠中铁元素的化合价为( )A、+2 B、+3 C、+5 D、+68. 下列实验现象的描述正确的是( )A、磷在氧气中燃烧产生大量的白色烟雾 B、木炭在氧气中燃烧产生明亮的白色火焰 C、硫在氧气中燃烧发出淡蓝色火焰,生成带刺激性气味的气体 D、铁丝在氧气中剧烈燃烧,火星四射9. 2022年2月2日,北京冬奥会火炬接力在北京奥林匹克森林公园开启。火炬燃烧必须具备的条件是:①有可燃物;②有足够的氧气;③温度达到可燃物的着火点;④使用碳纤维材料作外壳。( )A、①②③ B、②③ C、①③④ D、①②④10. 2022年将在北京举行冬奥会。火炬中的燃料X燃烧后不会对环境造成污染,体现了“绿色奥运”的理念。反应的化学方程式为X +5O2 3CO2+4H2O,则X是( )A、C2H4 B、C2H6 C、C3H6 D、C3H811. 下列物质暴露在空气中,质量不会发生变化的是( )A、浓H2SO4 B、生石灰 C、铁钉 D、石灰石12. 下列选项中,实验操作不能够达到相对应实验目的是( )
桔子 pH=3.6
6. 北京冬奥会上品种丰富的美味佳肴是为运动员们特殊的营养需求制作的。以下是为运动员准备的一份晚餐:香肠、炖牛肉、米饭、红烧鱼、鸡蛋汤,这份晚餐还需要的营养素是( )A、糖类 B、油脂 C、蛋白质 D、维生素7. 高铁酸钠(Na2FeO4)是一种“绿色环保高效”的饮用水消毒剂.高铁酸钠中铁元素的化合价为( )A、+2 B、+3 C、+5 D、+68. 下列实验现象的描述正确的是( )A、磷在氧气中燃烧产生大量的白色烟雾 B、木炭在氧气中燃烧产生明亮的白色火焰 C、硫在氧气中燃烧发出淡蓝色火焰,生成带刺激性气味的气体 D、铁丝在氧气中剧烈燃烧,火星四射9. 2022年2月2日,北京冬奥会火炬接力在北京奥林匹克森林公园开启。火炬燃烧必须具备的条件是:①有可燃物;②有足够的氧气;③温度达到可燃物的着火点;④使用碳纤维材料作外壳。( )A、①②③ B、②③ C、①③④ D、①②④10. 2022年将在北京举行冬奥会。火炬中的燃料X燃烧后不会对环境造成污染,体现了“绿色奥运”的理念。反应的化学方程式为X +5O2 3CO2+4H2O,则X是( )A、C2H4 B、C2H6 C、C3H6 D、C3H811. 下列物质暴露在空气中,质量不会发生变化的是( )A、浓H2SO4 B、生石灰 C、铁钉 D、石灰石12. 下列选项中,实验操作不能够达到相对应实验目的是( )选项
实验目的
实验操作
A
除去CO2中的少量H2O和HCl
先通过足量氢氧化钠溶液,再通过浓硫酸
B
探究NaOH固体是否变质
取少量固体,加水溶解,滴加足量稀盐酸,观察是否有气泡产生
C
验证Al、Mg的金属活动性大小
将打磨过的大小相同的Al片和Mg片分别浸入等质量且等浓度的稀盐酸中,观察产生气泡的速率快慢
D
用酚酞溶液鉴别:①NaCl溶液
②稀硫酸③NaOH溶液
不再使用其他任何试剂就能鉴别
A、A B、B C、C D、D13.下列各组转化中,一定条件下均能一步实现的组合是( )
 A、①② B、②③ C、①③ D、①②③
A、①② B、②③ C、①③ D、①②③二、多选题
-
14. 下列事实与相应的解释不一致的是( )
选项
事实
解释
A
10mL酒精和10mL水混合后体积小于20mL
混合后分子变小了
B
氢氧化钠和氢氧化钙化学性质相似
在其溶液中都含有OH-
C
化肥硫酸铵不能和熟石灰混放或混用
硫酸铵和熟石灰发生中和反应
D
氮气常用作焊接金属时的保护气
氮气的化学性质不活泼
A、A B、B C、C D、D15. 下列说法中正确的是( )A、等质量的甲烷和二氧化碳中,氢元素与氧元素的质量比为11﹕32 B、碳、硫充分燃烧消耗等质量的氧气时,消耗的碳的质量比硫的质量大 C、等质量的镁和铁的粉末分别加入等质量等浓度的稀盐酸中,放出的气体一定质量相等 D、向一定质量的氢氧化钠和氢氧化钾的固体混合物中加入100g质量分数为7.3%的稀盐酸,恰好完全反应,得到109.6g该温度下的不饱和溶液。则原固体混合物中金属元素的质量分数约为64.6%三、填空题
-
16. 化学就在我们身边,一些物质在生产生活中有重要的用途。现有①青铜 ②干冰 ③氯化钠 ④活性炭 ⑤氧气 ⑥稀盐酸,选择适当的物质填空(填序号)。(1)、在人胃里帮助消化的是;(2)、用于冰箱除味的是;(3)、可用作医疗急救的是;(4)、用于人工降雨的是;(5)、生活中作调味品的是;(6)、使用最早的合金是。17. 在宏观、微观和符号之间建立联系是化学学科的特点
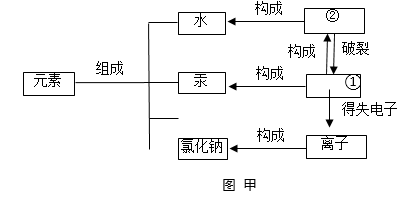 (1)、物质的组成和构成关系如图甲所示,图中①为(填“分子”、“原子”或“离子”),汞是由组成的。氯化钠中阴离子的符号是。(2)、氧、硫、氯三种元素的原子结构示意图如图乙所示。则x=。这三种元素的原子在化学反应中都容易(填“得到”或“失去”)电子,和硫的化学性质相似的粒子是(填化学符号)。
(1)、物质的组成和构成关系如图甲所示,图中①为(填“分子”、“原子”或“离子”),汞是由组成的。氯化钠中阴离子的符号是。(2)、氧、硫、氯三种元素的原子结构示意图如图乙所示。则x=。这三种元素的原子在化学反应中都容易(填“得到”或“失去”)电子,和硫的化学性质相似的粒子是(填化学符号)。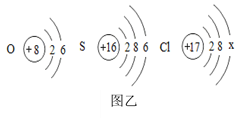 (3)、汽车尾气处理装置能将CO和NO转化为没有污染的气体,发生反应的微观示意图如图丙所示,如果有28gCO能吸收gNO。
(3)、汽车尾气处理装置能将CO和NO转化为没有污染的气体,发生反应的微观示意图如图丙所示,如果有28gCO能吸收gNO。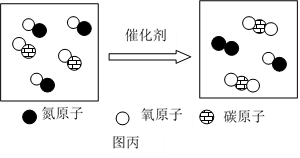 18. 水是生命之源,为了人类和社会经济的可持续发展,我们应该了解一些有关水的知识,请你回答:(1)、天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是。(2)、向水中加入活性炭,利用其性,除去水样中的色素和异味。(3)、如图是电解水的实验装置,请写出该实验的化学反应方程式 , 负极产生的气体是(填写化学式),该实验证明水是由组成。
18. 水是生命之源,为了人类和社会经济的可持续发展,我们应该了解一些有关水的知识,请你回答:(1)、天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是。(2)、向水中加入活性炭,利用其性,除去水样中的色素和异味。(3)、如图是电解水的实验装置,请写出该实验的化学反应方程式 , 负极产生的气体是(填写化学式),该实验证明水是由组成。 19. 写出下列反应的化学方程式(1)、磷在空气中充分燃烧;(2)、锌和稀硫酸反应;(3)、碳酸氢钠溶液与稀盐酸混合。20. 溶液与人们的生活密切相关。(1)、用井水洗衣服时,肥皂不易起泡沫且产生大量浮渣,该井水是(填“硬水”或“软水”)。(2)、洗洁精清洗碗壁上的油污,是利用了洗洁精的作用。(3)、雨水会溶解空气里的部分CO2 , 故正常雨水的pH7(填“>”、“<”或“=”)(4)、10%的葡萄糖口服液可用于低血糖症的治疗。配制50g溶质质量分数为10%的葡萄糖溶液,实验步骤为:
19. 写出下列反应的化学方程式(1)、磷在空气中充分燃烧;(2)、锌和稀硫酸反应;(3)、碳酸氢钠溶液与稀盐酸混合。20. 溶液与人们的生活密切相关。(1)、用井水洗衣服时,肥皂不易起泡沫且产生大量浮渣,该井水是(填“硬水”或“软水”)。(2)、洗洁精清洗碗壁上的油污,是利用了洗洁精的作用。(3)、雨水会溶解空气里的部分CO2 , 故正常雨水的pH7(填“>”、“<”或“=”)(4)、10%的葡萄糖口服液可用于低血糖症的治疗。配制50g溶质质量分数为10%的葡萄糖溶液,实验步骤为:①计算:葡萄糖g;②称量;③量取;④;⑤装瓶贴签。
(5)、硝酸钾的溶解度曲线如图1所示。向100g水中加入硝酸钾固体或改变温度,得到相应如图2所示的混合物体系①~⑤。
Ⅰ、①中溶液(选填“是”或“不是”)饱和溶液。
Ⅱ、②中溶液的质量为g。
Ⅲ、②~③变化过程中,溶剂的质量 , 溶质的质量。(填序号)
A.不变 B.变大 C.变小
Ⅳ、⑤中析出晶体的质量为g。
21. 化学为人类的科学进步起到了重要的作用。(1)、雪上项目是冬奥会重要项目之一、制作滑雪板各部分所对应的材料中,下列不含有机合成材料的是____。A、板面—尼龙纤维 B、板芯—木质 C、板底—聚乙烯塑料 D、复合层—玻璃纤维与合成树脂(2)、“嫦娥五号“上使用的记忆合金、SiC颗粒增强铝基复合材料等材料引起了全世界的关注。①硬度非常大的SiC,其结构类似金刚石,则构成SiC的基本粒子为(填序号)。
A.分子 B.原子 C.离子 D.电子
②工业制取记忆合金中的钛,先用热浓硫酸处理钛铁矿(主要成分为FeTiO3)反应中各元素化合价不变,得到硫酸钛[Ti(SO4)2]、硫酸亚铁和一种氧化物,该反应的化学方程式为。
22. 铁及其化合物在生活生产中有重要的应用。请回答下列问题:(1)、2022年北京冬奥会国家速滑馆“冰丝带”采用世界跨度最大的单层双向正交马鞍形索网屋面,用钢量仅为传统屋面的四分之一、下列关于钢铁的说法错误的是____。A、铁是目前年产量最高的金属 B、钢铁在潮湿的空气中不发生锈蚀 C、用磁铁可区分铁制品和铝制品 D、钢的许多性能优于生铁(2)、把铁粉和碳粉的混合物放入硝酸银溶液中,充分反应后,过滤,为确定滤渣和滤液的成分,甲同学向滤渣中滴加稀盐酸,无气泡产生;乙同学向滤液中滴加稀盐酸,产生白色沉淀。根据两同学实验的现象,分析下列结论错误的是____(填序号)。A、滤渣中只含银 B、滤渣中可能含有银,一定含有碳 C、滤液中一定有Ag+、Fe2+ D、滤液中只含Ag+ , 不含Fe2+(3)、废铁屑的主要成分是铁,同时还有少量铁锈(Fe2O3),生产动物饲料添加剂硫酸亚铁的工艺流程之一如下图所示:
在反应器中发生反应的化学方程式有:
①Fe+H2SO4═FeSO4+H2↑、②、③Fe2(SO4)3+Fe═3FeSO4。
滤液M中肯定含有的溶质的化学式是;
(4)、取生铁5.8g(除碳外,无其它杂质),加入到足量的20.0g的稀硫酸中,充分反应后,所得混合物的总质量为25.6g。则生铁中铁的质量为g。四、综合题
-
23. 请结合图示实验装置,回答下列问题:
 (1)、仪器a的名称是。(2)、实验室用A装置制取氧气的化学方程式为。(3)、实验室中既能制取O2又能制取CO2和H2的发生装置为(填字母序号),收集CO2气体一般不选择E装置的原因是 , 请写出实验室制取CO2气体的化学方程式。(4)、若选用F装置收集氢气,气体应从(填“c”或“d”)导管口通入。24. 在粗盐的提纯实验中同学们进行了如下操作
(1)、仪器a的名称是。(2)、实验室用A装置制取氧气的化学方程式为。(3)、实验室中既能制取O2又能制取CO2和H2的发生装置为(填字母序号),收集CO2气体一般不选择E装置的原因是 , 请写出实验室制取CO2气体的化学方程式。(4)、若选用F装置收集氢气,气体应从(填“c”或“d”)导管口通入。24. 在粗盐的提纯实验中同学们进行了如下操作 (1)、其主要操作步骤顺序是。
(1)、其主要操作步骤顺序是。①过滤 ②溶解 ③蒸发 ④计算产率
(2)、图1是某同学过滤的操作图,图中有一处明显的不正确;(3)、蒸发时,蒸发皿内出现时应停止加热。(4)、通过以上操作只能除去粗盐中难溶性杂质,欲除去可溶性杂质MgCl2、CaCl2得到纯净的NaCl,可采用如图2所示流程。①图中所用甲、乙、丙三种试剂依次是。
A.NaOH溶液、Na2CO3溶液、稀盐酸
B.Na2CO3溶液、KOH溶液、稀盐酸
C.NaOH溶液、Na2CO3溶液、稀硫酸
②通过以上规范操作,制得氯化钠的质量比原粗盐样品中含氯化钠的质量(填“增多”、“减少”、“不变”)。
五、计算题
-
25. “新型冠状病毒”在全球全面爆发,“抗疫”任重道远。医疗上大量使用体积分数为70%~75%的酒精溶液作消毒剂,请根据酒精(C2H5OH)的信息,完成下列问题。(1)、酒精中C、H、O元素质量比为 ;(2)、酒精中碳元素的质量分数为。(结果精确到0.1%)。26. 家里蒸馒头用的纯碱中含有少量的氯化钠,课外探究小组的同学欲测定纯碱中碳酸钠的含量。他们取该纯碱样品11.0g,全部溶解在100.0g水中,再加入氯化钙溶液141.0g,恰好完全反应。过滤干燥后,称得沉淀质量为10.0g。请计算:(1)、纯碱样品中碳酸钠的质量;(2)、反应后所得滤液中溶质的质量分数。