上海市徐汇区2022年中考二模化学试题
试卷更新日期:2022-05-16 类型:中考模拟
一、单选题
-
1. 能够形成酸雨的气体是( )A、O2 B、SO2 C、CO2 D、N22. 属于化学变化的是( )A、浓盐酸挥发 B、干冰升华 C、分离液态空气制氧气 D、稀硫酸除铁锈3. 若农作物缺乏钾元素,可适量施用下列哪种化肥( )A、Ca(H2PO4)2 B、(NH4)2SO4 C、KCl D、CO(NH2)24. 室温下用pH试纸测得家中常见四种液体的pH,其中酸性最强的是( )A、洁厕灵:pH=1 B、可乐:pH=4 C、84消毒液:pH=10 D、油烟净:pH=135. 下列物质的性质和用途对应错误的是( )A、氦气的化学性质稳定一一作保护气体 B、活性炭具有吸附性一一饮用水消毒 C、铜具有导电性一一制成电线 D、一氧化碳具有还原性一一冶炼金属6. 工业冶炼金属锰的原理是3MnO2+4Al3Mn+2Al2O3 , 该反应属于( )A、置换反应 B、化合反应 C、分解反应 D、复分解反应7. 下列实验现象描述正确的是( )A、铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 B、红磷在空气中燃烧产生大量白色烟雾 C、木炭在氧气中燃烧,发出红色的光 D、硫在氧气中燃烧,发出明亮的蓝紫色火焰8. 为验证锌和铜的金属活动性顺序,所选用试剂错误的是( )A、锌片、铜片、稀硫酸 B、铁片、硫酸铜溶液、硫酸锌溶液 C、锌片、铜片、硝酸银溶液 D、锌片、硫酸铜溶液9. 下列事实的解释正确的是( )A、白磷保存在冷水中一一隔绝空气,防止燃烧 B、打开汽水瓶盖,冒出大量气泡一一温度升高,气体的溶解度减小 C、金刚石硬度大,石墨质地软一一构成物质的原子不同 D、水变为水蒸气后体积增大一一水分子的体积变大10. 甲烷和二氧化碳在Al2O3的催化下可以制取气态化工原料,下图是其原理的微观示意图,关于该反应的说法错误的是( )
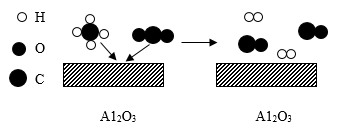 A、该气态化工原料的主要成分是H2和CO B、反应前后Al2O3的质量和化学性质不变 C、参加反应的甲烷和二氧化碳的物质的量相等 D、反应前后分子个数保持不变11. 在实验室中制备有毒气体X的装置如图所示,下列说法错误的是( )
A、该气态化工原料的主要成分是H2和CO B、反应前后Al2O3的质量和化学性质不变 C、参加反应的甲烷和二氧化碳的物质的量相等 D、反应前后分子个数保持不变11. 在实验室中制备有毒气体X的装置如图所示,下列说法错误的是( ) A、制取X的反应能在常温下发生 B、该发生装置的优点是可以控制反应的发生和停止 C、X的密度小于空气 D、烧杯中液体的作用是处理尾气12. 实验室中硝酸银溶液常保存在棕色试剂瓶中,其原因是硝酸银见光易分解,该反应的化学方程式是 , 物质X的化学式是( )A、NO B、NO2 C、N2O4 D、N2O513. 鉴别下列物质时选用试剂错误的是( )
A、制取X的反应能在常温下发生 B、该发生装置的优点是可以控制反应的发生和停止 C、X的密度小于空气 D、烧杯中液体的作用是处理尾气12. 实验室中硝酸银溶液常保存在棕色试剂瓶中,其原因是硝酸银见光易分解,该反应的化学方程式是 , 物质X的化学式是( )A、NO B、NO2 C、N2O4 D、N2O513. 鉴别下列物质时选用试剂错误的是( )选项
鉴别物质
选用试剂
A
NaCl、NaNO3
AgNO3溶液
B
AgNO3溶液、Na2SO4溶液
BaCl2溶液
C
CuSO4、NaCl
水
D
盐酸、硫酸
Ba(NO3)2溶液
A、A B、B C、C D、D14. 在密闭容器中放入amol碳和bmol氧气,充分反应后,容器内不含有毒气体,则a,b的值可能是( )A、a=2,b=3 B、a=2,b=1.5 C、a=2,b=1 D、a=1,b=0.7515. 在组装如图所示的装置前,烧瓶中添加了一种物质,胶头滴管中吸取了液体。实验时将胶头滴管中液体加入烧瓶,能观察到气球先膨胀再恢复原状的是( )
选项
烧瓶中的物质
胶头滴管中的液体
A
CO2
NaOH溶液
B
生石灰
水
C
大理石
稀盐酸
D
硫酸钡
稀硝酸
A、A B、B C、C D、D二、多选题
-
16. 有三种常见的消毒剂:3%双氧水、碘酒、消毒酒精,下列说法正确的是( )A、三种消毒剂的溶剂相同 B、碘酒的溶质是单质 C、碘酒和消毒酒精中含有机物 D、三种消毒剂都是化合物17. 镁与稀硫酸反应时会放出大量热,将一段表面有氧化镁层的镁带与过量稀硫酸在密闭容器中混合,用压强传感器测得容器内压强和反应时间的变化曲线如下图所示,下列分析正确的是( )
 A、AB段主要发生的反应是 B、气体温度升高是造成BC段压强增大的唯一原因 C、90秒时镁带恰好完全溶解 D、C点、D点、E点时反应生成气体的质量相同
A、AB段主要发生的反应是 B、气体温度升高是造成BC段压强增大的唯一原因 C、90秒时镁带恰好完全溶解 D、C点、D点、E点时反应生成气体的质量相同三、填空题
-
18. 科技的助力让北京冬奥会更绿色、更安全、更精彩。请用所学化学知识回答下列问题。(1)、乙二醇(化学式为C2H6O2)合成的材料可以制作防撞滑雪服,乙二醇分子中碳、氢、氧的原子个数比为 , 2mol乙二醇中含有个分子。(2)、制作冰壶的花岗岩主要含SiO2 , 其中硅元素的化合价为。(3)、往届奥运会的火炬常用丙烷(化学式为C3H8)做燃料,北京冬奥会火炬的燃料是氢气,用氢气代替丙烷做燃料的优点是。
四、综合题
-
19.(1)、具有漂白功能的洗衣粉中添加了过碳酸钠(化学式为2Na2CO3·3H2O2)。查阅资料得知过碳酸钠易溶于水,其溶液中只含有两种溶质,它们分别含有两种元素和三种元素。兴趣小组通过实验进行探究这两种溶质。
步骤
实验内容和操作
实验现象
结论
①
将适量过碳酸钠固体溶于水
无色溶液
②
将上述溶液加入盛有二氧化锰固体的试管,试管门放置带火星的木条。
有气泡生成,带火星的木条复燃
生成的气体是
③
待上述反应完全后,将上层清液分为三份。取第一份清液,用洁净的铂丝蘸取后,在火焰上加热
火焰的颜色为
溶质中含有钠元素
④
取第二份清液于试管中,滴加(填试剂的名称)
无色溶液变为红色
溶液呈碱性
⑤
取第一份清液于试管中,滴加足量盐酸
有气泡生成
溶质中含有(填原子团的名称)
(2)、步骤⑤中生成的气体可以用澄清石灰水检验,请写出该反应的化学方程式。(3)、根据步骤①②推测过碳酸钠水溶液中含有的溶质是(填化学式,下同),根据步骤③④⑤推测过碳酸钠水溶液中含有的溶质是。(4)、选择与步骤⑤中不同类的试剂,设计实验代替步骤⑤完成检验。20. 苦卤主要含有水、氯化钠和硫酸镁,某化工厂欲用苦卤为原料制备硫酸镁。(1)、查阅资料,不同温度下氯化钠、硫酸镁、七水合硫酸镁的溶解度(见表1)和溶解度曲线(见图1)。
温度
20℃
50℃
70℃
溶解度(g/100g水)
氯化钠
36
37
37.8
硫酸镁
33.5
49
37.8
七水合硫酸镁
106
207
253
表1
①硫酸镁的溶解度曲线是(请字母编号)。
②50℃的饱和氯化钠溶液质量分数为。
(2)、该化工厂根据20℃时原料苦卤的成分(见表2),设计了两套生产硫酸镁的方案。资料:硫酸镁从溶液中析出时会带有结晶水形成七水合硫酸镁晶体,200℃烘干能使其完全失去结晶水。
水
氯化钠
硫酸镁
100g
36g
24g
表2
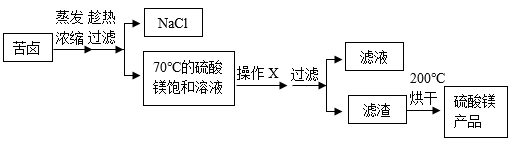
方案一:
方案二:
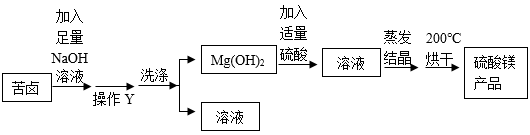
①操作X、操作Y的名称分别是 , 。
②方案中有酸和碱发生的反应,写出该反应的化学方程式。
③方案二中若要使160g苦卤完全沉淀出Mg(OH)2 , 根据化学方程式计算至少要加多少摩尔NaOH?。
④若两套方案使用相同质量的苦卤进行生产,请比较产品中硫酸镁的质量:m(方案一)m(方案二)。(填“<”、“>”或“=”)
⑤请从产品纯度角度分析、比较两套方案。
21. 化学社团为测定水中氢、氧元素质量比,用如下装置设计实验。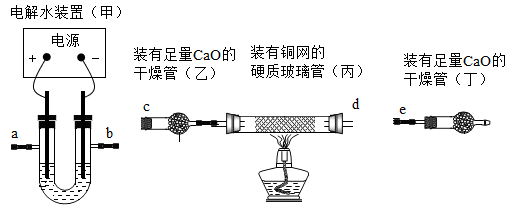 (1)、用电解水的产物制备氧化铜
(1)、用电解水的产物制备氧化铜①请写出电解水的化学方程式。
②连接ac,打开电源,点燃酒精灯,一段时间后,丙中观察到的现象为。
③熄灭酒精灯,断开ac,冷却装置待用。
(2)、化学社团的同学提出:连接bc、de,用电解水的产物还原上述制备的氧化铜,可以通过称量各装置反应前后的质量差(下表所示)来测定水中氢、氧元素质量比装置编号
甲
乙
丙
丁
反应前后的质量差(单位:g)
m1
m2
m3
m4
①要达到测定目的,必须称量的装置为。(填写装置编号)
②实验时,打开电源,过段时间后,再点燃酒精灯的目的是。写出丙装置中发生反应的化学方程式。
③实验测得数值要与理论值作比较,理论上水中氢、氧元素质量比:。
④若其他操作无误,在实验结束时的操作为熄灭酒精灯→拆卸装置→冷却后称量,则实验测得水中的氢、氧元素质量比的数值会有怎样的变化?并解释原因。。
-