山东省淄博市周村区2022年中考一模化学试题
试卷更新日期:2022-05-16 类型:中考模拟
一、单选题
-
1. 分类法是学习化学的重要方法之一。下列说法正确的是( )A、钙、铁、锌、硒都是人体所需微量元素 B、合金、塑料、合成纤维都是合成材料 C、CO、SO2、PM2.5都是空气污染物 D、一氧化碳、甲烷、乙醇都是有机物2. “宏观辨识与微观探析”是化学学科的核心素养之一。下列关于宏观和微观间联系的叙述错误的是( )A、分离液态空气制氧气,说明分子可以再分 B、切洋葱时可闻到刺激性气味,说明分子在不断运动 C、6000L氧气可以压缩进40L的钢瓶中,说明加压可使分子间的间隔变小 D、酸碱中和反应都生成水,其实质是H+与OH-结合生成了H2O3. 规范的实验操作是进行化学实验的重要保障。下列有关实验操作的说法中,不合理的是( )A、给试管中的液体加热时,试管口不可对着自己或他人 B、实验室用CO还原Fe2O3 , 应先通入CO气体,然后用酒精喷灯加热 C、稀释浓硫酸时,把浓硫酸沿器壁慢慢注入水中,并不断搅拌 D、测定某溶液的pH,应先用蒸馏水将pH试纸润湿,再进行测定4. 归纳总结是学习化学的基本方法。下列知识点归纳完全正确的是( )
A化学与健康
B化学与环境
霉变的大米煮熟后可以食用
禁止食用甲醛溶液浸泡过的海产品
人体缺乏维生素C会引起坏血病
明矾可以将硬水转化为软水
为了节约和环保,分类回收生活垃圾
随意丢弃塑料制品会造成“白色污染”
C化学与农业
D化学与生活
常用熟石灰改良酸性土壤
硝酸钾、碳酸钾都是常用的钾肥
农业上采用喷灌和滴灌可节约用水
玻璃钢、钢筋混凝土都属于复合材料
炒菜时油锅着火可用锅盖盖灭
糖类、油脂和蛋白质都可以为生命体提供能量
A、A B、B C、C D、D5. 科学家用滤纸和二氧化钛(TiO2)制出一种“纳米纸”。在纳米纸上“铺”一层“萘胺”(C10H9N)染料制成试纸,用于检测食品中亚硝酸盐(主要是NaNO2)浓度的高低。下列说法正确的是( )A、二氧化钛中Ti的化合价为+2 B、该试纸属于混合物 C、TiO2和NaNO2都属于氧化物 D、萘胺是由碳、氢、氮三种原子构成的6. 10℃时,将3g甲、乙两种可溶性固体分别放入盛有10mL水的试管中。两种物质的溶解情况见图Ⅰ,两种物质的溶解度随温度的变化见图Ⅱ。下面对甲、乙两种物质的判断正确的是( )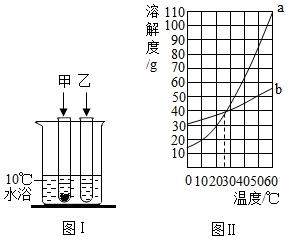 A、图Ⅰ甲、乙两物质的溶液可能都是饱和溶液 B、乙物质对应的溶解度曲线为b C、若温度升高至25℃,试管中甲、乙两物质的溶质质量分数均不变 D、图Ⅰ甲溶液中溶质与溶液的质量比为1:57. 下列实验设计不能达到实验目的的是( )
A、图Ⅰ甲、乙两物质的溶液可能都是饱和溶液 B、乙物质对应的溶解度曲线为b C、若温度升高至25℃,试管中甲、乙两物质的溶质质量分数均不变 D、图Ⅰ甲溶液中溶质与溶液的质量比为1:57. 下列实验设计不能达到实验目的的是( )选项
实验目的
实验设计
A
验证铜、银、铁三种金属的活动性顺序
用铜丝、AgNO3和FeSO4溶液进行实验
B
鉴别H2SO4、Ba(OH)2、CuCl2三种溶液
不用其它试剂即可鉴别
C
除去CO2中的CO杂质
通过灼热的铜丝网
D
配制50g质量分数为10%的NaCl溶液
称取5g NaCl加入45mL水中完全溶解
A、A B、B C、C D、D8. 近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与储存,过程如图所示: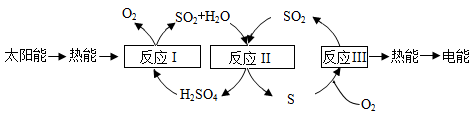
下列说法错误的是( )
A、整个流程最终实现太阳能转化为电能 B、反应Ⅰ属于分解反应,有三种物质生成 C、反应Ⅱ中催化剂在反应前后质量和化学性质不变 D、反应Ⅲ中发出蓝紫色火焰,产生无色无味的气体9. 我国是口罩生产大国。佩戴口罩可以有效阻挡新冠病毒的传播。制造口罩用的熔喷布的主要成分是聚丙烯(部分结构如图所示),生产聚丙烯的原料是石油。下列说法错误的是( ) A、从石油到聚丙烯的转化过程中一定有化学变化发生 B、口罩可滤去大部分附着有病毒的可吸入颗粒物和小液滴 C、点燃口罩,用干冷的小烧杯罩在火焰上方,烧杯内壁有水雾出现 D、点燃聚丙烯,会闻到一种刺鼻性气味10. 如图所示进行有关物质的性质实验,下列说法正确的是( )
A、从石油到聚丙烯的转化过程中一定有化学变化发生 B、口罩可滤去大部分附着有病毒的可吸入颗粒物和小液滴 C、点燃口罩,用干冷的小烧杯罩在火焰上方,烧杯内壁有水雾出现 D、点燃聚丙烯,会闻到一种刺鼻性气味10. 如图所示进行有关物质的性质实验,下列说法正确的是( ) A、甲处发生的反应体现了二氧化碳的还原性 B、乙处发生的反应为置换反应 C、丙处试管可以防止液体倒吸 D、将丁出氢氧化钠溶液改为澄清石灰水,可检验乙处反应生成的二氧化碳11. 结构决定性质,性质决定用途,下列对应关系错误的是( )A、石墨、金刚石的硬度不同,原因是碳原子排列方式不同 B、活性炭多孔,可用于制糖工业脱色 C、稀盐酸可以与常见金属氧化物反应,所以常用来金属除锈 D、CO和CO2组成元素相同,化学性质相似12. 有一种人造氢原子(可表示为H)的原子核中有3个中子,它可以结合成H2分子。下列对每个H2分子的描述错误的是( )A、含有2个原子 B、含有2个质子 C、相对分子质量为6 D、含有2个电子13. 下列物质的用途主要利用其化学性质的是( )A、生石灰用作干燥剂 B、液氮用于医疗手术 C、金刚石用作玻璃刀 D、铝制成铝箔用于包装14. 核电荷数为6的元素组成了神奇的新材料石墨烯,下列关于该元素的说法正确的是( )A、属于金属元素 B、原子核外电子数为6 C、化学性质活泼 D、空气中不含该元素15. 下列反应方程式正确且书写正确的是( )A、正常雨水的pH值接近5.6的原因:CO2+H2O=H2CO3 B、证明铜的活动性比银强:Cu+2AgCl=CuCl2+2Ag C、医疗上用氢氧化镁中和过多胃酸:Mg(OH)2+2HCl=MgCl2+H2O D、用稀硫酸除铁锈:H2SO4+FeO=FeSO4+H2O
A、甲处发生的反应体现了二氧化碳的还原性 B、乙处发生的反应为置换反应 C、丙处试管可以防止液体倒吸 D、将丁出氢氧化钠溶液改为澄清石灰水,可检验乙处反应生成的二氧化碳11. 结构决定性质,性质决定用途,下列对应关系错误的是( )A、石墨、金刚石的硬度不同,原因是碳原子排列方式不同 B、活性炭多孔,可用于制糖工业脱色 C、稀盐酸可以与常见金属氧化物反应,所以常用来金属除锈 D、CO和CO2组成元素相同,化学性质相似12. 有一种人造氢原子(可表示为H)的原子核中有3个中子,它可以结合成H2分子。下列对每个H2分子的描述错误的是( )A、含有2个原子 B、含有2个质子 C、相对分子质量为6 D、含有2个电子13. 下列物质的用途主要利用其化学性质的是( )A、生石灰用作干燥剂 B、液氮用于医疗手术 C、金刚石用作玻璃刀 D、铝制成铝箔用于包装14. 核电荷数为6的元素组成了神奇的新材料石墨烯,下列关于该元素的说法正确的是( )A、属于金属元素 B、原子核外电子数为6 C、化学性质活泼 D、空气中不含该元素15. 下列反应方程式正确且书写正确的是( )A、正常雨水的pH值接近5.6的原因:CO2+H2O=H2CO3 B、证明铜的活动性比银强:Cu+2AgCl=CuCl2+2Ag C、医疗上用氢氧化镁中和过多胃酸:Mg(OH)2+2HCl=MgCl2+H2O D、用稀硫酸除铁锈:H2SO4+FeO=FeSO4+H2O二、填空题
-
16. 新型高导热镁合金常用作电动汽车和消费电子产品的散热器。请根据如图回答有关问题。
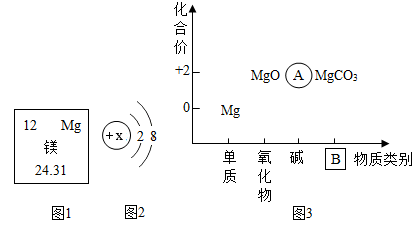 (1)、由图1可知,镁的相对原子质量为 。(2)、图2为镁离子的结构示意图,则x的数值为 , 表示镁离子的符号为 。(3)、以化合价为纵坐标、物质类别为横坐标所绘制的图叫价类二维图。图3为镁的价类二维图,B处的物质类别是 。价类二维图中的物质在一定条件下可以相互转化,例如金属镁和水发生反应可以生成A和一种可燃性单质,则该反应的化学方程式为 。17. 化学与生活息息相关。(1)、如图是某电子产品拆解图片。图中标示的材料属于有机合成材料的是;选择钛合金作为螺丝材料,是因为合金的硬度比组成金属的硬度(填“大”或“小”)。
(1)、由图1可知,镁的相对原子质量为 。(2)、图2为镁离子的结构示意图,则x的数值为 , 表示镁离子的符号为 。(3)、以化合价为纵坐标、物质类别为横坐标所绘制的图叫价类二维图。图3为镁的价类二维图,B处的物质类别是 。价类二维图中的物质在一定条件下可以相互转化,例如金属镁和水发生反应可以生成A和一种可燃性单质,则该反应的化学方程式为 。17. 化学与生活息息相关。(1)、如图是某电子产品拆解图片。图中标示的材料属于有机合成材料的是;选择钛合金作为螺丝材料,是因为合金的硬度比组成金属的硬度(填“大”或“小”)。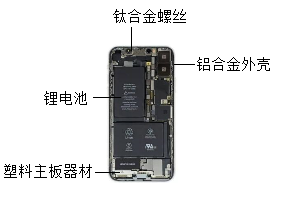 (2)、常用的电池内部填有氯化铵和二氧化锰等物质,若通过分离得到氯化铵,在实验室需进行的操作是溶解、过滤和 , 得到的氯化铵在农业上又可用作 , 其使用的主意事项是。
(2)、常用的电池内部填有氯化铵和二氧化锰等物质,若通过分离得到氯化铵,在实验室需进行的操作是溶解、过滤和 , 得到的氯化铵在农业上又可用作 , 其使用的主意事项是。三、综合题
-
18. 根据如图所示的实验回答相关问题。
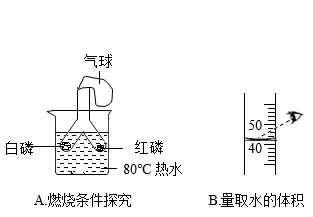
 (1)、A实验中白磷燃烧,红磷不燃烧,可得出的燃烧条件是。(2)、配制一定溶质质量分数的溶液时,在其他操作和步骤均正确的情况下,B操作会使所得溶液的溶质质量分数(填“偏大”、“偏小”或“不变”)。(3)、C实验(填“能”或“不能”)用于验证质量守恒定律。在此过程中燃烧掉的蜡烛质量(填“大于”、“小于”或“等于”)生成的二氧化碳和水蒸气的质量之和。(4)、D实验可用于研究CO2与NaOH溶液的反应。关闭弹簧夹K,将NaOH溶液全部挤入烧瓶,振荡。最后打开弹簧夹K时,观察到的实验现象是。19. 实验室制取气体时需要的一些装置如图所示。请回答下列问题。
(1)、A实验中白磷燃烧,红磷不燃烧,可得出的燃烧条件是。(2)、配制一定溶质质量分数的溶液时,在其他操作和步骤均正确的情况下,B操作会使所得溶液的溶质质量分数(填“偏大”、“偏小”或“不变”)。(3)、C实验(填“能”或“不能”)用于验证质量守恒定律。在此过程中燃烧掉的蜡烛质量(填“大于”、“小于”或“等于”)生成的二氧化碳和水蒸气的质量之和。(4)、D实验可用于研究CO2与NaOH溶液的反应。关闭弹簧夹K,将NaOH溶液全部挤入烧瓶,振荡。最后打开弹簧夹K时,观察到的实验现象是。19. 实验室制取气体时需要的一些装置如图所示。请回答下列问题。 (1)、写出图中标有序号的仪器的名称:①;②。(2)、在实验室连接B、D装置进行实验,若D中蜡烛燃烧得更剧烈,则B中反应的化学方程式为。(3)、CO2能用向上排空气法收集,是因为;若用E装置干燥二氧化碳气体,E中应盛放的药品名称为 , 气体从端通入。(4)、SO2易溶于水,溶于水可生成亚硫酸,实验室常用亚硫酸钠固体和稀硫酸反应常温下制取SO2 , 若想控制反应速率,图中最适宜的发生装置是。F实验中可观察到试管内。20. 为解决能源与环境问题,有学者提出如图所示的含碳物质转化的技术路线。
(1)、写出图中标有序号的仪器的名称:①;②。(2)、在实验室连接B、D装置进行实验,若D中蜡烛燃烧得更剧烈,则B中反应的化学方程式为。(3)、CO2能用向上排空气法收集,是因为;若用E装置干燥二氧化碳气体,E中应盛放的药品名称为 , 气体从端通入。(4)、SO2易溶于水,溶于水可生成亚硫酸,实验室常用亚硫酸钠固体和稀硫酸反应常温下制取SO2 , 若想控制反应速率,图中最适宜的发生装置是。F实验中可观察到试管内。20. 为解决能源与环境问题,有学者提出如图所示的含碳物质转化的技术路线。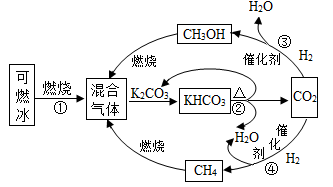 (1)、“可燃冰”中甲烷完全燃烧的化学方程为。反应②的化学方程式为 , 该反应基本类型是。(2)、反应④中,参加反应的CO2和生成的CH4的分子数目之比为。(3)、该技术路线有利用于实现____(填标号)。A、碳循环利用 B、减少碳排放 C、减少白色污染21. 在学习复分解反应发生的条件后,同学们利用已学知识,对稀盐酸与四种化合物溶液之间能否发生反应作出判断,并进行如图的实验验证:
(1)、“可燃冰”中甲烷完全燃烧的化学方程为。反应②的化学方程式为 , 该反应基本类型是。(2)、反应④中,参加反应的CO2和生成的CH4的分子数目之比为。(3)、该技术路线有利用于实现____(填标号)。A、碳循环利用 B、减少碳排放 C、减少白色污染21. 在学习复分解反应发生的条件后,同学们利用已学知识,对稀盐酸与四种化合物溶液之间能否发生反应作出判断,并进行如图的实验验证: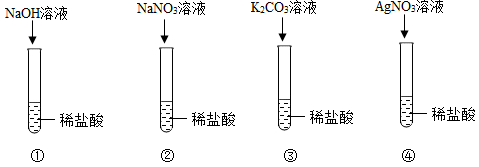 (1)、实验③观察到的现象是 , 实验②中不能发生反应的原因是 , 实验④的化学方程式是。(2)、【提出问题】如何证明没有明显实验现象的物质间发生了化学反应?
(1)、实验③观察到的现象是 , 实验②中不能发生反应的原因是 , 实验④的化学方程式是。(2)、【提出问题】如何证明没有明显实验现象的物质间发生了化学反应?【实验方案】以实验①为例,向NaOH溶液中加入以下可选试剂进行实验:酚酞试液、石蕊试液、稀盐酸、氯化铵溶液、硝酸银溶液。
【实验过程】
组号
实验思路
操作
实验现象
结论
1
证明NaOH消失
向NaOH溶液中滴加a,再逐滴加入过量的稀盐酸
溶液先变红色,最终变为无色
稀盐酸与氢氧化钠能发生反应
2
证明NaOH消失
向反应后的溶液中滴入适量氯化铜溶液
b
3
证明NaCl生成
向反应后的溶液中滴入适量AgNO3溶液
有白色沉淀
上表中,a处试剂是 , b处现象是。
(3)、有同学认为组号3实验设计不正确,理由是。四、计算题
-
22. 某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品24.6g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示。请回答:
 (1)、该纯碱样品中Na2CO3的质量分数。(写出计算过程)(2)、根据以上条件,此题还可计算出下列数据中的。(填序号)
(1)、该纯碱样品中Na2CO3的质量分数。(写出计算过程)(2)、根据以上条件,此题还可计算出下列数据中的。(填序号)①该纯碱样品中NaCl的质量分数;
②反应所用稀盐酸中溶质的质量分数;
③20℃时,氯化钠的溶解度;
④反应后所得溶液中NaCl的质量分数。