广东省惠州市2022届高三第一次模拟考试化学试题
试卷更新日期:2022-05-09 类型:高考模拟
一、单选题
-
1. 下列括号中所列高分子材料的主要成分不属于蛋白质的是( )




A.刀枪把(竹木)
B.头盔(羽毛)
C.髯口(毛发)
D.戏衣(丝绸)
A、A B、B C、C D、D2. 下列情况对应的化学知识或原理正确的是( )选项
素质教育
化学知识或原理
A
音乐:“音乐焰火”创造出火树银花不夜天
焰色反应属于化学变化
B
体育:北京冬奥会火炬外壳材料是由高性能树脂与碳纤维融合而成的复合材料
该复合材料具有耐高温、耐腐蚀等优良的特性
C
美术:宋代《千里江山图》中的绿色来自孔雀石颜料[主要成分为Cu(OH)2·CuCO3],青色来自蓝铜矿颜料[主要成分为Cu(OH)2·2CuCO3]
孔雀石、蓝铜矿颜料不易被空气氧化且耐酸、耐碱
D
文学:爆竹声中一岁除,春风送暖入屠苏
传统爆炸粉为黑火药,其主要成分为木炭、硫磺、KClO3
A、A B、B C、C D、D3. 下列相关微粒的化学用语错误的是( )A、中子数为12的钠原子: Na B、石墨和C60互为同素异形体 C、Cl的原子结构示意图: D、的电子式:
D、的电子式: 4. 用所给试剂与图示装置能够制取相应气体的是(夹持仪器略)( )
4. 用所给试剂与图示装置能够制取相应气体的是(夹持仪器略)( )
A
B
C
D
X 中试剂
浓盐酸
浓硫酸
双氧水
浓氨水
Y 中试剂
MnO2
C2H5OH
MnO2
NaOH
气体
Cl2
C2H4
O2
NH3
A、A B、B C、C D、D5. “劳动创造幸福,实干成就伟业”。下列劳动项目所涉及的化学知识错误的是( )选项
劳动项目
化学知识
A
AgBr用来制作照相胶片
AgBr见光易分解
B
NaCl的溶解度随温度变化不大
在盐田中晾晒海水,得到粗盐
C
利用含小苏打的发酵粉烘焙蛋糕
小苏打是碳酸氢钠
D
SiO2制作光导纤维
SiO2导电
A、A B、B C、C D、D6. 萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是( ) A、M和N均能使酸性KMnO4溶液褪色 B、M和N互为同分异构体 C、M分子中所有碳原子均处于同一平面上 D、N能发生取代,消去,加成反应7. 下列选用的仪器和药品能达到实验目的的是( )A、
A、M和N均能使酸性KMnO4溶液褪色 B、M和N互为同分异构体 C、M分子中所有碳原子均处于同一平面上 D、N能发生取代,消去,加成反应7. 下列选用的仪器和药品能达到实验目的的是( )A、 加热熔融的氢氧化钠固体
B、
加热熔融的氢氧化钠固体
B、 吸收CO2中的HCl杂质
C、
吸收CO2中的HCl杂质
C、 蒸馏时的接收装置
D、
蒸馏时的接收装置
D、 吸收尾气中的Cl2
8. 硫及其化合物的“价−类”二维图体现了化学变化之美。下列有关说法正确的是( )
吸收尾气中的Cl2
8. 硫及其化合物的“价−类”二维图体现了化学变化之美。下列有关说法正确的是( )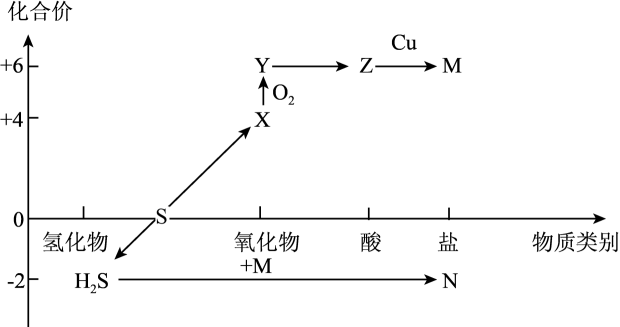 A、燃煤时为减少X的排放,可在煤中添加石灰石 B、X有漂白性,可使石蕊试液先变红后褪色 C、Z与铁反应时,Z的浓度越大,反应速率越快 D、N可由其相应单质直接化合生成9. 设NA为阿伏加德罗常数的值。下列说法正确的是( )A、32g甲醇中含有C-H键的数目为4NA B、1 molFe溶于过量稀硫酸,转移的电子数目为3NA C、0.1 mol·L- 1H2S溶液中含有阳离子总数为0.2 NA D、标准状况下,22.4LN2和O2混合气中含有的原子数为2NA10. 联氨(N2H4)可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中一种反应机理如图所示。下列叙述错误的是( )
A、燃煤时为减少X的排放,可在煤中添加石灰石 B、X有漂白性,可使石蕊试液先变红后褪色 C、Z与铁反应时,Z的浓度越大,反应速率越快 D、N可由其相应单质直接化合生成9. 设NA为阿伏加德罗常数的值。下列说法正确的是( )A、32g甲醇中含有C-H键的数目为4NA B、1 molFe溶于过量稀硫酸,转移的电子数目为3NA C、0.1 mol·L- 1H2S溶液中含有阳离子总数为0.2 NA D、标准状况下,22.4LN2和O2混合气中含有的原子数为2NA10. 联氨(N2H4)可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中一种反应机理如图所示。下列叙述错误的是( ) A、①转化中N2H4是还原剂 B、工业上也可使用Na2SO3处理锅炉水中的溶解氧 C、1mol N2H4可处理水中1.5 molO2 D、③中发生反应后溶液的pH增大11. 短周期元素W、X、Y、Z构成的化合物结构式如图所示,其中W、Y原子的最外层都满足8电子结构;W、X同主族,W、Y同周期,Z的一种同位素原子是核聚变的原料,Y是海水中含量最多的元素。下列说法错误的是( )
A、①转化中N2H4是还原剂 B、工业上也可使用Na2SO3处理锅炉水中的溶解氧 C、1mol N2H4可处理水中1.5 molO2 D、③中发生反应后溶液的pH增大11. 短周期元素W、X、Y、Z构成的化合物结构式如图所示,其中W、Y原子的最外层都满足8电子结构;W、X同主族,W、Y同周期,Z的一种同位素原子是核聚变的原料,Y是海水中含量最多的元素。下列说法错误的是( ) A、原子半径:Y>Z B、最高价氧化物的水化物的酸性:W>X C、最简单氢化物的稳定性:W>Y D、W组成的某些化合物可以造成水体富营养化12. 下列离子方程式书写正确的是( )A、氨水与稀盐酸反应:OH−+H+=H2O B、FeI2溶液中加入足量的Br2:2Fe2++4I-+3Br2=2Fe3++2I2+6Br- C、Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++SO=BaSO4↓+H2O D、大理石与稀盐酸反应:CO+2H+=CO2↑+H2O13. N2O和CO是环境污染性气体,可在Pt2O+表面转化为无害气体,有关化学反应的物质变化过程及能量变化过程分别如图甲、乙所示。下列说法错误的是( )
A、原子半径:Y>Z B、最高价氧化物的水化物的酸性:W>X C、最简单氢化物的稳定性:W>Y D、W组成的某些化合物可以造成水体富营养化12. 下列离子方程式书写正确的是( )A、氨水与稀盐酸反应:OH−+H+=H2O B、FeI2溶液中加入足量的Br2:2Fe2++4I-+3Br2=2Fe3++2I2+6Br- C、Ba(OH)2溶液与稀硫酸反应:Ba2++OH-+H++SO=BaSO4↓+H2O D、大理石与稀盐酸反应:CO+2H+=CO2↑+H2O13. N2O和CO是环境污染性气体,可在Pt2O+表面转化为无害气体,有关化学反应的物质变化过程及能量变化过程分别如图甲、乙所示。下列说法错误的是( )
 A、总反应为N2O(g)+CO(g)=CO2(g)+N2(g) ΔH=ΔH1+ΔH2 B、为了实现转化,需不断向反应器中补充Pt2O+和Pt2O C、该反应正反应的活化能小于逆反应的活化能 D、总反应的ΔH=-226 kJ·mol-114. 研究反应2CO2(g)+6H2(g)CH3CH2OH(g)+3H2O(g) , 对实现“碳中和”有重要意义。在密闭容器中充入1molCO2与3mol H2 , 发生上述反应并达平衡,测得平衡体系中各种物质的体积分数随温度变化如图所示。下列说法正确的是( )
A、总反应为N2O(g)+CO(g)=CO2(g)+N2(g) ΔH=ΔH1+ΔH2 B、为了实现转化,需不断向反应器中补充Pt2O+和Pt2O C、该反应正反应的活化能小于逆反应的活化能 D、总反应的ΔH=-226 kJ·mol-114. 研究反应2CO2(g)+6H2(g)CH3CH2OH(g)+3H2O(g) , 对实现“碳中和”有重要意义。在密闭容器中充入1molCO2与3mol H2 , 发生上述反应并达平衡,测得平衡体系中各种物质的体积分数随温度变化如图所示。下列说法正确的是( ) A、表示CH3CH2OH组分的曲线是Ⅲ B、图中曲线交点a对应的转化率大于交点b C、图中曲线交点a、b对应反应平衡常数Ka<Kb D、若使用催化剂,则b点向上移动15. 可用于检测CO的某气敏传感器的工作原理如图所示。下列说法错误的是( )
A、表示CH3CH2OH组分的曲线是Ⅲ B、图中曲线交点a对应的转化率大于交点b C、图中曲线交点a、b对应反应平衡常数Ka<Kb D、若使用催化剂,则b点向上移动15. 可用于检测CO的某气敏传感器的工作原理如图所示。下列说法错误的是( ) A、工作过程中化学能转化为电能 B、工作一段时间后溶液的pH几乎不变 C、电极I上发生反应:CO - 2e- + H2O = CO2 + 2H+ D、电极II上发生反应:O2 + 2H2O + 4e- = 4OH16. 向100mL 0.1mol·L-1K2CO3溶液中缓慢滴加100mL 0.2mol·L-1盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(H+和OH-未画出),已知:碳酸的电离平衡常数Ka1=4.31×10-7 , Ka2=5.60×10-11 , 下列说法错误的是( )
A、工作过程中化学能转化为电能 B、工作一段时间后溶液的pH几乎不变 C、电极I上发生反应:CO - 2e- + H2O = CO2 + 2H+ D、电极II上发生反应:O2 + 2H2O + 4e- = 4OH16. 向100mL 0.1mol·L-1K2CO3溶液中缓慢滴加100mL 0.2mol·L-1盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(H+和OH-未画出),已知:碳酸的电离平衡常数Ka1=4.31×10-7 , Ka2=5.60×10-11 , 下列说法错误的是( ) A、滴加至A点时, B、滴加至B点时, C、滴加至C点时, D、滴加至D点时,溶液的pH<7
A、滴加至A点时, B、滴加至B点时, C、滴加至C点时, D、滴加至D点时,溶液的pH<7二、综合题
-
17. 为检验溶液中是否含有Cl- , 某同学采用向溶液中先加HNO3 , 再加AgNO3 , 若有白色沉淀生成,则证明有Cl-。对此结论,有人提出了质疑,溶液中可能有SO , 设计了如下探究性实验。(1)、实验一:向Na2SO4溶液中滴加AgNO3溶液
编号
Na2SO4溶液
AgNO3溶液
现象
体积
mL
浓度
mol·L−1
体积
滴
浓度
mol·L−1
混合后Ag+浓度mol·L−1
①
1
1
3
2
0.2
出现大量白色沉淀
②
1
1
3
0.5
0.05
出现少量白色沉淀
③
1
1
3
0.1
0.01
有些许浑浊
④
1
1
3
0.01
0.001
无明显变化
实验一中产生沉淀的离子方程式为。
(2)、已知:25℃时Ksp(Ag2SO4)=1.2×10-5 , Ksp(AgCl)=1.8×10-10实验一中编号④无明显变化,若要产生浑浊,溶液中c(SO)理论上至少达到mol·L−1。若向l mL某浓度的NaCl与Na2SO4混合溶液中加入3滴0.1mol·L−1AgNO3溶液,分析上面数据,判断下列说法正确的是(填字母序号)。
A.混合液中c(SO)=1mol·L−1时不会产生Ag2SO4沉淀
B.混合液中c(SO)=0.1 mol·L−1时不会产生Ag2SO4沉淀
C.无论SO浓度大小都会产生Ag2SO4沉淀
D.若使用0.01 mol·L−1AgNO3溶液,可基本排除SO对Cl-检验构成的干扰
(3)、将实验一编号③中的理论计算结果与现象对照,发现理论上大部分Ag+应该形成沉淀,这与“有些许浑浊”的现象相矛盾。为探究真相,在实验一的基础上继续设计了以下实验。实验二:
编号
AgNO3浓度/mol·L−1
现象
滴加硝酸后的现象
①
2
出现大量白色沉淀
滴加稀硝酸,沉淀大量溶解;改加浓硝酸,沉淀较快消失
②
0.5
出现少量白色沉淀
滴加稀硝酸,沉淀基本消失
对于Ag2SO4溶于硝酸的原因提出了如下假设,请完成假设二。
假设一:NO对Ag2SO4溶解起作用。
假设二:。
(4)、选择适当试剂并设计实验方案,分别验证假设一和假设二是否成立。请写出实验步骤和现象。编号
操作
现象
结论
①
取少量Ag2SO4于试管中,加入2mL水,振荡
固体不溶解
②
将①的浊液分成两等份
③
向其中一份加入1mL0.1mol/L的NaNO3 , 振荡
假设一不成立
④
向另一份加入
假设二成立
(5)、通过(4)的实验,请用平衡理论解释Ag2SO4溶解的原因。(已知:H2SO4=H++HSO、HSOH++SO)。(6)、用硝酸银滴定法,可以测定水体中氯化物的含量。洗涤沉淀必须干燥后才能称量,沉淀完全干燥的判断方法是。18. 锂在新能源等领域应用广泛。从粉煤灰(含Al2O3、Fe2O3、Li2O、SiO2等)中回收提取铝、锂元素的化合物的流程如图所示:
已知:碳酸锂的溶解度(g·L-1)见表。
温度/℃
0
10
20
30
40
50
60
80
100
Li2CO3
1.54
1.43
1.33
1.25
1.17
1.08
1.01
0.85
0.72
回答下列问题
(1)、“粉碎”的目的是 , 滤渣1的成分主要是。(填化学式)(2)、“调pH”的目的是沉淀Fe3+、Al3+。当离子浓度≤1.0×10-5mol·L-1时表示该离子沉淀完全。常温下,如果溶液pH=4,Fe3+、Al3+ (填“能”或“否”)均沉淀完全,若沉淀完全,此时溶液中c(Fe3+)、c(Al3+)之比为。(已知:Ksp[Fe(OH)3]=8.0×10-38 , Ksp[Al(OH)3]=2.0×10-33)(3)、从滤渣2中分离出Al(OH)3 , 可用如图所示方法,试剂X是 , “步骤2”中主要发生的离子反应方程式有OH-+CO2=HCO、。 (4)、“沉锂”中的“一系列操作”依次为蒸发浓缩、、洗涤、干燥。检验母液主要溶质的阴离子所用的试剂为。母液的用途(任写一种)。(5)、太阳能路灯蓄电池是磷酸铁锂电池,其工作原理如图所示。电池总反应式为LixC6 + Li1−xFePO4 LiFePO4 + 6C。试写出充电时,该电池正极材料上的反应式:。
(4)、“沉锂”中的“一系列操作”依次为蒸发浓缩、、洗涤、干燥。检验母液主要溶质的阴离子所用的试剂为。母液的用途(任写一种)。(5)、太阳能路灯蓄电池是磷酸铁锂电池,其工作原理如图所示。电池总反应式为LixC6 + Li1−xFePO4 LiFePO4 + 6C。试写出充电时,该电池正极材料上的反应式:。 19. 温室气体的利用是当前环境和能源领域的研究热点,合理利用燃料废气中的CO2 , 也是实现“碳中和”的途径之一。(1)、I.温室气体CO2转化为重要的工业原料甲酸是目前科学研究的热点。回答下列问题:
19. 温室气体的利用是当前环境和能源领域的研究热点,合理利用燃料废气中的CO2 , 也是实现“碳中和”的途径之一。(1)、I.温室气体CO2转化为重要的工业原料甲酸是目前科学研究的热点。回答下列问题:已知:①CO(g)+H2O(g) HCOOH(g) △H1=−72.6kJ·mol−1
②2CO(g)+O2(g) 2CO2(g) △H2=−566.0kJ·mol−1
则反应③的平衡常数表达式K= , 写出反应③的热化学方程式。
(2)、刚性绝热密闭容器中,等物质的量的CO2(g)和H2O(g)发生反应③,下列可判断反应达到平衡的是____(填标号)。A、CO2(g)和H2O(g)的物质的量之比不变 B、容器中气体平均摩尔质量不变 C、2υ正(CO2)= υ逆(O2) D、容器内温度不变(3)、在催化剂作用下CO2和H2也可以合成甲酸,主要涉及以下反应:i.СО2(g)+Н2(g) НСООН(g) △H3<0
ii.CO2(g)+H2(g) CO(g)+H2O(g) △H4
刚性密闭容器中CO2(g)和H2(g)按物质的量1:1投料,平衡时HCOOH和CO的选择性随温度变化如图所示。(选择性是指转化成目标产物的反应物在实际消耗的反应物中的占比)

①曲线a随温度升高而下降的原因是;为同时提高CO2的平衡转化率和平衡时HCOOH的选择性,应选择的反应条件为(填标号)。
A. 低温、低压 B.高温、高压 C.高温、低压 D.低温、高压
②240℃时,容器内压强随时间的变化如下表所示:
时间/min
0
20
40
60
80
压强/MPa
p0
0.91p0
0.85p0
0.80p0
0.80p0
反应i的速率可表示为υ=k·p(CO2)·p(H2)(p为气体分压,分压=总压×气体的物质的量分数, k为常数),则反应在60 min时υ=(用含p0、k的式子表示)。
(4)、Ⅱ.CO2−CH4催化重整对减少温室气体的排放、改善大气环境具有重要的意义。在密闭容器中通入物质的量均为0.2mol的CH4和CO2 , 在一定条件下发生反应CH4(g)+CO2(g) 2CO(g)+2H2(g),CH4的平衡转化率与温度及压强的关系如图所示。

①由如图可知:压强p1p2(填“>”、“<”或“=”)。
②Y点:υ(正)υ(逆)(填“>”、“<”或“=”)。
20. 2020年12月17日凌晨1时59分,“嫦娥五号”首次实现了我国地外天体采样返回,标志着我国航天事业迈出了一大步。带回的月壤中包含了H、O、N、Al、S、Cd、Zn、Ti、Cu、Au、Cr等多种元素。回答下列问题:(1)、锌(Zn)、镉(Cd)位于同一副族相邻周期,Cd的原子序数更大,则基态Cd原子的价电子轨道表示式(电子排布图)为。(2)、S与O可形成多种微粒,其中SO的空间构型为;液态SO3冷却到289.8K时,能得到一种螺旋状单链结构的固体,其结构如图所示,此固态SO3中S原子的杂化轨道类型是 。 (3)、重铬酸铵为桔黄色单斜结晶,常用作有机合成催化剂,Cr2O的结构如图所示。则1mol重铬酸铵中含σ键与π键个数比为。
(3)、重铬酸铵为桔黄色单斜结晶,常用作有机合成催化剂,Cr2O的结构如图所示。则1mol重铬酸铵中含σ键与π键个数比为。 (4)、α—Al2O3是“嫦娥五号”中用到的一种耐火材料,具有熔点高(2054℃)、硬度大的特点,主要原因为。(5)、一种铜金合金具有储氢功能,其晶体为面心立方最密堆积结构,晶胞中Cu原子处于面心,Au原子处于顶点,则Au原子的配位数为。该储氢材料储氢时,氢分子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与ZnS的结构相似(如图),该晶体储氢后的化学式为。
(4)、α—Al2O3是“嫦娥五号”中用到的一种耐火材料,具有熔点高(2054℃)、硬度大的特点,主要原因为。(5)、一种铜金合金具有储氢功能,其晶体为面心立方最密堆积结构,晶胞中Cu原子处于面心,Au原子处于顶点,则Au原子的配位数为。该储氢材料储氢时,氢分子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与ZnS的结构相似(如图),该晶体储氢后的化学式为。 (6)、“嫦娥五号”某核心部件主要成分为纳米钛铝合金,其结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),已知该结构单元底面(正六边形)边长为anm,该合金的密度为ρg·cm-3 , 则高为h=nm(列出计算式,NA为阿伏加德罗常数的值)。
(6)、“嫦娥五号”某核心部件主要成分为纳米钛铝合金,其结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),已知该结构单元底面(正六边形)边长为anm,该合金的密度为ρg·cm-3 , 则高为h=nm(列出计算式,NA为阿伏加德罗常数的值)。 21. H是药物合成中的一种重要中间体,下面是H的一种合成路线:
21. H是药物合成中的一种重要中间体,下面是H的一种合成路线:

回答下列问题:
(1)、X的结构简式为 , 其中所含官能团的名称为;Y生成Z的反应类型为。(2)、Z的分子式为;R的化学名称是。(3)、由Z和E合成F的化学方程式为。(4)、同时满足苯环上有4个取代基,且既能发生银镜反应,又能发生水解反应的Y的同分异构体有种,其中核磁共振氢谱上有4组峰,峰面积之比为1∶2∶2∶3的同分异构体的结构简式为(一种即可)。(5)、参照上述合成路线,以乙醛和 为原料(其他试剂任选),设计制备肉桂醛(
为原料(其他试剂任选),设计制备肉桂醛( )的合成路线。
)的合成路线。