河南省安阳市滑县2022年中考模拟化学试题
试卷更新日期:2022-05-06 类型:中考模拟
一、单选题
-
1. 生话中的下列变化属于化学变化的是( )A、水果榨汁 B、燃气燃烧 C、轮胎爆裂 D、电灯通电发光2. 在测定锌,铟等元素的相对原子质量方面做出卓越贡献的中国科学家是( )A、张青莲 B、屠呦呦 C、袁隆平 D、侯德榜3. 为强化地下水资源节约与保护,我国《地下水管理条例》自2021年12月1日起施行。下列说法或做法正确的是( )A、可用活性炭吸附地下水中泥沙 B、利用高压泵把废水打入地下,避免污染河流 C、大力开采地下水,缓解水资源的短缺 D、利用化学技术,加强地下水监测4. 下图所示实验操作,正确的是( )A、
 称量固体氢氧化钠
B、
称量固体氢氧化钠
B、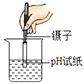 测溶液pH
C、
测溶液pH
C、 过滤
D、
过滤
D、 稀释浓硫酸
5. 2022年北京、张家口将联合举办冬奥会,为办成绿色奥运,下列措施不可行的是( )A、发展公共交通,提倡绿色出行 B、采用脱硫技术,减少SO2的排放 C、大力发展太阳能、风能等新能源 D、加高燃煤锅炉烟囱,将废气排到高空6. 下列物质的性质和用途关系错误的是( )A、金刚石的硬度大,可用于切割玻璃 B、活性炭具有吸附性,可用于脱色、除异味 C、稀有气体性质不活泼,可用于焊割金属用保护气 D、铝的化学性质稳定,可在铁栏杆的表面涂铝粉防止生锈7. 运用分子的性质判断。以下事实的解释错误的是( )A、新装修的房子中有异味——分子在不断地运动 B、自行车轮胎在阳光下暴晒而炸裂——分子受热,体积变大 C、用扫描隧道显微镜观测到分子——分子的体积很小 D、过氧化氢分解生成水和氧气——化学变化中分子可以再分8. 下列关于实验现象的描述正确的是( )A、硝酸铵固体溶于水,溶液温度升高 B、硫在氧气中燃烧,生成二氧化硫气体 C、打开盛有浓盐酸的试剂瓶盖,瓶口出现白雾 D、将尿素[CO(NH2)2]与熟石灰混合研磨,闻到氨味9. 2020年6月23日,最后一颗北斗卫星在西昌卫星发射中心成功发射。发射时火箭燃料偏二甲肼(C2H8N2)和四氧化二氮发生反应,反应的化学方程式为:。下列有关说法错误的是( )A、X为CO2 B、该反应放出热量 C、该反应产物会污染环境 D、燃烧过程并不一定需要氧气10. 分类、归纳等是化学学习的常用方法。下列分类、归纳中正确的是( )A、混合物:冰水混合物、石油、不锈钢 B、单质:金刚石、液态氧气、水银 C、碱:熟石灰、烧碱、纯碱 D、合成材料:塑料、羊毛纤维、合成橡胶11. 在点燃条件下,A和B反应生成C和D,反应前后分子变化的微观示意图如图所示。下列说法错误的是( )
稀释浓硫酸
5. 2022年北京、张家口将联合举办冬奥会,为办成绿色奥运,下列措施不可行的是( )A、发展公共交通,提倡绿色出行 B、采用脱硫技术,减少SO2的排放 C、大力发展太阳能、风能等新能源 D、加高燃煤锅炉烟囱,将废气排到高空6. 下列物质的性质和用途关系错误的是( )A、金刚石的硬度大,可用于切割玻璃 B、活性炭具有吸附性,可用于脱色、除异味 C、稀有气体性质不活泼,可用于焊割金属用保护气 D、铝的化学性质稳定,可在铁栏杆的表面涂铝粉防止生锈7. 运用分子的性质判断。以下事实的解释错误的是( )A、新装修的房子中有异味——分子在不断地运动 B、自行车轮胎在阳光下暴晒而炸裂——分子受热,体积变大 C、用扫描隧道显微镜观测到分子——分子的体积很小 D、过氧化氢分解生成水和氧气——化学变化中分子可以再分8. 下列关于实验现象的描述正确的是( )A、硝酸铵固体溶于水,溶液温度升高 B、硫在氧气中燃烧,生成二氧化硫气体 C、打开盛有浓盐酸的试剂瓶盖,瓶口出现白雾 D、将尿素[CO(NH2)2]与熟石灰混合研磨,闻到氨味9. 2020年6月23日,最后一颗北斗卫星在西昌卫星发射中心成功发射。发射时火箭燃料偏二甲肼(C2H8N2)和四氧化二氮发生反应,反应的化学方程式为:。下列有关说法错误的是( )A、X为CO2 B、该反应放出热量 C、该反应产物会污染环境 D、燃烧过程并不一定需要氧气10. 分类、归纳等是化学学习的常用方法。下列分类、归纳中正确的是( )A、混合物:冰水混合物、石油、不锈钢 B、单质:金刚石、液态氧气、水银 C、碱:熟石灰、烧碱、纯碱 D、合成材料:塑料、羊毛纤维、合成橡胶11. 在点燃条件下,A和B反应生成C和D,反应前后分子变化的微观示意图如图所示。下列说法错误的是( ) A、参加反应的A和B的质量比为17:8 B、在反应中氮元素和氧元素的化合价都发生了改变 C、生成C和D的分子个数比为1:3 D、一个A分子和一个D分子中均含有10个电子12. 通过一步化学反应实现如图所示的X、Y、Z三种物质间转化,表格中X、Y、Z对应的物质不能实现这种转化的是( )
A、参加反应的A和B的质量比为17:8 B、在反应中氮元素和氧元素的化合价都发生了改变 C、生成C和D的分子个数比为1:3 D、一个A分子和一个D分子中均含有10个电子12. 通过一步化学反应实现如图所示的X、Y、Z三种物质间转化,表格中X、Y、Z对应的物质不能实现这种转化的是( )
X
Y
Z
A
CO2
Na2CO3
CaCO3
B
CuO
Cu(NO3)2
Cu(OH)2
C
HCl
BaCl2
NaCl
D
Mg
MgO
MgCl2
A、A B、B C、C D、D13. 下列图像分别与选项中的实验过程相对应,其中正确的是( )A、 室温下,向一定质量饱和石灰水中加入氧化钙
B、
室温下,向一定质量饱和石灰水中加入氧化钙
B、 向一定量NaOH和Ba(NO3)2混合溶液中加入过量的稀硫酸
C、
向一定量NaOH和Ba(NO3)2混合溶液中加入过量的稀硫酸
C、 等质量的镁和氧气在点燃条件下充分反应
D、
等质量的镁和氧气在点燃条件下充分反应
D、 向等质量、等浓度的稀硫酸中分别加入过量的Zn和Fe
14. 将2.4gMg、6.5gZn、5.6gFe及3.2gCu组成的混合物加入一定量稀硫酸中,充分反应后剩余固体6.0g,则生成氢气的质量是( )A、0.4g B、0.5g C、0.6g D、0.7 g
向等质量、等浓度的稀硫酸中分别加入过量的Zn和Fe
14. 将2.4gMg、6.5gZn、5.6gFe及3.2gCu组成的混合物加入一定量稀硫酸中,充分反应后剩余固体6.0g,则生成氢气的质量是( )A、0.4g B、0.5g C、0.6g D、0.7 g二、填空题
-
15. 人体中含量最多的金属元素是。画出有机物中一定含有的元素的原子结构示意图。16. 我国研制成功的氢能源汽车采用的是液氢作燃料,液氢燃烧的化学方程式为。一些乡村使用的燃料沼气属于(填“可再生”或“不可再生”)能源:关闭家用燃气阀门可使火焰灭火,其灭火原理是。17. 家用消毒剂常用75%的酒精。保存时要远离火源防止其燃烧,写出酒精燃烧的化学方程式。红枣中含有蛋白质、糖类及维生素等营养素,其中起到调节人体新陈代谢、预防疾病作用的营养素是。工厂常用稀盐酸除去铁制品表面的锈蚀。该反应的化学方程式为。18. 铜在加热条件下可以与浓硫酸反应,除生成水外,还生成一种蓝色溶液和造成酸雨的主要气体,该反应的化学方程式为;将木炭与铜粉的混合物在空气中完全灼烧后,发现灼烧前后质量相等,则原混合物中木炭与铜粉的质量之比为(填最简整数比)。19. 室温下将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化的曲线图所示。
 (1)、写出该反应的化学方程式。(2)、稀盐酸与氢氧化钠溶液发生的中和反应是(填“吸热”“放热”或“无热量变化”)反应。20. 烧杯中盛有FeCl2和CuCl2的混合溶液,向其中不断加入足量的锌粒,溶液的质量和加入锌粒的质量关系如图所示,回答下列问题。
(1)、写出该反应的化学方程式。(2)、稀盐酸与氢氧化钠溶液发生的中和反应是(填“吸热”“放热”或“无热量变化”)反应。20. 烧杯中盛有FeCl2和CuCl2的混合溶液,向其中不断加入足量的锌粒,溶液的质量和加入锌粒的质量关系如图所示,回答下列问题。 (1)、写出AB段发生反应的化学方程式。(2)、B点溶液中含有的溶质是。(3)、对D点烧杯中的物质进行过滤,向得到的滤渣中加入稀盐酸,产生的现象是。
(1)、写出AB段发生反应的化学方程式。(2)、B点溶液中含有的溶质是。(3)、对D点烧杯中的物质进行过滤,向得到的滤渣中加入稀盐酸,产生的现象是。三、综合题
-
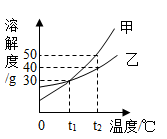
21. 下图是甲、乙两种固体的溶解度曲线。甲和乙的溶解度相等时的温度为℃;t2℃时,分别用甲、乙的固体配制相同质量甲、乙的饱和溶液,所需要水的质量关系为:甲乙(填“大于” “小于”或“等于”);t2℃时,将75g甲的饱和溶液与50g水混合后所得溶液中溶质的质量分数为。
 22. A~E 是初中化学常见的五种不同类别的物质,它们之间的关系如图所示(部分生成物已略去)。其中 E 中金属的质量分数为40%,E 常用于配制农药波尔多液。则 A 与 B、A 与 E 反应所属的基本反应类型为;B 转化为 C 的化学方程式为;D 与 E 反应可观察到的现象为。
22. A~E 是初中化学常见的五种不同类别的物质,它们之间的关系如图所示(部分生成物已略去)。其中 E 中金属的质量分数为40%,E 常用于配制农药波尔多液。则 A 与 B、A 与 E 反应所属的基本反应类型为;B 转化为 C 的化学方程式为;D 与 E 反应可观察到的现象为。 23. 利用如图所示的长柄W形玻璃管(省略夹持仪器)可以进行燃烧条件的微型实验探究。
23. 利用如图所示的长柄W形玻璃管(省略夹持仪器)可以进行燃烧条件的微型实验探究。
向W形玻璃管中放入足量红磷和白磷,塞好橡皮塞,关闭活塞,然后将其放入80℃的热水中。
(1)、实验时玻璃管中可观察到的现象是什么?。(2)、该实验可得出的燃烧条件是什么?。24. 结合如图所示气体制取和收集的几种实验装置,回答下列问题。 (1)、请写出用装置A制取氧气的化学方程式。(2)、某气体只能用E装置收集,写出该气体一定具有的性质。(3)、用F装置可以收集氢气,H2从b管通入,请将装置补画完整。25. 酸、碱、盐是一类重要的化合物。(1)、酸、碱、盐之间发生复分解反应的条件是。(2)、在探究氢氧化钠的性质时,某化学小组设计了如图所示实验。
(1)、请写出用装置A制取氧气的化学方程式。(2)、某气体只能用E装置收集,写出该气体一定具有的性质。(3)、用F装置可以收集氢气,H2从b管通入,请将装置补画完整。25. 酸、碱、盐是一类重要的化合物。(1)、酸、碱、盐之间发生复分解反应的条件是。(2)、在探究氢氧化钠的性质时,某化学小组设计了如图所示实验。
①当把分液漏斗中的氢氧化钠溶液滴入装有CO2的密闭瓶中后,可观察到的现象是 , 则证明CO2与氢氧化钠溶液发生了反应,写出该反应的化学方程式。
②反应后溶液中的溶质可能只含有碳酸钠。也可能还含有氢氧化钠,请设计实验检验溶质的成分,简要写出实验步骤现象和结论。(提示:碳酸钠溶液呈碱性)
(3)、除去NaCl溶液中CaCl2、MgCl2、Na2SO4杂质的操作顺序为:i.加过量的NaOH溶液;ii.加过量的BaCl2溶液;iii.加过量的Na2CO3溶液;ⅳ.过滤;v.加适量的稀盐液。①为什么加过量的NaOH溶液后。镁离子被彻底除去而钙离子不能被彻底除去。
②加入适量稀盐酸的目的是。
③最终得到的氯化钠固体质量比粗盐中含有的氯化钠质量大,原因是。
(4)、取20g部分变质的氢氧化钠样品,加水配制成溶液,然后向其中加入足量的氯化钡溶液,生成沉淀的质为19.7g。计算该样品中所含杂质的质量分数。