重庆市南川区2022年中考一模化学试题
试卷更新日期:2022-05-05 类型:中考模拟
一、单选题
-
1. 下列物质不属于纯净物的是( )A、金刚石 B、冰水混合物 C、钢 D、碳酸钙2. 关于化学反应中能量变化的叙述正确的是( )A、化学反应过程中常伴随有能量的变化 B、在化学反应中只有燃烧反应才能放出热量 C、凡是要加热才能进行的反应都是吸热反应 D、人类利用的能量都是通过化学反应获得的3. 化学反应前后肯定没有发生变化的是()
①原子数目;②分子数目;③元素种类;④物质种类;⑤原子种类;⑥物质的总质量。
A、①④⑥ B、①③⑤⑥ C、①②⑥ D、②③⑤4. 人们常把金、银、铜、铁、锡等五种金属统称为“五金”。下列相关叙述错误的是( )A、“金银铜铁锡”是按照金属活泼性由弱到强的顺序排列的 B、五种金属中,只有两种金属能和酸发生置换反应生成氢气 C、五种金属中,金的化学性质最不活泼 D、焊锡是锡铅合金,其熔点比锡的熔点低5. 下列物质的性质中,属于化学性质的是( )A、碳酸钙难溶于水 B、白磷在空气中能自燃 C、胆矾晶体(CuSO4·5H2O)呈蓝色 D、浓盐酸的挥发性6. 同学们参加考试时,必须使用2B铅笔填涂答题卡,2B铅笔芯的主要成分是( )A、铅 B、二氧化锰 C、黑色油墨 D、石墨7. 根据化学知识和生活常识判断,铁钉在下列哪种情况下最不容易生锈( )A、干燥的空气中 B、潮湿的空气中 C、全部浸没在植物油中 D、部分浸入食盐水中8. 青少年每天要补充适量的蛋白质促进生长发育。以下食物富含蛋白质的是( )A、牛奶 B、面包 C、白菜 D、西瓜9. 我国已承诺在2060年前实现碳中和。“碳中和”是指通过植树造林、节能减排等手段使二氧化碳净增量为零。下列说法错误的是( )A、二氧化碳的大量排放会加剧温室效应 B、生态园林建设有利于吸收二氧化碳 C、推广和使用脱硫煤可有效减少CO2的排放 D、采用新技术将含碳温室气体转换为含碳固体,有利于实现“碳中和”10. 芯片是信息产业的基础与核心。研究高性能“中国芯”是我国的当务之急。芯片核心材料是高纯度的单质硅,工业上制取硅的化学方程式为:。下列说法正确的是( )A、硅是地壳中含量最多的非金属元素 B、该反应的基本类型为复分解反应 C、反应中硅元素和碳元素的化合价都发生了变化 D、该反应体现了碳单质的氧化性11. 下图表示水在密闭容器里的冷却过程中温度随时间而变化的关系。a、b、c表示水在不同时刻的存在状态,下列有关判断错误的是( )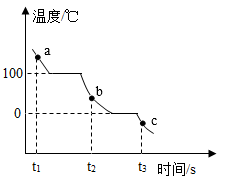 A、b→c过程中发生了结冰现象 B、水分子的运动速率:b>c C、水分子间的间隔:a>b D、a→b→c水分子的体积逐渐变小12. 下列装置是实验室用高锰酸钾制取氧气的部分操作,其中操作不符合题意且会造成器材受损的是( )A、制备
A、b→c过程中发生了结冰现象 B、水分子的运动速率:b>c C、水分子间的间隔:a>b D、a→b→c水分子的体积逐渐变小12. 下列装置是实验室用高锰酸钾制取氧气的部分操作,其中操作不符合题意且会造成器材受损的是( )A、制备 B、收集
B、收集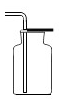 C、装药品
C、装药品 D、验满
D、验满 13. “土豆农膜”是一种新型环保农膜,通过在塑料中添加土豆淀粉制成。“土豆农膜”可被细菌和微生物释放的酶分解。下列有关说法正确的是( )A、土豆农膜被酶分解没有发生化学变化 B、土豆农膜比普通塑料农膜容易降解 C、淀粉不属于高分子化合物 D、塑料属于天然高分子材料14. 我们南川城区和多数乡镇的自来水主要取之于水库,下图是自来水厂净化水的步骤,相关说法错误的是( )
13. “土豆农膜”是一种新型环保农膜,通过在塑料中添加土豆淀粉制成。“土豆农膜”可被细菌和微生物释放的酶分解。下列有关说法正确的是( )A、土豆农膜被酶分解没有发生化学变化 B、土豆农膜比普通塑料农膜容易降解 C、淀粉不属于高分子化合物 D、塑料属于天然高分子材料14. 我们南川城区和多数乡镇的自来水主要取之于水库,下图是自来水厂净化水的步骤,相关说法错误的是( ) A、步骤a、b结合能除去水中的泥沙等悬浮物 B、步骤c中加氯会发生化学反应 C、经过步骤a、b、c不会将硬水转化成软水 D、最终得到的净水是纯净物,可直接饮用15. 某石灰工厂由于操作失误,制取的生石灰(主要成分是CaO)含有一定量未分解的碳酸钙。为掌握生石灰的具体含量,化验室技术员进行了抽样分析得知样品中Ca元素与C元素的质量比是5:1(忽略其它杂质的影响),则此生石灰中碳酸钙和氧化钙的质量比是( )A、15:16 B、25:7 C、15:14 D、25:1416. 以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(“浓度”指溶质的质量分数)
A、步骤a、b结合能除去水中的泥沙等悬浮物 B、步骤c中加氯会发生化学反应 C、经过步骤a、b、c不会将硬水转化成软水 D、最终得到的净水是纯净物,可直接饮用15. 某石灰工厂由于操作失误,制取的生石灰(主要成分是CaO)含有一定量未分解的碳酸钙。为掌握生石灰的具体含量,化验室技术员进行了抽样分析得知样品中Ca元素与C元素的质量比是5:1(忽略其它杂质的影响),则此生石灰中碳酸钙和氧化钙的质量比是( )A、15:16 B、25:7 C、15:14 D、25:1416. 以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(“浓度”指溶质的质量分数)实验序号
H2O2溶液浓度
H2O2溶液质量
温度
MnO2质量
①
5%
12g
20℃
0.2g
②
30%
12g
20℃
0.2g
③
30%
12g
40℃
无
④
30%
12g
90℃
无
若要研究温度对化学反应快慢的影响,应选哪两组实验数据进行对照( )
A、①和② B、②和③ C、③和④ D、②和④二、填空题
-
17. 建立“宏观—微观—符号”之间的联系是化学学科的重要特点。用化学用语填空。(1)、2个硫离子。(2)、硝酸钾、氯化铵、硫酸铵中属于复合肥的是。(3)、某原子的结构示意图为
 , 已知该原子在化学反应中失去2个电子形成相对稳定结构,该原子为。 18. 甲、乙、丙三种固体物质的溶解度曲线如下图所示。回答下列问题:
, 已知该原子在化学反应中失去2个电子形成相对稳定结构,该原子为。 18. 甲、乙、丙三种固体物质的溶解度曲线如下图所示。回答下列问题: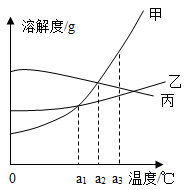 (1)、a3℃时,三种物质的溶解度由大到小的顺序是;(2)、三种物质中的溶解度随温度变化趋势与气体溶解度的变化相似(填“甲”或“乙”或“丙”)。(3)、在a3℃时将等质量的甲、乙两物质饱和溶液分别降温至a1℃,析出固体的质量甲乙(填“>”或“<”或“=”);(4)、在a2℃时,将16g乙固体加入50g水中,充分搅拌后,仍有2.5g乙固体未溶解,则a2℃时乙的溶解度为;该温度下将16g丙固体加入50g水中得到丙的不饱和溶液,若将此不饱和溶液变成饱和溶液,可采用的方法是:(任写一种即可)。19. 化学与我们的生活息息相关,化学源于生活,服务于生活。请你运用生活经验及所学化学知识填空:(1)、糖类、脂肪和蛋白质都是人类的基本营养物质,它们所属的类别是(填“有机物”或“无机物”)。(2)、维生素C又名抗坏血酸,在酸性环境下稳定,高温下不稳定。它主要存在于水果和蔬菜中,能增强人体对疾病的抵抗能力。根据信息可知,维生素C溶液显(填“酸性”、“中性”或“碱性”)。(3)、袋装膨化食品中常通入一种气体以防止该食品被压碎,已知该气体是组成空气的主要成分之一,该气体是。(4)、长期饮用硬水不利于我们的身体健康,在生活中我们可以用来区分硬水和软水。
(1)、a3℃时,三种物质的溶解度由大到小的顺序是;(2)、三种物质中的溶解度随温度变化趋势与气体溶解度的变化相似(填“甲”或“乙”或“丙”)。(3)、在a3℃时将等质量的甲、乙两物质饱和溶液分别降温至a1℃,析出固体的质量甲乙(填“>”或“<”或“=”);(4)、在a2℃时,将16g乙固体加入50g水中,充分搅拌后,仍有2.5g乙固体未溶解,则a2℃时乙的溶解度为;该温度下将16g丙固体加入50g水中得到丙的不饱和溶液,若将此不饱和溶液变成饱和溶液,可采用的方法是:(任写一种即可)。19. 化学与我们的生活息息相关,化学源于生活,服务于生活。请你运用生活经验及所学化学知识填空:(1)、糖类、脂肪和蛋白质都是人类的基本营养物质,它们所属的类别是(填“有机物”或“无机物”)。(2)、维生素C又名抗坏血酸,在酸性环境下稳定,高温下不稳定。它主要存在于水果和蔬菜中,能增强人体对疾病的抵抗能力。根据信息可知,维生素C溶液显(填“酸性”、“中性”或“碱性”)。(3)、袋装膨化食品中常通入一种气体以防止该食品被压碎,已知该气体是组成空气的主要成分之一,该气体是。(4)、长期饮用硬水不利于我们的身体健康,在生活中我们可以用来区分硬水和软水。三、综合题
-
20. 小明同学在化学实验室废液桶中收集了溶有大量FeSO4、CuSO4的废液,他想从中回收金属铜和硫酸亚铁,设计了下图实验方案。请你结合实验方案回答下列问题:
 (1)、金属X与含有FeSO4、CuSO4的废液发生的化学方程式是。操作a的名称是。(2)、加入过量溶液Y的目的是。(3)、理论上所得硫酸亚铁的质量(填“大于”、“小于”或“等于”)原废液中硫酸亚铁的质量。21. 今年3月以来,重庆市部分地区爆发了一波新冠疫情,为了预防新冠病毒,我区各学校常用消毒剂对校园进行消毒。某校化学兴趣小组调查发现,学校常用84消毒液和过氧化氢溶液作为消毒剂,于是兴趣小组同学们决定对这两种消毒剂的组成和性质进行探究。(1)、【实验1】取少量3%的过氧化氢溶液于试管中,加热,发现有气泡产生,同学们觉得应该是氧气,用排水法收集了一瓶该气体,同学们(填写实验操作和现象),证明产生的气体是氧气。(2)、【实验2】取少量84消毒液于试管中,滴加过氧化氢溶液,发现有大量气泡产生。
(1)、金属X与含有FeSO4、CuSO4的废液发生的化学方程式是。操作a的名称是。(2)、加入过量溶液Y的目的是。(3)、理论上所得硫酸亚铁的质量(填“大于”、“小于”或“等于”)原废液中硫酸亚铁的质量。21. 今年3月以来,重庆市部分地区爆发了一波新冠疫情,为了预防新冠病毒,我区各学校常用消毒剂对校园进行消毒。某校化学兴趣小组调查发现,学校常用84消毒液和过氧化氢溶液作为消毒剂,于是兴趣小组同学们决定对这两种消毒剂的组成和性质进行探究。(1)、【实验1】取少量3%的过氧化氢溶液于试管中,加热,发现有气泡产生,同学们觉得应该是氧气,用排水法收集了一瓶该气体,同学们(填写实验操作和现象),证明产生的气体是氧气。(2)、【实验2】取少量84消毒液于试管中,滴加过氧化氢溶液,发现有大量气泡产生。【查阅资料】84消毒液的有效成分是次氯酸钠(化学式为NaClO)。
【提出问题】在上述反应中,NaClO的作用是什么?
【作出猜想】猜想一:作反应物,NaClO与过氧化氢溶液发生化学反应。
猜想二:作 , 类似分解过氧化氢溶液制氧气时MnO2的作用。
(3)、【实验探究】按如图所示组装实验装置,并检验装置气密性后进行实验。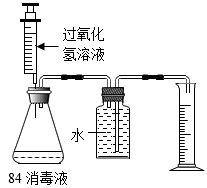
①向锥形瓶中加入25mL84消毒液,注射器中吸入25mL过氧化氢溶液。
②将注射器中的过氧化氢溶液平均分5次推入锥形瓶中:每次推入过氧化氢溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响)见下表。
次数
第1次
第2次
第3次
第4次
第5次
收集气体的总体积/mL
80
160
210
X
220
①分析表中的数据:第三次加入过氧化氢溶液产生的气体体积是 , 继续分析得出X=。
②综合上述分析,于是得出结论:。(填:“猜想一正确”或“猜想二正确”)
22. 下列各图是实验室常用的组装仪器或实验操作示意图,根据初中化学所学实验知识,回答下列问题: (1)、在实验室里,用A、B装置能制取同一种气体,该气体是 , 其中用A装置制取该气体时发生反应的化学反应方程式是:。(2)、装置D中用手握住的仪器的名称是 , 进行此操作的目的是。(3)、某同学用量筒量取某种液体,读数时将量筒平放在桌面,如D图所示,液体的体积为mL。23. 为探究稀盐酸的化学性质,同学们进行如图所示实验,请根据实验回答下列问题:(1)、为验证酸的某些性质,向编号为Ⅰ、Ⅱ、Ⅲ的三支试管中事先加入一定量稀盐酸,然后分别加入石蕊试液、Ca(OH)2溶液、CuO粉末(图甲),其中没有明显现象的是(填试管编号)。试管Ⅲ中发生的化学反应方程式是。(2)、向滴有酚酞试液的石灰水溶液中逐滴滴加稀盐酸至过量(如图乙所示),观察到的现象是 , 发生化学反应的类型是。(3)、向(2)所得到的溶液中逐渐滴加Na2CO3溶液并用pH计同步测量溶液的pH值,溶液pH的变化如图丙所示。同学们发现,最终所得溶液的pH大于7,于是查阅资料并通过实验证明Na2CO3溶液呈碱性。则加入Na2CO3溶液的体积0-V1mL时段,与加入Na2CO3反应的主要物质应是(填化学式),加入Na2CO3溶液的体积V1mL-V2mL时段,发生的主要反应的化学方程式是。(注:NaCl、CaCl2溶液呈中性)
(1)、在实验室里,用A、B装置能制取同一种气体,该气体是 , 其中用A装置制取该气体时发生反应的化学反应方程式是:。(2)、装置D中用手握住的仪器的名称是 , 进行此操作的目的是。(3)、某同学用量筒量取某种液体,读数时将量筒平放在桌面,如D图所示,液体的体积为mL。23. 为探究稀盐酸的化学性质,同学们进行如图所示实验,请根据实验回答下列问题:(1)、为验证酸的某些性质,向编号为Ⅰ、Ⅱ、Ⅲ的三支试管中事先加入一定量稀盐酸,然后分别加入石蕊试液、Ca(OH)2溶液、CuO粉末(图甲),其中没有明显现象的是(填试管编号)。试管Ⅲ中发生的化学反应方程式是。(2)、向滴有酚酞试液的石灰水溶液中逐滴滴加稀盐酸至过量(如图乙所示),观察到的现象是 , 发生化学反应的类型是。(3)、向(2)所得到的溶液中逐渐滴加Na2CO3溶液并用pH计同步测量溶液的pH值,溶液pH的变化如图丙所示。同学们发现,最终所得溶液的pH大于7,于是查阅资料并通过实验证明Na2CO3溶液呈碱性。则加入Na2CO3溶液的体积0-V1mL时段,与加入Na2CO3反应的主要物质应是(填化学式),加入Na2CO3溶液的体积V1mL-V2mL时段,发生的主要反应的化学方程式是。(注:NaCl、CaCl2溶液呈中性)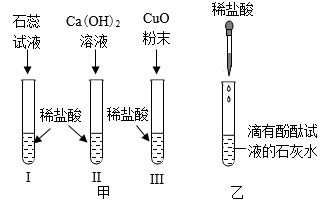

四、计算题
-
24. 鸡蛋壳的主要成分是碳酸钙,其它成分不溶于水,也不与酸反应。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,称取鸡蛋壳12.3g,捣碎,放在烧杯中,然后向其中加入80g某浓度的稀盐酸,使之充分反应,测得烧杯中的反应剩余物质量m与反应时间t的关系如图所示,其中,当反应进行到B点时,盐酸刚好消耗了加入量的一半。试计算:
 (1)、产生的CO2气体质量是。(2)、鸡蛋壳中碳酸钙的质量分数为。(保留一位小数)。(3)、求该稀盐酸的溶质质量分数(写出计算过程,结果保留一位小数)。
(1)、产生的CO2气体质量是。(2)、鸡蛋壳中碳酸钙的质量分数为。(保留一位小数)。(3)、求该稀盐酸的溶质质量分数(写出计算过程,结果保留一位小数)。