四川省广安市华蓥市2022年九年级学业水平模拟(一诊)化学试题
试卷更新日期:2022-04-29 类型:中考模拟
一、单选题
-
1. 生活中充满着变化,下列变化属于化学变化的是( )A、葡萄酿酒 B、玻璃破碎 C、酒精挥发 D、蜡烛熔化2. 下列物质中,前者属于混合物,后者属于纯净物的是( )A、五水硫酸铜 液氧 B、牛奶 冰水混合物 C、干冰 白醋 D、稀有气体 矿泉水3. 重视生态文明建设,加强自然环境保护。下列做法中,不符合这一要求的是( )A、就地焚烧秸秆 B、垃圾分类处理 C、坚持绿色出行 D、废水达标排放4. 下列实验设计不能达到其对应实验目的的是( )A、稀释浓硫酸
 B、制取炭黑
B、制取炭黑 C、检验稀盐酸显酸性
C、检验稀盐酸显酸性 D、检查气密性
D、检查气密性 5. 下列叙述错误的是( )A、点燃可燃性气体前要进行验纯 B、CO具有还原性可用于冶炼金属 C、固体物质的溶解度均随温度的升高而增大 D、用洗涤剂清洗餐具上的油渍利用了乳化原理6. 84消毒液(主要成分是NaClO)在防疫期间被很多学校广泛使用。专家特别提醒,它不能和洁厕灵(主要成分是HCl)混合使用,否则会产生有毒气体,其反应原理是。由此能做出的判断是( )A、有毒气体X为氯气 B、NaClO是一种氧化物 C、该反应为复分解反应 D、反应中氯元素的化合价均发生改变7. 如图所示,向装有水的试管中加入某种固体物质后,U型管左侧液面上升,右侧液面下降。则加入的固体物质可能是()
5. 下列叙述错误的是( )A、点燃可燃性气体前要进行验纯 B、CO具有还原性可用于冶炼金属 C、固体物质的溶解度均随温度的升高而增大 D、用洗涤剂清洗餐具上的油渍利用了乳化原理6. 84消毒液(主要成分是NaClO)在防疫期间被很多学校广泛使用。专家特别提醒,它不能和洁厕灵(主要成分是HCl)混合使用,否则会产生有毒气体,其反应原理是。由此能做出的判断是( )A、有毒气体X为氯气 B、NaClO是一种氧化物 C、该反应为复分解反应 D、反应中氯元素的化合价均发生改变7. 如图所示,向装有水的试管中加入某种固体物质后,U型管左侧液面上升,右侧液面下降。则加入的固体物质可能是() A、食盐 B、蔗糖 C、硝酸铵 D、氢氧化钠8. 下列选项中,物质的俗称、化学式、类别、用途对应均正确的是( )A、生石灰 Ca(OH)2 碱 改良酸性土壤 B、纯碱 Na2CO3 盐 治疗胃酸过多 C、酒精 CH3CH2OH 有机物 作燃料 D、小苏打 NaHCO3 酸 发酵粉的主要成分9. 甲、乙两种固体的溶解度曲线如下图所示。下列说法正确的是( )
A、食盐 B、蔗糖 C、硝酸铵 D、氢氧化钠8. 下列选项中,物质的俗称、化学式、类别、用途对应均正确的是( )A、生石灰 Ca(OH)2 碱 改良酸性土壤 B、纯碱 Na2CO3 盐 治疗胃酸过多 C、酒精 CH3CH2OH 有机物 作燃料 D、小苏打 NaHCO3 酸 发酵粉的主要成分9. 甲、乙两种固体的溶解度曲线如下图所示。下列说法正确的是( ) A、甲的溶解度大于乙的溶解度 B、30℃时,80g甲的饱和溶液稀释到20%需加水40g C、甲的饱和溶液中混有少量的乙,可采用降温结晶的方法提纯甲 D、甲、乙的饱和溶液从30℃降温到20℃,析出固体质量甲大于乙10. 化学符号是学习化学的重要工具。下列对①~④所示化学符号的意义叙述正确的是:①He;②Zn;③Zn2+;④H2O2( )A、①④都表示一个分子 B、②可表示1个锌原子和锌这种物质 C、③中“2+”表示锌元素的化合价 D、④表示H2O2中含有氢分子和氧分子11. 甲、乙、丙三种物质的转化关系如图所示(“→”表示反应一步实现,部分物质和反应条件已略去)。下列各组物质按照甲、乙、丙的顺序不符合要求的是( )
A、甲的溶解度大于乙的溶解度 B、30℃时,80g甲的饱和溶液稀释到20%需加水40g C、甲的饱和溶液中混有少量的乙,可采用降温结晶的方法提纯甲 D、甲、乙的饱和溶液从30℃降温到20℃,析出固体质量甲大于乙10. 化学符号是学习化学的重要工具。下列对①~④所示化学符号的意义叙述正确的是:①He;②Zn;③Zn2+;④H2O2( )A、①④都表示一个分子 B、②可表示1个锌原子和锌这种物质 C、③中“2+”表示锌元素的化合价 D、④表示H2O2中含有氢分子和氧分子11. 甲、乙、丙三种物质的转化关系如图所示(“→”表示反应一步实现,部分物质和反应条件已略去)。下列各组物质按照甲、乙、丙的顺序不符合要求的是( ) A、H2SO4、H2、H2O B、NaOH、NaNO3、NaCl C、Fe、Cu、Ag D、H2O2、O2、H2O12. 下列在酸性溶液或碱性溶液中都能大量共存的一组离子是( )A、 B、 C、 D、
A、H2SO4、H2、H2O B、NaOH、NaNO3、NaCl C、Fe、Cu、Ag D、H2O2、O2、H2O12. 下列在酸性溶液或碱性溶液中都能大量共存的一组离子是( )A、 B、 C、 D、二、填空题
-
13. 用化学用语表示(1)、地壳中含量最多的金属元素;(2)、碳酸根离子;(3)、汞。14. 化学就在我们身边,生活中蕴藏着丰富的化学知识。(1)、均衡膳食,保持良好的饮食习惯,就能满足健康成长的需要,不必刻意用保健品来补充。某天,妈妈准备的午餐如下:米饭、红烧肉、排骨汤、炸鸡腿。从均衡营养的角度看,这份午餐还缺少的营养素是____(填字母)。A、糖类 B、蛋白质 C、油脂 D、维生素(2)、妈妈炒菜的铁锅、烧水的铝查都属于材料。(选填“金属”、“无机非金属”、“有机高分子”、“复合材料”)15. 宏观与微观统一研究物质,是科学研究的基本方法。如图表示治理汽车尾气所涉及反应的微观过程,请根据该微观模型回答下列问题。
 (1)、该反应的化学方程式是。(2)、该反应生成物中的“
(1)、该反应的化学方程式是。(2)、该反应生成物中的“ ”,在物质分类上属于纯净物中的。 16. 空气和水是人类宝贵的自然资源。(1)、氧气可用于抢救危重病人,是因为氧气能。(2)、某同学取自来水于试管中,加入适量肥皂水,振荡后发现产生较多浮渣,说明该自来水属于(填硬水或软水)。生活中可采用的方法来软化。(3)、下列实验能验证水的元素组成的是____(填字母)。A、水的蒸发 B、水的电解 C、水的净化17. 某化学兴趣小组设计的微型实验装置如图所示。则a处观察到的实验现象是;b处澄清石灰水变浑浊,写出该反应的化学方程式:;移开挡板后发现低处蜡烛先熄灭,由此可推出CO2的性质为。
”,在物质分类上属于纯净物中的。 16. 空气和水是人类宝贵的自然资源。(1)、氧气可用于抢救危重病人,是因为氧气能。(2)、某同学取自来水于试管中,加入适量肥皂水,振荡后发现产生较多浮渣,说明该自来水属于(填硬水或软水)。生活中可采用的方法来软化。(3)、下列实验能验证水的元素组成的是____(填字母)。A、水的蒸发 B、水的电解 C、水的净化17. 某化学兴趣小组设计的微型实验装置如图所示。则a处观察到的实验现象是;b处澄清石灰水变浑浊,写出该反应的化学方程式:;移开挡板后发现低处蜡烛先熄灭,由此可推出CO2的性质为。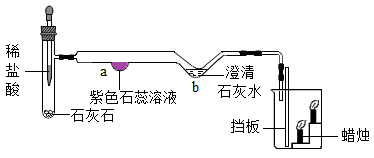 18. 请根据如图回答问题:
18. 请根据如图回答问题: (1)、以上装置A~F中有一处明显的不正确,请加以改正。利用改正后的装置完成后面的实验;(2)、若选用装置B、D、G制取并收集干燥的二氧化碳气体,正确的装置接口顺序为。(3)、实验室用过氧化氢和二氧化锰制取氧气,反应的化学方程式为;若要收集一瓶纯净的氧气,最好选用。(填字母)
(1)、以上装置A~F中有一处明显的不正确,请加以改正。利用改正后的装置完成后面的实验;(2)、若选用装置B、D、G制取并收集干燥的二氧化碳气体,正确的装置接口顺序为。(3)、实验室用过氧化氢和二氧化锰制取氧气,反应的化学方程式为;若要收集一瓶纯净的氧气,最好选用。(填字母)三、综合题
-
19. A、B、C、D四种物质(或其溶液)分别是HCl、NaOH、CuSO4、CuO中的一种,它们之间的关系如图所示(反应条件与其他物质均已略去)。“→”表示可以向箭头所指方向一步转化,“一”表示两端的物质可以发生反应。
 (1)、举出氢氧化钠的一种用途。(2)、B是。(3)、A与D反应的化学方程式为。
(1)、举出氢氧化钠的一种用途。(2)、B是。(3)、A与D反应的化学方程式为。四、计算题
-
20. 为了测定某黄铜(Cu、Zn合金)样品中锌的质量分数,某化学小组进行了如图实验:

请分析并计算:
(1)、反应中生成氢气的质量为g。(2)、该黄铜样品中锌的质量分数。(精确到0.1%)五、科学探究题
-
21. 实验课上,老师向滴有无色酚酞试液的NaOH红色溶液中滴加稀HCl,同学们观察到溶液颜色由红色变为无色,说明酸碱发生了中和反应。(1)、【提出问题】HCl和NaOH是否恰好完全反应了?
【查阅资料】I.常温下,酚酞在pH≤8.2的溶液中呈无色,在pH>8.2的溶液中呈红色。
Ⅱ.相同温度下,NaOH稀溶液中溶质的质量分数越大,溶液pH越大。
【猜想假设】① , 溶液pH>7;
②恰好完全反应,溶液pH=7;
③HCl过量,溶液pH<7。
(2)、【理论论证】分别取少量反应后的无色溶液于3支试管中,按下列方案实验:实验操作
实验现象
实验结论
方案1
滴加几滴碳酸氢钠溶液
无气泡产生
假设不正确(填序号)
方案2
加热蒸发
蒸发过程中,发现溶液由无色变为红色
假设①正确方案3的化学反应方程式
方案3
滴加几滴硫酸铜溶液
有蓝色沉淀生成
(3)、【结论分析】反应后的无色溶液中还有少量NaOH,此时pH的范围;加热蒸发一段时间后,恢复至常温,当溶液的pH>8.2时,变为红色。(4)、【反思总结】向某碱性溶液中滴加2~3滴无色酚酞试液,振荡后,溶液的颜色变为红色。(填“一定”或“不一定”)(5)、【拓展应用】在探究酸碱性质的实验中,可借助pH传感器监测溶液pH的变化情况。常温下,向盐酸中加水稀释,溶液pH变化与下图吻合的是。(填序号)
-
-