山东省济宁市高新区2022年中考一模化学试题
试卷更新日期:2022-04-22 类型:中考模拟
一、单选题
-
1. 下列做法及叙述正确的是( )
A
化学与生活
用甲醛溶液浸泡海产品保鲜
B
化学与农业
铵态氮肥不能与碱性物质混用
C
化学与安全
浓硫酸沾在皮肤上,涂NaOH溶液
D
化学与环保
空气污染指数越高,空气质量越好
A、A B、B C、C D、D2. 推理是化学学习常用的方法。下列说法正确的是( )A、碱中含有氢、氧元素,所以含有氢、氧元素的物质一定是碱 B、红磷燃烧可用于测定空气中氧气的含量,则木炭燃烧也可以 C、溶液是均一、稳定的,但均一、稳定的液体不一定是溶液 D、分子可以构成物质,所以物质一定都是由分子构成的3. La(镧)是一种活动性比锌还强的金属元素,它的氧化物 La2O3 所对应的碱 La(OH)3 难溶于水,而LaCl3、La(NO3)3 都溶于水.下列各组中物质能直接反应制得 LaCl3 的是( )A、La 与盐酸 B、La2O3 与 AgCl C、La(OH)3 与 MgCl2 D、BaCl2 与 La(NO3)34. 批杷中富含的维生素A1具有预防夜盲症、抗衰老和促进股骨髓生长等功效,其化学式为C20H30O。下列说法正确的是( )A、维生素A1是一种氧化物 B、维生素A1中碳元素的质量分数最大 C、维生素A1由20个碳原子、30个氢原子、1个氧原子构成 D、维生素A1中碳元素、氢元素、氧元素的质量比为20:30:15. 如图是3种物质的溶解度曲线。下列叙述正确的是( ) A、0℃时,NaCl的溶解度小干NH4Cl的溶解度 B、40℃时,饱和Na2 CO3溶液的溶质质量分数为49% C、将饱和Na2 CO3溶液由80℃冷却至40℃时,有固体析出 D、80℃时,分别将等质量的NH4Cl和NaCl固体溶于适量的水,恰好均配成饱和溶液,所得溶液的质量前者小于后者6. 芯片是中美经贸摩擦的焦点之一。制造芯片的高纯硅可以用下述方法制取,据图分析判断,下列各项中不正确的是( )
A、0℃时,NaCl的溶解度小干NH4Cl的溶解度 B、40℃时,饱和Na2 CO3溶液的溶质质量分数为49% C、将饱和Na2 CO3溶液由80℃冷却至40℃时,有固体析出 D、80℃时,分别将等质量的NH4Cl和NaCl固体溶于适量的水,恰好均配成饱和溶液,所得溶液的质量前者小于后者6. 芯片是中美经贸摩擦的焦点之一。制造芯片的高纯硅可以用下述方法制取,据图分析判断,下列各项中不正确的是( )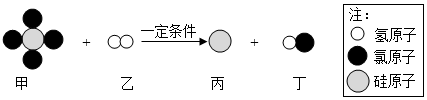 A、该反应属于置换反应 B、反应中乙、丙两物质质量之比为1∶14 C、物质丁是由分子构成的 D、反应前后氢元素的化合价发生了改变7. 某钠盐溶液中含有Cl﹣、OH﹣、CO32﹣三种阴离子,仅用一份样品溶液,利用下面的试剂与操作就可将溶液中的三种阴离子依次检验出来,正确的实验操作顺序是( )
A、该反应属于置换反应 B、反应中乙、丙两物质质量之比为1∶14 C、物质丁是由分子构成的 D、反应前后氢元素的化合价发生了改变7. 某钠盐溶液中含有Cl﹣、OH﹣、CO32﹣三种阴离子,仅用一份样品溶液,利用下面的试剂与操作就可将溶液中的三种阴离子依次检验出来,正确的实验操作顺序是( )①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液.
A、①②④②③ B、④②①②③ C、③②①②④ D、④②③②①8. 下列有关物质的检验、鉴别、分离、除杂所用的试剂或方法正确的是( )选项
实验目的
所用试剂或方法
A
检验一瓶气体是否为CO2
燃着的木条
B
鉴别氢氧化钠溶液和饱和石灰水
升高温度
C
分离铁粉和铜粉混合物
过量稀硫酸、过滤
D
除去NaOH溶液中的Na2CO3
过量氢氧化钙溶液、过滤
A、A B、B C、C D、D9. 一定质量的Zn加入到含有Fe(NO3)2和AgNO3两种物质的混合溶液中,充分反应后过滤液仍为浅绿色,下列叙述正确的是( )①滤液中一定有Zn2+、Fe2+
②滤液中可能有Ag+
③滤渣中一定有Ag,可能有Fe
A、①② B、①③ C、②③ D、①②③10. 有一包白色粉末可能由氯化钠、硫酸钠、硫酸铜、碳酸钠、碳酸钙中的一种或几种组成,为确定其组成,进行如下实验:①称取一定质量的该白色粉末加足量水溶解,得无色溶液A;
②在无色溶液A中加入过量氯化钡溶液,充分反应后过滤,分别得无色溶液B和白色沉淀C;将白色沉淀C洗涤,烘干后称得质量为19g;
③在19g白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出;
④在无色溶液B中滴加硝酸银溶液和稀硝酸,产生白色沉淀;
根据上述实验现象判断,下列说法正确的是( )
A、白色粉末中不含碳酸钙、硫酸钠、硫酸铜 B、白色粉末中一定含有氯化钠 C、无色溶液B中一定含有两种溶质 D、步骤③生成的气体质量可能是4.4g二、填空题
-
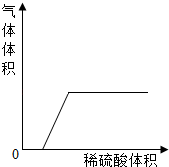
11. 用化学用语填空。(1)、空气中能作为植物光合作用的原料:。(2)、硝酸铵中的阴阳离子:。(3)、次氯酸钾的化学式是KClO,那么次氯酸钙的化学式:。(4)、铁粉加入到稀硫酸中反应后得到的溶液中的溶质是:。12. 从HCl、NaCl、NaOH、Na2CO3、Ca(OH)2几种溶液中,每次取出两种混合。(1)、若混合后溶液质量减小,则全部可能的组合为:。(2)、若混合后溶液质量不变,但发生了化学反应,有关的化学方程式为:、。(3)、若混合后无明显现象,但滴入稀硫酸后,产生的气体与加入稀硫酸的量有如图所示的关系,则这样的组合是。
 13. 健康、环境与资源已成为人们日益关注的问题。(1)、近日,中国石化胜利海上油田首次开采出无色、透明、清澈如水的凝析原油,被称为天然汽油,写出汽油的主要成分之一辛烷(C8H18)完全燃烧的化学方程式。(2)、下列有关物质的性质与用途对应关系正确的是____(填字母)。A、氧气可以支持很多物质燃烧,可作燃料 B、二氧化碳能溶于水且能与水反应,可用来灭火 C、洗洁精能与油污发生化学反应,可用于清洗餐具上的油污 D、酚醛塑料因具有较好的热固性,可制成锅具的手柄(3)、每100g番茄中营养成分的含量如表:
13. 健康、环境与资源已成为人们日益关注的问题。(1)、近日,中国石化胜利海上油田首次开采出无色、透明、清澈如水的凝析原油,被称为天然汽油,写出汽油的主要成分之一辛烷(C8H18)完全燃烧的化学方程式。(2)、下列有关物质的性质与用途对应关系正确的是____(填字母)。A、氧气可以支持很多物质燃烧,可作燃料 B、二氧化碳能溶于水且能与水反应,可用来灭火 C、洗洁精能与油污发生化学反应,可用于清洗餐具上的油污 D、酚醛塑料因具有较好的热固性,可制成锅具的手柄(3)、每100g番茄中营养成分的含量如表:蛋白质/g
脂肪/g
糖类/g
钙/mg
磷/mg
铁/mg
维生素C/mg
0.6
0.3
2
8
37
0.4
11
上述营养成分中,属于必需微量元素的是(填元素符号)。
(4)、抗击“新型冠状病寄”用到的过氧乙酸(C2H4O3)是一种高效消毒剂。将20mL20%的过氧乙酸(密度为1.1g/cm3)稀释为0.5%的过氧乙酸(密度为1.0g/cm3),需加入水的体积为mL。三、综合题
-
14. 氮化硼(BN)陶瓷基复合材料在航天领域应用广泛。硼单质是制备氮化硼(BN)的原料之一,某工厂利用硼砂(主要成分为Na2B4O7·10H2O,杂质中含少量Fe3+)制备硼(B)单质的部分流程如下图所示:
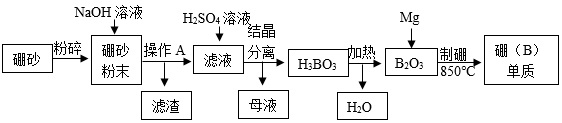
请完成下列问题:
(1)、粉碎硼砂的目的是。(2)、操作A的名称是。(3)、滤渣的成分为(填化学式)。(4)、写出H3BO3加热分解的化学方程式。(5)、“制硼”反应的化学方程式为。15. 实验是化学的根本,请根据如所示实验装置图,回答有关问题: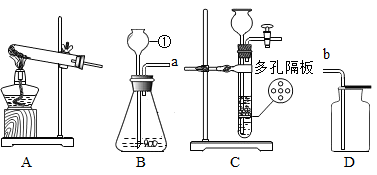
 (1)、写出有标号的仪器名称:。(2)、若用装置A制取相对纯净的氧气,反应的化学方程式为 , 应该选择的收集装置为 , 气体集满的标志是。(3)、B或C装置均可用于实验室制取二氧化碳,C装置相对于B装置的优点是 , 实验室里为了制取纯净、干燥的二氧化碳气体,其装置接口正确的连接顺序为a→→b(填接口对应的字母)。16. 某兴趣小组在实验室里准备常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中,有一瓶未盖瓶塞且标签破损的溶液(如图),他们决定对这瓶溶液的成分进行探究。
(1)、写出有标号的仪器名称:。(2)、若用装置A制取相对纯净的氧气,反应的化学方程式为 , 应该选择的收集装置为 , 气体集满的标志是。(3)、B或C装置均可用于实验室制取二氧化碳,C装置相对于B装置的优点是 , 实验室里为了制取纯净、干燥的二氧化碳气体,其装置接口正确的连接顺序为a→→b(填接口对应的字母)。16. 某兴趣小组在实验室里准备常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中,有一瓶未盖瓶塞且标签破损的溶液(如图),他们决定对这瓶溶液的成分进行探究。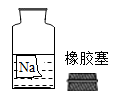
【提出问题】这瓶溶液的溶质是什么?
【获得信息】
酸、碱、盐的性质实验中用到含钠元素的物质有氯化钠、氢氧化钠、碳酸钠、碳酸氢钠。
实验室里盛放碱性溶液的试剂瓶通常使用橡胶塞。
碳酸氢钠溶液与氯化钡溶液不反应;氯化钡溶液呈中性。
【提出猜想】猜想一:氢氧化钠;猜想二:碳酸钠;猜想三:碳酸氢钠。
【实验探究】
(1)、小军取样滴加稀盐酸有气泡产生,得出结论:该溶液的溶质是。(2)、小军另取样加入过量的氯化钡溶液,观察到有产生,进而得出结论:该溶液的溶质是碳酸钠。(3)、小华认为小军的结论不完全正确,理由是。小组同学讨论后一致认为还需要进行如下实验:取小军第二次实验后的上层清液,滴入无色酚酞溶液,溶液呈红色。
(4)、【实验结论】这瓶溶液的原溶质是。
(5)、【探究启示】实验中取用液体药品时,应注意。
四、简答题
-
17. 科学家经过多年研究证明,某些油炸食品中含有致癌物质丙烯酰胺(C3HxON)。请你根据丙烯酰胺(C3HxON)的化学式计算:(1)、丙烯酰胺中碳元素和氮元素的质量比为。(2)、丙烯酰胺(C3HxON)的相对分子质量为71,则x的数值为。
五、计算题
-
18. 洁厕灵的有效成分为HCl,李强同学测定某品牌洁厕灵中HCl的质量分数。他将100.0g洁厕灵倒入锥形瓶中,逐次加入等质量相同质量分数的Na2CO3溶液,测出每次完全反应后溶液的总质量,实验数据记录如下表。
第一次
第二次
第三次
第四次
第五次
加入Na2CO3溶液的质量/g
20.0
20.0
20.0
20.0
20.0
反应后溶液的总质量/g
118.9
137.8
M
175.6
195.6
请根据实验数据分析解答下列问题:
(1)、表格中M的数值为。(2)、恰好完全反应时消耗Na2CO3的质量是多少(3)、该洁厕灵中HCl的质量分数是多少?
-