广西南宁市宾阳县2022年中考一模化学试题
试卷更新日期:2022-04-15 类型:中考模拟
一、单选题
-
1. 人在深呼吸的过程中,吸入的空气中含量最多的气体是( )A、氧气 B、二氧化碳 C、氮气 D、稀有气体2. 下列化肥从外观即可与其它化肥相区别的是( )A、氯化钾 B、硝酸钾 C、硫酸铵 D、磷矿粉3. 下列家庭小实验中,主要发生物理变化的是( )A、蜡烛燃烧生成炭黑 B、用活性炭净水 C、鸡蛋壳放入食醋 D、牛奶制酸奶4. 医院里的下列物质属于纯净物的是( )A、生理盐水 B、止咳糖浆 C、液氧 D、碘酒5. 在城巿建设过程中,经常用到玻璃材料。切割玻璃的玻璃刀头上镶的物质是( )A、石墨 B、硬玻璃 C、不锈钢 D、金刚石6. 正确的实验操作是科学探究成功的基础。下列操作中正确的是( )A、
 滴加少量液体
B、
滴加少量液体
B、 称量氯化钠
C、
称量氯化钠
C、 闻气味
D、
闻气味
D、 稀释浓硫酸
7. 将少量下列生活中常见的物质分别放入水中,不能形成溶液的是( )A、味精 B、苏打粉 C、白糖 D、面粉8. 某无土栽培的营养液中含有磷酸钾(K3PO4)。其中磷元素的化合价为()A、-3 B、+1 C、+3 D、+59. 恰当的安全措施能减少生命财产损失。下列事故处理措施正确的是A、油锅着火,立即盖上锅盖 B、电器着火,立即用水扑灭 C、高层住房内着火,立即打开所有门窗 D、煤气泄露,立即打开排气扇的电源开关10. “建设美丽中国”是新时代的目标。下列做法不符合这一要求的是( )A、不任意排放工业废水 B、推广使用清洁能源 C、农业上合理使用农药化肥 D、焚烧方法处理塑料垃圾11. 关于电解水实验的下列说法中正确的是( )A、从现象上判断:正极产生的是氢气 B、从能量上分析:由化学能转化为电能 C、从宏观上分析:水是由氧气和氢气组成的 D、从微观上分析:水分子是由氢原了和氧原子构成的12. 下列实验现象描述正确的是( )A、硝酸铵晶体溶解于水,形成的溶液温度明显升高 B、镁条在空气中燃烧,发出耀眼的白光,生成白色固体 C、细铁丝在空气中剧烈燃烧,火星四射,生成四氧化三铁 D、硫在氧气中燃烧,产生淡蓝色火焰,生成有刺激性气味的气体13. 下列生活中的做法或说法正确的是( )A、用甲醛溶液浸泡海鲜防腐 B、用食醋除去水壶中的水垢 C、天然泉水不含任何化学物质 D、儿童患佝偻病是因为体内缺乏碘元素14. 氧气是我们身边常见的物质,下列有关氧气的说法中不正确的是( )A、氧气能供给呼吸 B、氧气的化学性质比较活泼 C、液氧可做宇宙火箭的燃料 D、物质与氧气发生的反应都是氧化反应15. 下面图示为某些物品对应的pH范围,其中显弱碱性的是()
稀释浓硫酸
7. 将少量下列生活中常见的物质分别放入水中,不能形成溶液的是( )A、味精 B、苏打粉 C、白糖 D、面粉8. 某无土栽培的营养液中含有磷酸钾(K3PO4)。其中磷元素的化合价为()A、-3 B、+1 C、+3 D、+59. 恰当的安全措施能减少生命财产损失。下列事故处理措施正确的是A、油锅着火,立即盖上锅盖 B、电器着火,立即用水扑灭 C、高层住房内着火,立即打开所有门窗 D、煤气泄露,立即打开排气扇的电源开关10. “建设美丽中国”是新时代的目标。下列做法不符合这一要求的是( )A、不任意排放工业废水 B、推广使用清洁能源 C、农业上合理使用农药化肥 D、焚烧方法处理塑料垃圾11. 关于电解水实验的下列说法中正确的是( )A、从现象上判断:正极产生的是氢气 B、从能量上分析:由化学能转化为电能 C、从宏观上分析:水是由氧气和氢气组成的 D、从微观上分析:水分子是由氢原了和氧原子构成的12. 下列实验现象描述正确的是( )A、硝酸铵晶体溶解于水,形成的溶液温度明显升高 B、镁条在空气中燃烧,发出耀眼的白光,生成白色固体 C、细铁丝在空气中剧烈燃烧,火星四射,生成四氧化三铁 D、硫在氧气中燃烧,产生淡蓝色火焰,生成有刺激性气味的气体13. 下列生活中的做法或说法正确的是( )A、用甲醛溶液浸泡海鲜防腐 B、用食醋除去水壶中的水垢 C、天然泉水不含任何化学物质 D、儿童患佝偻病是因为体内缺乏碘元素14. 氧气是我们身边常见的物质,下列有关氧气的说法中不正确的是( )A、氧气能供给呼吸 B、氧气的化学性质比较活泼 C、液氧可做宇宙火箭的燃料 D、物质与氧气发生的反应都是氧化反应15. 下面图示为某些物品对应的pH范围,其中显弱碱性的是() A、小苏打 B、杨梅 C、栗子 D、菠萝16. 推理是学习化学的一种重要方法。下列推理合理的是( )A、离子是带电荷的粒子,所以带电荷的粒子一定是离子 B、溶液具有均一性、稳定性,所以具有均一、稳定的液体都属于溶液 C、一氧化碳和二氧化碳的分子构成不同,所以它们的化学性质也不相同 D、原子和分子都是微观粒子,化学变化中原子不能再分,所以分子也不能再分17. 甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下:
A、小苏打 B、杨梅 C、栗子 D、菠萝16. 推理是学习化学的一种重要方法。下列推理合理的是( )A、离子是带电荷的粒子,所以带电荷的粒子一定是离子 B、溶液具有均一性、稳定性,所以具有均一、稳定的液体都属于溶液 C、一氧化碳和二氧化碳的分子构成不同,所以它们的化学性质也不相同 D、原子和分子都是微观粒子,化学变化中原子不能再分,所以分子也不能再分17. 甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下: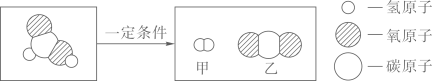
下列说法正确的是( )
A、甲酸分子中氢、氧原子个数比为1:2 B、乙中碳、氧元素质量比为1:2 C、46g甲酸中氢元素质量为2g D、生成甲与乙的分子个数比为2:118. 下列图像不能符合题意反映对应变化关系的是( )实验设计




实验目的
A.红磷燃烧测定空气中氧气的含量
B.探究石蜡燃烧后有二氧化碳生成
C.验证氢气的密度比空气小
D.向一定量的二氧化锰中加入过氧化氢溶液
A、A B、B C、C D、D19. 下列四组物质的溶液,不用其它试剂(可组内两两混合)就能鉴别出来的是( )A、NaNO3、NaCl、AgNO3、稀HCl B、稀HNO3、Na2CO3、NaCl、Na2SO4 C、BaCl2、K2SO4、NaOH、MgCl2 D、BaCl2、K2SO4、Na2CO3、HNO320. 有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。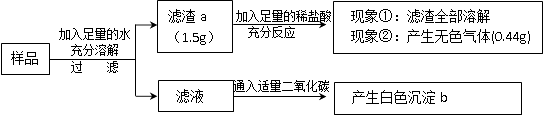
下列说法不正确的是( )
A、滤渣a的成分是碳酸钙和氢氧化镁 B、滤液中溶质的成分除氯化钠还有氢氧化钠、硫酸钠 C、白色沉淀b的成分是碳酸钡 D、若现象①“滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则不能确定原样品中一定存在氯化镁二、填空题
-
21. 请用适合的化学符号填空:(1)、钾元素。(2)、2个硫原子。(3)、硝酸的阴离子。(4)、相对分子质量最小的氧化物。(5)、标出氧化铜中铜元素的化合价。22. 化学与生产、生活息息相关,请你用化学知识回答以下生活中的问题:(1)、铁制品在潮湿的空气中生锈的原因是。(2)、生活中常用的方法降低水的硬度,同时又可以杀菌消毒。(3)、用洗洁精除去餐具上的油污,是由于洗洁精对油污有作用。(4)、红烧牛肉是小燕最爱吃的一道菜,其中牛肉富含的营养素是。(5)、区别棉纤维、羊毛纤维和合成纤维的最简单方法是。23. 元素周期律是学习和研究化学的重要工具。下图甲、乙是氧元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
 (1)、氧元素的相对原子质量为 , 钙元素的原子序数(即质子数)为。(2)、若D为原子,则D中的x= , D与B结合形成化合物的化学式为。(3)、和A粒子具有相似的化学性质的粒子是(填序号)。24. 将80g物质M加入50g水中,充分溶解,测得溶液的质量随温度的变化曲线如图所示。
(1)、氧元素的相对原子质量为 , 钙元素的原子序数(即质子数)为。(2)、若D为原子,则D中的x= , D与B结合形成化合物的化学式为。(3)、和A粒子具有相似的化学性质的粒子是(填序号)。24. 将80g物质M加入50g水中,充分溶解,测得溶液的质量随温度的变化曲线如图所示。 (1)、20℃时,物质M的溶解度为g。(2)、比较A,B,C点溶液的溶质质量分数大小 , 其中A溶液的溶质质量分数为。(3)、由图可知,物质M的溶解度随温度升高而(填“增大”或“减小”)。(4)、恒温蒸发物质M的溶液,现象如下图所示,烧杯(填序号)中的溶液一定是不饱和溶液。
(1)、20℃时,物质M的溶解度为g。(2)、比较A,B,C点溶液的溶质质量分数大小 , 其中A溶液的溶质质量分数为。(3)、由图可知,物质M的溶解度随温度升高而(填“增大”或“减小”)。(4)、恒温蒸发物质M的溶液,现象如下图所示,烧杯(填序号)中的溶液一定是不饱和溶液。 25. 金属及金属材料在生产、生活中有广泛的应用。(1)、图1为学校配备的非接触红外测温仪,能及时对人体体温进行检测,图2为红外测温仪电池的剖面图。按要求回答下列问题:
25. 金属及金属材料在生产、生活中有广泛的应用。(1)、图1为学校配备的非接触红外测温仪,能及时对人体体温进行检测,图2为红外测温仪电池的剖面图。按要求回答下列问题:
①其中属于有机合成材料的是。
②回收废弃电池过程中,如要在铜和锌的混合物回收铜,可以在混合物中加入适量的 , 充分反应后,再进行过滤、干燥(填操作)。
③写出NH4Cl的一种用途。
(2)、口罩上的鼻梁条一般由铝合金制成,下列说法正确的是____(填字母)。A、氧化铝是铝合金 B、铝合金属于金属材料 C、铝合金用于制作鼻梁条利用了其密度小、质软、抗腐蚀好等特点。(3)、向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,反应过程中,测得混合物中溶液的质量与加入铁粉的质量关系如图所示。有关该反应过程中的下列说法正确的是____ A、a点,向溶液中滴加稀盐酸,无白色沉淀 B、d点,溶液中的溶质为Fe(NO3)2和Cu(NO3)2 C、e点,过滤后得到的固体中只含有2种物质 D、c点,向过滤后得到的固体中滴加稀盐酸,无气泡产生
A、a点,向溶液中滴加稀盐酸,无白色沉淀 B、d点,溶液中的溶质为Fe(NO3)2和Cu(NO3)2 C、e点,过滤后得到的固体中只含有2种物质 D、c点,向过滤后得到的固体中滴加稀盐酸,无气泡产生三、综合题
-
26. 2022年冬季,奥运五环再次飘扬在北京市上空。小燕同学仿照奥运五环设计了如下图所示的化学五连环。“五环”中相交两环中的物质间能够发生化学反应。其中A、B、C、D分别是NaOH、Fe、CuO、CuCl2中的一种。
 (1)、C的名称是。(2)、“五环”中的物质Fe可以替换成(填一种即可)。(3)、写出A与B反应的化学方程式:;B与C的反应属于(填基本反应类型)(4)、C与H2SO4反应的微观实质是。27. 某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag)探究相关物质的性质并回收镍,设计流程如图(部分产物已略去)。
(1)、C的名称是。(2)、“五环”中的物质Fe可以替换成(填一种即可)。(3)、写出A与B反应的化学方程式:;B与C的反应属于(填基本反应类型)(4)、C与H2SO4反应的微观实质是。27. 某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag)探究相关物质的性质并回收镍,设计流程如图(部分产物已略去)。
查阅资料:a.H2O2溶液可将Fe2+转化为Fe3+
b.Fe3+、Ni2+转化为对应的氢氧化物沉淀时,溶液pH如图:
 (1)、步骤1的操作为 , 滤渣①的成分为。(2)、镍与稀硫酸反应的化学方程式为。(3)、滤液②中有Ni2+、无Fe3+ , 则滤液②pH可能为____(填序号)。A、pH=1 B、pH=2 C、pH=6 D、pH=10(4)、Ni、Fe、Ag三种金属的活动性由强到弱的顺序是。28. 请根据下列实验装置图回答有关问题:
(1)、步骤1的操作为 , 滤渣①的成分为。(2)、镍与稀硫酸反应的化学方程式为。(3)、滤液②中有Ni2+、无Fe3+ , 则滤液②pH可能为____(填序号)。A、pH=1 B、pH=2 C、pH=6 D、pH=10(4)、Ni、Fe、Ag三种金属的活动性由强到弱的顺序是。28. 请根据下列实验装置图回答有关问题: (1)、写出②仪器的名称。(2)、写出利用A装置制取氧气的化学方程式。选择发生装置B和收集装置。(选填序号)可用于实验室制取的CO2:若将发生装置由B改为F,其优点是。(3)、某化学兴趣小组借助氧气传感器探究微粒的运动,数据处理软件可实时绘出氧气体积分数随时间变化的曲线。收集塑料瓶氧气进行以下三步实验:①敞口放置:②双手贴在塑料瓶外壁上:③将塑料瓶的瓶口朝下,三步实验中测得氧气的体积分数随时间变化的曲线依次为图2中的MN段、NP段PQ段。
(1)、写出②仪器的名称。(2)、写出利用A装置制取氧气的化学方程式。选择发生装置B和收集装置。(选填序号)可用于实验室制取的CO2:若将发生装置由B改为F,其优点是。(3)、某化学兴趣小组借助氧气传感器探究微粒的运动,数据处理软件可实时绘出氧气体积分数随时间变化的曲线。收集塑料瓶氧气进行以下三步实验:①敞口放置:②双手贴在塑料瓶外壁上:③将塑料瓶的瓶口朝下,三步实验中测得氧气的体积分数随时间变化的曲线依次为图2中的MN段、NP段PQ段。
①从实验步骤中能体现氧气的密度比空气大的曲线是。
A.MN段 B.NP段 C.PQ段
②MN段和NP段相比较,说明。
③随着实验的进行,传感器测出氧气的体积分数约为时几乎不再变化。
29. 小燕对实验室里久置于空气中变质的过氧化钠(Na2O2)固体的成分进行研究。【查阅资料】
①过氧化钠化学性质很活泼,能与水、二氧化碳反应。
其中机关反应: 。
②Ba(NO3)2溶液、NaNO3溶液均为中性溶液
(1)、【猜想与假设】猜想I:固体为Na2O2、NaOH、Na2CO3
猜想Ⅱ:固体为NaOH、Na2CO3
猜想Ⅲ:固体为NaOH
猜想Ⅳ:固体为。
(2)、【实验推断】实验操作
实验现象
实验结论
①取少量固体于试管中,加水振荡直至完全溶解
猜想1不成立
②取少量①的溶液于试管中,滴加过量的Ba(NO3)2溶液
证明有Na2CO3存在。该反应的化学方程式为
③取少量②的溶液于试管中,滴加无色酚酞试液
证明有NaOH存在
综合以上实验现象,说明猜想Ⅱ是成立的
(3)、【反思评价】Na2O2在变质成Na2CO3过程中除了资料中显示的两个反应外,还可能发生了其他反应,请写出该反应的化学方程式:。
四、计算题
-
30. 化学兴趣小组为测定某铜锌合金中成分金属的含量,称取10g样品放入烧杯中,向其中加入100g稀硫酸,恰好完全反应后。测得烧杯内所有物质的总质量为109.8g。
请完成下列分析及计算
(1)、反应中共生成气体g。(2)、计算合金中铜的质量分数。