湖南省株洲市茶陵县2021年中考模拟化学试题
试卷更新日期:2022-04-01 类型:中考模拟
一、单选题
-
1. 下列活动中涉及到化学变化的是( )A、手工刺绣 B、甘蔗榨汁 C、露天烧烤 D、冰冻凉粉2. 材料与人类生活密切相关,下列物品的主要成分是合成材料的是( )A、纯棉内衣 B、铝合金门窗 C、塑料篮子 D、玻璃水杯3. 下列实验操作正确的是( )A、
 读出液体的体积
B、
读出液体的体积
B、 过滤
C、
过滤
C、 熄灭酒精灯
D、
熄灭酒精灯
D、 稀释浓硫酸
4. 交警检查司机是否酒后驾车,常根据所用检测仪中的重铬酸钾(K2Cr2O7)与乙醇反应前后颜色变化来判断。重铬酸钾中Cr元素的化合价为( )A、+3 B、+4 C、+5 D、+65. 下列有关实验现象的描述正确的是( )A、红磷在空气中燃烧,产生大量烟雾 B、细铁丝在氧气中燃烧,生成四氧化三铁 C、打开浓盐酸的瓶盖,看到大量白雾 D、木炭在氧气中燃烧,发出耀眼的白光,产生黑色固体6. 稀土有“工业的维生素”的美誉。钇是一种重要的稀土元素,下列说法中不正确的是( )
稀释浓硫酸
4. 交警检查司机是否酒后驾车,常根据所用检测仪中的重铬酸钾(K2Cr2O7)与乙醇反应前后颜色变化来判断。重铬酸钾中Cr元素的化合价为( )A、+3 B、+4 C、+5 D、+65. 下列有关实验现象的描述正确的是( )A、红磷在空气中燃烧,产生大量烟雾 B、细铁丝在氧气中燃烧,生成四氧化三铁 C、打开浓盐酸的瓶盖,看到大量白雾 D、木炭在氧气中燃烧,发出耀眼的白光,产生黑色固体6. 稀土有“工业的维生素”的美誉。钇是一种重要的稀土元素,下列说法中不正确的是( ) A、钇原子的核外电子数为39 B、钇原子的中子数是39 C、钇的相对原子质量是88.91 D、钇属于金属元素7. 下列物质的名称、化学式、俗称均一致的是( )A、汞 Ag 水银 B、氧化钙 CaO 熟石灰 C、碳酸钠 Na2CO3 苏打 D、乙醇 CH3COOH 酒精8. 下列物质属于碱的是( )A、HNO3 B、NH4HCO3 C、NH3•H2O D、NO29. 乳酸具有帮助消化、增进食欲的功能。“某品牌”酸奶中含有乳酸,其化学式为C3H6O3.下列关于乳酸的说法不正确的是( )A、乳酸是一种有机物 B、乳酸由3个碳原子、6个氢原子和3个氧原子构成 C、乳酸由碳、氢、氧三种元素组成 D、乳酸中质量分数最大的是氧元素10. 下列物质置于空气中,一段时间后,发生化学变化使质量增大的是( )A、碳酸钙 B、氢氧化钠 C、浓盐酸 D、浓硫酸11. 将甲、 乙两 种金属片分别放入硫酸铜溶液中,甲表面析出金属铜,乙没有明显现象。据此判断,三种金属的金属活动性顺序是 ( )A、甲>铜>乙 B、乙>铜>甲 C、铜>甲>乙 D、甲>乙>铜12.
A、钇原子的核外电子数为39 B、钇原子的中子数是39 C、钇的相对原子质量是88.91 D、钇属于金属元素7. 下列物质的名称、化学式、俗称均一致的是( )A、汞 Ag 水银 B、氧化钙 CaO 熟石灰 C、碳酸钠 Na2CO3 苏打 D、乙醇 CH3COOH 酒精8. 下列物质属于碱的是( )A、HNO3 B、NH4HCO3 C、NH3•H2O D、NO29. 乳酸具有帮助消化、增进食欲的功能。“某品牌”酸奶中含有乳酸,其化学式为C3H6O3.下列关于乳酸的说法不正确的是( )A、乳酸是一种有机物 B、乳酸由3个碳原子、6个氢原子和3个氧原子构成 C、乳酸由碳、氢、氧三种元素组成 D、乳酸中质量分数最大的是氧元素10. 下列物质置于空气中,一段时间后,发生化学变化使质量增大的是( )A、碳酸钙 B、氢氧化钠 C、浓盐酸 D、浓硫酸11. 将甲、 乙两 种金属片分别放入硫酸铜溶液中,甲表面析出金属铜,乙没有明显现象。据此判断,三种金属的金属活动性顺序是 ( )A、甲>铜>乙 B、乙>铜>甲 C、铜>甲>乙 D、甲>乙>铜12.下图是X、Y、Z、W四种溶液的近似pH。下列判断不正确的是( )
 A、X一定显酸性 B、Y一定是水 C、Z一定显碱性 D、W的碱性一定比Z强13. 下列化学方程式正确且书写正确的是()
A、X一定显酸性 B、Y一定是水 C、Z一定显碱性 D、W的碱性一定比Z强13. 下列化学方程式正确且书写正确的是()
A、用硫酸除铁锈:FeO+H2SO4=FeSO4+H2O B、正常雨水的pH约为5.6的原因:CO2 + H2O=H2CO3 C、医疗上用碱性物质中和过多胃酸:NaOH+HCl=NaCl+H2O D、除去铜粉中少量的铁粉:2Fe+6HCl=2FeCl3+3H2↑14. 利用催化剂可消除室内装修材料释放的甲醛,如下图所示为该反应的微观示意图,下列说法不正确的( ) A、甲醛的化学式为CH2O B、反应后氧元素的化合价发生改变 C、该反应为置换反应 D、化学反应前后原子种类和数目不变15. 下列各项转化,按已有知识,不能一步实现的是( )A、KNO3→KCl B、Ca(OH)2→NaOH C、CuO→CuCl2 D、H2SO4→FeSO416. 已知,常温下氯化钠、氯化钡的水溶液呈中性,向含有盐酸和氯化钡的混合溶液中逐滴滴入过量的X,溶液pH与滴入X的量的关系如图所示,则X可能是下列物质中的( )
A、甲醛的化学式为CH2O B、反应后氧元素的化合价发生改变 C、该反应为置换反应 D、化学反应前后原子种类和数目不变15. 下列各项转化,按已有知识,不能一步实现的是( )A、KNO3→KCl B、Ca(OH)2→NaOH C、CuO→CuCl2 D、H2SO4→FeSO416. 已知,常温下氯化钠、氯化钡的水溶液呈中性,向含有盐酸和氯化钡的混合溶液中逐滴滴入过量的X,溶液pH与滴入X的量的关系如图所示,则X可能是下列物质中的( ) A、NaOH溶液 B、H2O C、AgNO3溶液 D、Na2CO3溶液17. 下列各组离子在pH=10的溶液中能大量共存的是( )A、K +、、Cl-、 B、H+、K+、Cl-、 C、Cu2+、Ba2+、Cl-、 D、K+、Na+、Cl-、18. 除去下列物质中的少量杂质,所选试剂及操作都正确的是( )
A、NaOH溶液 B、H2O C、AgNO3溶液 D、Na2CO3溶液17. 下列各组离子在pH=10的溶液中能大量共存的是( )A、K +、、Cl-、 B、H+、K+、Cl-、 C、Cu2+、Ba2+、Cl-、 D、K+、Na+、Cl-、18. 除去下列物质中的少量杂质,所选试剂及操作都正确的是( )序号
物质
杂质
试剂
操作
A
CO
CO2
足量NaOH溶液
洗气
B
O2
水蒸气
足量稀硫酸
洗气
C
NaOH溶液
Na2CO3
适量CaCl2溶液
过滤
D
Fe粉
CuO
过量盐酸
过滤
A、A B、B C、C D、D19. 逻辑推理是化学学习中常用的思维方法。下列推理正确的是( )A、中和反应生成盐和水,则生成盐和水的反应一定是中和反应 B、化合物是由不同种元素组成的纯净物。所以由不同种元素组成的纯净物一定是化合物 C、有机物是含碳元素的化合物,所以含碳元素的化合物一定是有机物 D、活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属20. 将a、b、c、d四种物质放入一个密闭容器中,在一定条件下反应段时间后,测得各物质的质量如表所示,则下列说法中不正确的是( )物质
a
b
c
d
反应前质量/g
6.4
3.2
4.0
0.5
反应后质量/g
待测
2.4
7.2
0.5
A、待测值为4 B、a与b的相对分子质量比为3:1 C、该反应属于化合反应 D、d可能是催化剂,也可能是杂质二、填空题
-
21. 用适当的数字和符号填空:(1)、4个氨分子;(2)、烧碱溶液中的阴离子;(3)、标出硫化亚铁中硫元素的化合价。22. 通过一年的化学学习,我们认识了“酸”和“碱”,请回答下列问题:(1)、碱有氢氧化钠、氢氧化钙等,这两种碱敞口放置在空气中都会变质。氢氧化钡溶液敞口放置在空气中也会变质,其反应的化学方程式为。(2)、热水瓶胆壁上的水垢的主要成分是碳酸钙和氢氧化镁,可用醋酸溶解除去。已知醋酸与氢氧化镁反应的化学方程式为:2CH3COOH+ Mg(OH)2 = (CH3COO)2Mg+2H2O,则醋酸与碳酸钙反应的化学方程式是。23. 根据以下四种粒子的结构示意图回答问题。
 (1)、写出①的符号: , ④的名称: 。(2)、属于同种元素的是:。(填序号)(3)、写出①、②元素形成的化合物的化学式:。24. 如图是甲、乙两种物质的溶解度曲线,请回答下列问题。
(1)、写出①的符号: , ④的名称: 。(2)、属于同种元素的是:。(填序号)(3)、写出①、②元素形成的化合物的化学式:。24. 如图是甲、乙两种物质的溶解度曲线,请回答下列问题。 (1)、将接近饱和的乙溶液变成饱和溶液的方法是。(2)、t2℃时,将50g甲物质加入50g水中,充分搅拌后形成的溶液的溶质质量分数是。(3)、t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,此时甲溶液的溶质质量分数乙溶液的溶质质量分数。(填“< ”或“=”或“>”)25. 下表为几种家用清洁剂的功能及有效成分:
(1)、将接近饱和的乙溶液变成饱和溶液的方法是。(2)、t2℃时,将50g甲物质加入50g水中,充分搅拌后形成的溶液的溶质质量分数是。(3)、t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,此时甲溶液的溶质质量分数乙溶液的溶质质量分数。(填“< ”或“=”或“>”)25. 下表为几种家用清洁剂的功能及有效成分:名 称
洁厕灵
活氧彩漂
漂白精
功 能
有效清除污垢与异味
漂洗使衣物色彩鲜艳
快速漂除衣物污渍
有效成分
HCl
H2O2
NaClO
(1)、往活氧彩漂中加入少量二氧化锰,观察到的现象是。(2)、“洁厕灵”与“漂白精”不能混用,二者混合易产生一种有毒气体X。反应原理为:NaClO + 2HCl = NaCl + X↑ + H2O ,则X的化学式为。26.(1)、洗涤剂和汽油都能清除油污,其原理相同吗?并说明理由。(2)、用微粒的观点解释温度计中汞柱热胀冷缩现象。三、综合题
-
27. 下列图中字母A﹣I分别表示初中化学常见的物质.其中C是能使澄清石灰水变浑浊的气体,B是一种黑色固体.“→”表示物质间存在转化关系,部分反应条件和部分生成物已略去.请回答:
 (1)、写出下列物质的化学式A.;(2)、操作1的名称为;(3)、写出反应①的化学方程式;(4)、写出G+F→I的化学方程式 .28. 2019年诺贝尔化学奖授予对锂离子电池研究作出贡献的三位科学家。下图是从钴酸锂废极片(主要成分为钴酸锂(LiCoO2)中回收得到Co2O3和Li2CO3的一种工艺流程。
(1)、写出下列物质的化学式A.;(2)、操作1的名称为;(3)、写出反应①的化学方程式;(4)、写出G+F→I的化学方程式 .28. 2019年诺贝尔化学奖授予对锂离子电池研究作出贡献的三位科学家。下图是从钴酸锂废极片(主要成分为钴酸锂(LiCoO2)中回收得到Co2O3和Li2CO3的一种工艺流程。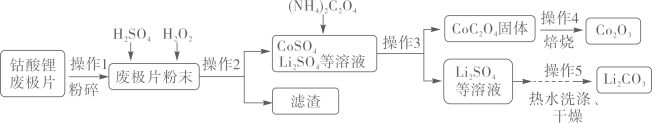 (1)、操作1中,粉碎废极片的目的是;(2)、实验室中完成操作2时,需用到的玻璃仪器是(填一种即可);(3)、操作4中,在高温条件下,CoC2O4在空气中反应生成Co2O3和二氧化碳,化学方程式为;(4)、操作5中,Li2CO3晶体用热水洗涤比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高面。29. 实验室部分装置如图所示,回答下列问题:
(1)、操作1中,粉碎废极片的目的是;(2)、实验室中完成操作2时,需用到的玻璃仪器是(填一种即可);(3)、操作4中,在高温条件下,CoC2O4在空气中反应生成Co2O3和二氧化碳,化学方程式为;(4)、操作5中,Li2CO3晶体用热水洗涤比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高面。29. 实验室部分装置如图所示,回答下列问题:
 (1)、仪器X的名称是;实验室用装置B制O2的化学方程式为;(2)、实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷(CH4)气体,其发生装置为;(3)、某同学欲用活泼金属单质和稀盐酸反应制取纯净、干燥的H2 , 请从这些装置中选择并连接成一套组合装置,按照气流从左到右的流向,写出所选装置接口的连接顺序:b→。30. 我国大部分地区深受酸雨的危害,煤燃烧产生的SO2是形成酸雨的主要污染物,SO2与水结合生成弱酸性亚硫酸(H2SO3)。H2SO3易分解生成水和SO2 , 也易与空气中的氧气或稀硝酸反应生成H2SO4 。(1)、酸雨是pH小于的降雨。(2)、常用脱硫方法减少废气中的SO2 , 以生石灰(CaO)为脱硫剂,高温下与废气中的SO2与O2化合生成CaSO4 , 化学方程式为:。(3)、小鸿同学利用中和反应的原理,向空气中放置一段时间的酸雨(pH约为3)中加入足量的KOH,并就反应后混合溶液中的盐成分进行探究:
(1)、仪器X的名称是;实验室用装置B制O2的化学方程式为;(2)、实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷(CH4)气体,其发生装置为;(3)、某同学欲用活泼金属单质和稀盐酸反应制取纯净、干燥的H2 , 请从这些装置中选择并连接成一套组合装置,按照气流从左到右的流向,写出所选装置接口的连接顺序:b→。30. 我国大部分地区深受酸雨的危害,煤燃烧产生的SO2是形成酸雨的主要污染物,SO2与水结合生成弱酸性亚硫酸(H2SO3)。H2SO3易分解生成水和SO2 , 也易与空气中的氧气或稀硝酸反应生成H2SO4 。(1)、酸雨是pH小于的降雨。(2)、常用脱硫方法减少废气中的SO2 , 以生石灰(CaO)为脱硫剂,高温下与废气中的SO2与O2化合生成CaSO4 , 化学方程式为:。(3)、小鸿同学利用中和反应的原理,向空气中放置一段时间的酸雨(pH约为3)中加入足量的KOH,并就反应后混合溶液中的盐成分进行探究:【提出猜想】反应后的混合溶液中盐的成分是什么?
【查阅资料】
①H2SO3和SO2都能使红色的品红溶液褪色。
②亚硫酸盐能与盐酸发生类似于碳酸盐与盐酸的反应,并生成有刺激性的气体;
③、均能与Ba2+反应产生白色沉淀,BaSO3能溶于稀盐酸,不溶于稀硝酸。
【进行猜想】猜想1:只有K2SO3;
猜想2:;
猜想3:既有K2SO4 , 也有K2SO3。
(4)、【实验探究】步骤
实验操作
预期现象与结论
1
各取2 mL反应后的混合溶液分别加入A、B两支试管

2
向A试管中滴加足量的稀盐酸,再滴入几滴红色品红溶液
先观察到 , 再 , 证明含有K2SO3
3
向B试管中加入再加入足量的稀盐酸
先产生白色沉淀,后 , 证明猜想3成立
(5)、【反思交流】①写出亚硫酸钡与盐酸反应的化学方程式:。
②亚硫酸要密封保存,因为。(用化学方程式解释)
四、计算题
