湖南省娄底市娄星区2021年中考二模化学试题
试卷更新日期:2022-04-01 类型:中考模拟
一、单选题
-
1. 下列生活生产实践中,主要原理为化学变化的是( )A、分离液态空气制取氧气 B、云中撒播干冰人工降雨 C、熟石灰改良酸性土壤 D、冬天捞碱,夏天晒盐2. 下图中的符号表示2个氢气分子的是( )A、
 B、
B、 C、
C、 D、
D、 3. 下列图示的实验操作不正确的是( )A、给液体加热
3. 下列图示的实验操作不正确的是( )A、给液体加热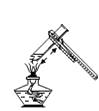 B、测溶液的pH
B、测溶液的pH 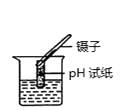 C、稀释浓硫酸
C、稀释浓硫酸 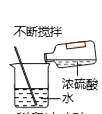 D、蒸发食盐水
D、蒸发食盐水  4. 聚合氯化铝[Al2(OH)mCln]是一种新型净水剂,经分析其中氢元素:氯元素质量比=2:71,则( )A、m=1 B、n=2 C、m=3 D、n=45. 归纳总结是学习化学的重要方法之一。下列选项正确的是( )A、金属的熔点: B、地壳中的元素含量: C、空气中气体的体积分数: D、金属的活动性顺序:6. 化学让我们的生活更美好,科学家为此作出了很大的努力,其中在制碱工业作出巨大贡献的是( )A、拉瓦锡 B、门捷列夫 C、汤姆生 D、侯德榜7. 甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示:
4. 聚合氯化铝[Al2(OH)mCln]是一种新型净水剂,经分析其中氢元素:氯元素质量比=2:71,则( )A、m=1 B、n=2 C、m=3 D、n=45. 归纳总结是学习化学的重要方法之一。下列选项正确的是( )A、金属的熔点: B、地壳中的元素含量: C、空气中气体的体积分数: D、金属的活动性顺序:6. 化学让我们的生活更美好,科学家为此作出了很大的努力,其中在制碱工业作出巨大贡献的是( )A、拉瓦锡 B、门捷列夫 C、汤姆生 D、侯德榜7. 甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示:
根据以上微观示意图得出的结论中,正确的是( )
A、反应前后分子的数目没有改变 B、水煤气的成分是一氧化碳和氧气 C、该反应中含氢元素的化合物有3种 D、该反应的化学方程式中甲烷和氢气的计量数之比为1꞉38. 判断推理是学习化学常用的思维方式,下列判断正确的是( )A、某固体物质加入稀盐酸能产生气体,则该固体可能是较为活泼的金属 B、给水通直流电可以产生氢气和氧气,则水是由氢气和氧气组成的 C、同种元素的原子质子数相同,则质子数相同的微粒属于同种元素 D、碱溶液的pH大于7,则pH大于7的溶液一定是碱溶液9. 一定条件下,甲、乙、丙、丁四种物质在密闭容器中发生反应,测得反应前后各物质的质量如下表所示。下列说法正确的是()物质
甲
乙
丙
丁
反应前质量/g
26
8
2
4
反应后质量/g
1
X
16
15
A、上表中X的值是0 B、该反应的基本反应类型是化合反应 C、乙一定是该反应的催化剂 D、丙和丁变化的质量比为14:1110. 下列图像不能正确反应其对应变化关系的是( ) A、图A是高温煅烧一定质量的石灰石 B、图B是将等质量的镁条和锌片分别加入相同体积、相同溶质质量分数的足量稀硫酸中 C、图C是向一定质量的稀盐酸中逐滴加入氢氧化钠溶液 D、图D是实验室电解水11. 化学与生活密切相关,下列说法不正确的是( )A、缺锌会引起甲状腺肿大,服用葡萄糖酸锌口服液能补锌 B、用肥皂水检验硬水和软水,硬水泡沫少,软水泡沫多 C、鉴别硫酸铵和氯化钾化肥,分别取少量,加熟石灰粉末研磨,闻气味 D、如果遇到火灾,要用湿毛巾捂住口鼻,蹲下靠近地面或沿墙壁跑离着火区域12. 为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计实验如下表所示。
A、图A是高温煅烧一定质量的石灰石 B、图B是将等质量的镁条和锌片分别加入相同体积、相同溶质质量分数的足量稀硫酸中 C、图C是向一定质量的稀盐酸中逐滴加入氢氧化钠溶液 D、图D是实验室电解水11. 化学与生活密切相关,下列说法不正确的是( )A、缺锌会引起甲状腺肿大,服用葡萄糖酸锌口服液能补锌 B、用肥皂水检验硬水和软水,硬水泡沫少,软水泡沫多 C、鉴别硫酸铵和氯化钾化肥,分别取少量,加熟石灰粉末研磨,闻气味 D、如果遇到火灾,要用湿毛巾捂住口鼻,蹲下靠近地面或沿墙壁跑离着火区域12. 为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计实验如下表所示。实验分组
锌的质量g
盐酸
环境温度/℃
体积/mL
浓度/%
①
0.5
5
5
25
②
0.5
5
10
25
③
0.5
5
5
50
下列说法正确的是( )
A、对比实验①和②,可研究盐酸的浓度对反应剧烈程度的影响 B、对比实验②和③,可研究盐酸的浓度对反应剧烈程度的影响 C、对比实验②和③,可研究温度对反应剧烈程度的影响 D、对比实验①和②,可研究温度对反应剧烈程度的影响13. 蓝莓中含有的花青素(化学式为 C15H11O6)具有缓解眼睛疲劳、保护视力的作用。酸能使花青素溶液变成红色,碱能使花青素溶液变成蓝色。下列说法不正确的是( )A、花青素中氢元素的质量分数最小 B、一个花青素分子中共有32个原子 C、向pH =11的草木灰水中滴加花青素溶液,溶液变成红色 D、花青素分子中碳、氢、氧原子个数比为 15∶11∶614. 能在pH=3的溶液中大量共存,且溶液无色透明的一组离子是( )A、K+、Na+、Cl-、NO3- B、Mg2+、OH-、SO42-、Cl- C、Na+、NH4+、NO3-、CO32- D、Ca2+、Cu2+、Cl、NO3-15. 提纯是化学实验常用的一种方法。除去下表混合物中的杂质,所选除杂试剂不正确的是( )选项
混合物(括号内为杂质)
除杂试剂
A
NaOH溶液(Na2CO3)
适量的氢氧化钙溶液
B
CaO粉末(CaCO3)
足量的蒸馏水
C
Cu粉(Fe)
足量的稀硫酸
D
HCl溶液(H2SO4)
适量的氯化钡溶液
A、A B、B C、C D、D二、填空题
-
16. 化学知识在生活、生产中有着广泛的应用,回答下列有关问题。(1)、某村民种植的玉米出现了大面积植株矮小、根系不发达的情况,应适当补充磷肥,下列物质中属于磷肥的是____。A、NH4NO3 B、K2SO4 C、KNO3 D、Ca(H2PO4)2(2)、水是生命之源,也是人类最宝贵的资源。习总书记在党的十八大报告中曾指出:“绿水青山就是金山银山”。我国淡水资源并不丰富,节约用水是爱护水资源的一个重要方面,请你写出生活中节约用水的具体措施(任写一条)。17.(1)、火灾的警示:文物保护意识应警钟长鸣,并构建安全保护机制。内容之一是在可燃建筑材料中加入阻燃剂,而Mg(OH)2是一种常见的阻燃剂,在380℃时分解成水蒸气和耐高温的MgO,吸收大量的热。
①写出Mg(OH)2阻燃时发生反应的化学方程式:。
②写出Mg(OH)2阻燃的一个原因:。
(2)、 除了四种基本反应类型外,人们还将有元素化合价发生变化的反应称为氧化还原反应 , 而元素化合价不发生变化的反应称为非氧化还原反应。例如:是氧化还原反应。①上述反应中化合价发生变化的元素为(写元素符号)
②四种基本反应类型中,一定是氧化还原反应的是 , 一定是非氧化还原反应的是。
18. 溴原子结构示意图如图所示,请回答下列问题: (1)、图中x的值为。(2)、溴元素的化学性质与如图中(填字母标号)的化学性质相似。
(1)、图中x的值为。(2)、溴元素的化学性质与如图中(填字母标号)的化学性质相似。 (3)、第117号元素在元素周期表中的部分信息如图所示,它与溴元素属同族元素,化学性质与溴元素相似,则第117号元素原子最外层有个电子。
(3)、第117号元素在元素周期表中的部分信息如图所示,它与溴元素属同族元素,化学性质与溴元素相似,则第117号元素原子最外层有个电子。 19. 硫酸锂(Li2SO4)和硝酸钾在不同温度时的溶解度如表:
19. 硫酸锂(Li2SO4)和硝酸钾在不同温度时的溶解度如表:温度/℃
0
10
20
30
40
溶解度/g
Li2SO4
36.1
35.4
34.8
34.3
33.9
KNO3
13.3
20.9
31.6
45.8
63.9
请回答下列问题
(1)、依据溶解度表,绘制溶解度曲线如图所示,其中能表示Li2SO4溶解度曲线的是。(填“甲”或“乙”) (2)、Li2SO4和KNO3在某一温度时具有相同的溶解度x,则x的范围是。(3)、40℃时,有含少量Li2SO4的KNO3饱和溶液,欲从中提纯KNO3晶体,方法是。
(2)、Li2SO4和KNO3在某一温度时具有相同的溶解度x,则x的范围是。(3)、40℃时,有含少量Li2SO4的KNO3饱和溶液,欲从中提纯KNO3晶体,方法是。三、科普阅读题
-
20. 阅读下面的科普短文。
硒(Se)是人体内重要的微量元素之一,在抗氧化、延缓机体衰老等方面发挥重要作用。含硒丰富的食物有水产品、动物内脏、蘑菇、富硒大米、白菜心等。摄入硒过少可能会导致克山病的发生,而过高会引起中毒,导致腹泻、失明、脱发、甚至死亡。人体中硒主要通过土壤﹣植物﹣机体食物链摄入。我国土壤中硒含量严重不均衡,因此国内对富硒食品进行了许多开发与研究。施用含硒肥料,可提高植物中硒的含量。食物中硒主要以硒酸钠(Na2SeO4)、亚硒酸钠(Na2SeO3)、植物活性硒形式存在。硒含量的检测可采取荧光光谱法,在相同条件下,将待测液荧光强度与标准曲线(图2)对比,即可快速获取结果。将10g某富硒大米、河虾样品分别制成1L待测液,进行5次实验,测得数据如图3。依据文章内容回答下列问题。

 (1)、富硒食品中“硒”指的是(填“元素”或“单质”)。(2)、亚硒酸钠(Na2SeO3)由种元素组成。(3)、下列说法中正确的是(填字母序号)。
(1)、富硒食品中“硒”指的是(填“元素”或“单质”)。(2)、亚硒酸钠(Na2SeO3)由种元素组成。(3)、下列说法中正确的是(填字母序号)。A每日摄入“硒”越多,越有利身体健康
B施用含硒肥料,可使植物中硒含量增加
C实验测定的富硒大米硒含量比河虾的高
四、综合题
-
21. 硫铁矿[主要成分是二硫化亚铁(FeS2)],其他成分不含铁,硫元素是一种重要的化工原料,常用来制备硫酸和氯化铁,工业生产流程如图所示。
 (1)、过滤中玻璃棒的作用 。(2)、步骤二中主要反应的化学方程式为 。(3)、溶液乙中一定有的阳离子。(4)、上述流程中所涉及的含硫的物质中,硫元素的化合价共有种。22. 如图是实验室制取气体的常用装置,请回答下列问题。
(1)、过滤中玻璃棒的作用 。(2)、步骤二中主要反应的化学方程式为 。(3)、溶液乙中一定有的阳离子。(4)、上述流程中所涉及的含硫的物质中,硫元素的化合价共有种。22. 如图是实验室制取气体的常用装置,请回答下列问题。 (1)、写出仪器①的名称:。(2)、用装置A制备O2 , 则A中发生反应的化学方程式为。用装置E收集一瓶O2 , 测得O2纯度偏低,原因可能是(填字母序号)。
(1)、写出仪器①的名称:。(2)、用装置A制备O2 , 则A中发生反应的化学方程式为。用装置E收集一瓶O2 , 测得O2纯度偏低,原因可能是(填字母序号)。a收集气体前,集气瓶中没有注满水 b导管口开始有气泡冒出,立刻收集
c收集气体后,集气瓶中仍有少量水 d收集气体后,集气瓶正放在桌面上
(3)、用装置D收集CO2 , 气体应从(填“m”或“n”)端进入。用装置C作发生装置,关闭弹簧夹,反应停止后,液面应位于(填“1”、“2”或“3”)处。(4)、根据C装置的优点,用此类装置还可进行的实验是(填字母)。A过氧化氢溶液制取氧气
B氯酸钾制取氧气
C锌粒与稀硫酸制取氢气
23. 某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验:将足量的氢氧化钠浓溶液装入分液漏斗中,先打开阀门K1 , 待氢氧化钠溶液完全进入广口瓶之后立即关闭K1 , 充分反应后, 打开止水夹K2 , 请填写现象: (1)、U 形管左侧的液体;广口瓶中的液体出现浑浊。广口瓶中生成沉淀的化学方程式为。同学们将实验后的废液倒入烧杯中,过滤得到白色沉淀和红色滤液,欲对滤液中溶质的成分进行探究,其 成分除了酚酞外的猜想有如下三种:
(1)、U 形管左侧的液体;广口瓶中的液体出现浑浊。广口瓶中生成沉淀的化学方程式为。同学们将实验后的废液倒入烧杯中,过滤得到白色沉淀和红色滤液,欲对滤液中溶质的成分进行探究,其 成分除了酚酞外的猜想有如下三种:猜想一:Na2CO3、NaOH;
猜想二:;
猜想三:NaOH。
(2)、设计如下实验方案,请你帮助他们完成探究报告:实验步骤
实验现象
实验结论
①取滤液样品于试管中,加入;
若有气泡冒出,且红色消失
猜想一正确
②另取滤液样品于试管中,加入。
若有白色沉淀出现,红色不消失
猜想二正确
【反思拓展】实验步骤①中所加的试剂可换成以下 , 也能通过观察现象得出同样的结论。
A CaCl2溶液
B Ba(OH)2溶液
C NaCl 溶液
五、计算题
-
24. 小苏打(主要成分为 NaHCO3)中常含有少量氯化钠。化学兴趣小组的同学为了测定某品牌小苏打中 NaHCO3的质量分数。取该固体样品20g,向其中逐滴加入稀盐酸,当加入稀盐酸的质量为50g、75g、100g、125g时,生成气体的质量见下表(气体的溶解度忽略不计)。
第一组
第二组
第三组
第四组
稀盐酸的质量g
50
75
100
125
生成气体的质量g
4.4
m
8.8
8.8
试分析计算:
(1)、第二组数据m为g。(2)、样品中碳酸氢钠的质量分数是多少?(3)、恰好完全反应时得到不饱和氯化钠溶液,求不饱和溶液中氯化钠的质量分数?(计算结果精确至0.1%)
-