湖南省娄底市涟源市2021年中考三模化学试题
试卷更新日期:2022-04-01 类型:中考模拟
一、单选题
-
1. “新冠肺炎”严重患者会出现肺部纤维化,呼吸功能受阻,此时可用于医疗急救的气体是( )A、N2 B、O2 C、CO2 D、稀有气体2. 下列事实与“花香四溢”的微观解释相同的是( )A、尘土飞扬 B、水通电分解 C、汽油挥发 D、细胞的运动3. 下列物质的用途中,利用其物理性质的是( )A、石墨可用于制作电极 B、熟石灰可用于改良酸性土壤 C、二氧化碳用作温室里的气体肥料 D、焦炭用于冶炼金属4. 下列操作不正确的是( )A、稀释浓硫酸
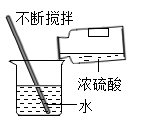 B、点燃酒精灯
B、点燃酒精灯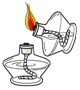 C、加热液体
C、加热液体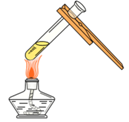 D、取用固体粉末
D、取用固体粉末 5. 下列不属于铁丝在氧气中燃烧现象的是( )A、放出热量 B、产生大量白烟 C、火星四射 D、生成黑色固体6. 模型认知是科学研究的一种方法。1911年,物理学家卢瑟福完成著名的a粒子轰击金箔实验,提出了有核原子模型。下列各项中,不属于卢瑟福原子结构理论观点的是( )A、原子就像充斥着正电荷的“葡萄干布丁” B、原子的质量几乎全部集中在原子核上 C、原子核带正电荷 D、电子在原子核外“很大”空间中运动7. 我国北斗三号全球卫星导航系统正式开通,北斗卫星天线金属丝的主要成分有高纯度钼,下图是钼元素在元素周期表中的信息及钼原子结构示意图,下列说法正确的是( )
5. 下列不属于铁丝在氧气中燃烧现象的是( )A、放出热量 B、产生大量白烟 C、火星四射 D、生成黑色固体6. 模型认知是科学研究的一种方法。1911年,物理学家卢瑟福完成著名的a粒子轰击金箔实验,提出了有核原子模型。下列各项中,不属于卢瑟福原子结构理论观点的是( )A、原子就像充斥着正电荷的“葡萄干布丁” B、原子的质量几乎全部集中在原子核上 C、原子核带正电荷 D、电子在原子核外“很大”空间中运动7. 我国北斗三号全球卫星导航系统正式开通,北斗卫星天线金属丝的主要成分有高纯度钼,下图是钼元素在元素周期表中的信息及钼原子结构示意图,下列说法正确的是( ) A、钼原子的中子数为42 B、钼元素的相对原子质量是95.94g C、钼原子核外电子排布图中x为18 D、钼原子在化学变化中易失去电子8. 化学让我们鉴赏了溶液的颜色美,下列物质加入水中能形成有色溶液的是( )A、碳酸钙 B、硫酸铜 C、植物油 D、氯化钠9. 今年我国将发射火星探测器。以下是关于火星的部分已知信息:
A、钼原子的中子数为42 B、钼元素的相对原子质量是95.94g C、钼原子核外电子排布图中x为18 D、钼原子在化学变化中易失去电子8. 化学让我们鉴赏了溶液的颜色美,下列物质加入水中能形成有色溶液的是( )A、碳酸钙 B、硫酸铜 C、植物油 D、氯化钠9. 今年我国将发射火星探测器。以下是关于火星的部分已知信息:①其橘红色外表是因为地表被赤铁矿覆盖;
②火星上无液态水,但有大量冰;
③火星大气的成分为二氧化碳95.3%、氮气 2.7%、氩气 1.6%、氧气和水汽 0.4%。
下列说法正确的是( )
A、赤铁矿的主要成分是四氧化三铁 B、火星上的冰转化为液态水要放出热量 C、未来在火星上可用 CO 获取铁单质 D、蜡烛在火星大气中可以燃烧10. 下列有关化学用语表示正确的是( )A、五氧化二磷:P2O5 B、银元素:AG C、2个镁离子:2Mg+2 D、8个硫原子:S811. 课外实验具有趣味性、实践性等特点。对维生素C溶液的性质探究过程如下(已知:维生素C能使蓝色的淀粉碘酒溶液褪色)。其中不正确的选项是( ) A、实验①中维生素C溶液呈酸性 B、实验②FeCl3可与维生素C反应 C、实验③加热不会破坏维生素C D、每步实验操作都是正确的12. 2020年,脱贫攻坚决战决胜之年,某中学科普小组走进乡村,为农民伯伯宣讲《魅力化学》。下列对“肥料”的宣讲,不正确的是( )A、化学肥料要合理使用 B、KNO3是一种常见的复合肥料 C、硝酸铵可与草木灰(呈碱性)混合使用 D、通过闻气味的方法可以区分 NH4HCO3和K2SO413. 将200g溶有物质M的溶液从95℃降低到10℃,不同温度时析出溶质M的质量如下表所示。下列说法正确的是( )
A、实验①中维生素C溶液呈酸性 B、实验②FeCl3可与维生素C反应 C、实验③加热不会破坏维生素C D、每步实验操作都是正确的12. 2020年,脱贫攻坚决战决胜之年,某中学科普小组走进乡村,为农民伯伯宣讲《魅力化学》。下列对“肥料”的宣讲,不正确的是( )A、化学肥料要合理使用 B、KNO3是一种常见的复合肥料 C、硝酸铵可与草木灰(呈碱性)混合使用 D、通过闻气味的方法可以区分 NH4HCO3和K2SO413. 将200g溶有物质M的溶液从95℃降低到10℃,不同温度时析出溶质M的质量如下表所示。下列说法正确的是( )温度/℃
95
90
80
30
10
析出M的质量/g
0
0
15
100
116
A、95℃时该溶液为饱和溶液 B、M的溶解度随温度的升高而减小 C、30℃时析出M后所得溶液中含100g水 D、从M的不饱和溶液中析出M可采用先蒸发溶剂、再冷却结晶的方法14. 小明同学在做酸碱中和实验时,取少量NaOH溶液于试管中,立即滴加无色酚酞[酚酞的变色范围:pH在8.2~10.0之间],看到了溶液变成了红色,正准备向试管中再滴加稀盐酸时,发现试管中红色渐渐褪成了无色,对产生此现象原因的猜想不合理的是( )A、无色酚酞常温下不稳定,易分解 B、试管内壁上有酸性物质附着 C、NaOH溶液已变质 D、NaOH溶液的浓度过大15. 下列除杂方法正确的是( )选项
物质
试剂
操作
A
MnO2(KCl)
H2O
溶解、过滤、洗涤、干燥
B
KNO3(NaCl)
AgNO3溶液
溶解、过滤
C
NaOH溶液(Na2CO3)
稀盐酸
加入试剂至不再产生气泡
D
CO2(CO)
O2
点燃
A、A B、B C、C D、D二、填空题
-
16. 我们美丽的生活中蕴含着许多化学知识。请按要求回答下列问题:(1)、夏天鱼塘含氧量减少,是因为气体的溶解度与有关。(2)、用洗洁精清洗餐具,植物油分散成细小的液滴,便于洗涤。这种现象称为。(3)、生活中将硬水转化为软水的方法是。(4)、包饺子的食材有面粉、韭菜、瘦肉、植物油、食盐等,其中富含糖类的是。(5)、为了健康,我国推广使用强化铁酱油,这里的“铁”指的是(填“单质”或“元素”或“原子”)。(6)、许多家庭做饭用罐装的液化石油气作燃料。液化石油气是石油化工的一种产品,石油是一种能源(填“可再生”或“不可再生”);若厨房不慎失火时,移走液化石油气罐,这是利用了原理灭火。17. 构建类价二维图是化学学习元素及其化合物的重要方法。如图表示的是硫元素的类价二维图,请回答下列问题:
 (1)、a对应物质的类别是;c点对应物质的化学式为。(2)、如图是某反应的微粒示意图:
(1)、a对应物质的类别是;c点对应物质的化学式为。(2)、如图是某反应的微粒示意图:
该反应的化学方程式是;甲物质会导致雨水pH减小,形成。可通过甲物质与(写化学式)反应生成CaSO3来降低对环境的危害。
(3)、根据类价二维图信息,从含硫物质中选择合适物质完成下列化学方程式:Na2S2O3+═Na2SO4+b↑+S↓+H2O(写化学式)。三、科普阅读题
-
18. 阅读下列科技短文,回答问题。
2021年5月,娄底市首次实施初中毕业学生英语口语考查,考查过程中很多学校使用了我国自主生产的骨传导耳机,该耳机获德国红点设计多项国际大奖,耳机釆用钛合金骨架,与皮肤接触的部位选用了橡胶及塑料材质,配以最新的蓝牙芯片和双麦克风降噪等技术。用于制取金属钛的原料是化合物钛酸锂(Li2TiO3),可用适量TiO2和Li2CO3一起加热至约950℃来制取碳酸锂,同时生成温室气体。钛酸锂为白色粉末,不溶于水,应密闭放置在阴凉干燥处,避光,不能与明火接触。
 (1)、耳机所用材质属于有机合成材料的是(填一种物质即可)。(2)、使用的钛合金相对于纯金属的优点有(填一个即可)。(3)、请写出TiO2和Li2CO3制取钛酸锂反应的化学方程式。
(1)、耳机所用材质属于有机合成材料的是(填一种物质即可)。(2)、使用的钛合金相对于纯金属的优点有(填一个即可)。(3)、请写出TiO2和Li2CO3制取钛酸锂反应的化学方程式。四、综合题
-
19. 波尔多液含氢氧化钙、氢氧化铜和硫酸钙等物质,是农业上常用的杀菌剂。一种生产波尔多液的工艺流程如图。
 (1)、“煅烧”的化学方程式为 ,该反应属于基本反应类型中的反应。(2)、“混合”时不能用铁制容器,原因是(用化学方程式表示)。(3)、“混合”时需不断搅拌,目的是。(4)、“混合”后得到的波尔多液温度明显高于室温,原因是。20. 化学是一门以实验为基础的学科。请结合下列实验装置图回答问题:
(1)、“煅烧”的化学方程式为 ,该反应属于基本反应类型中的反应。(2)、“混合”时不能用铁制容器,原因是(用化学方程式表示)。(3)、“混合”时需不断搅拌,目的是。(4)、“混合”后得到的波尔多液温度明显高于室温,原因是。20. 化学是一门以实验为基础的学科。请结合下列实验装置图回答问题: (1)、写出图中标号①仪器的名称。(2)、某同学加热高锰酸钾制取并收集氧气,反应的化学方程式为;应选择的装置组合是。(填字母)(3)、A装置与C装置比较,A装置的优点是可以控制反应的发生和停止。请写出一个利用A装置此优点的反应化学方程式。(4)、实验室可用金属与浓硫酸反应制取SO2气体,金属锌或金属铜都能与浓硫酸反应制SO2气体。欲制取一瓶较纯净的SO2气体,最好选择金属(填“锌”或“铜”),选择理由是。21. 化学兴趣小组对“可乐除铁锈”实验展开探究。同学们将几枚生锈的铁钉放入某品牌的可乐中,观察到铁钉表面有气泡产生,容器底部沉有固体物质。取出铁钉后用水清洗,铁钉恢复光亮。(1)、Ⅰ.容器底部固体成分探究。
(1)、写出图中标号①仪器的名称。(2)、某同学加热高锰酸钾制取并收集氧气,反应的化学方程式为;应选择的装置组合是。(填字母)(3)、A装置与C装置比较,A装置的优点是可以控制反应的发生和停止。请写出一个利用A装置此优点的反应化学方程式。(4)、实验室可用金属与浓硫酸反应制取SO2气体,金属锌或金属铜都能与浓硫酸反应制SO2气体。欲制取一瓶较纯净的SO2气体,最好选择金属(填“锌”或“铜”),选择理由是。21. 化学兴趣小组对“可乐除铁锈”实验展开探究。同学们将几枚生锈的铁钉放入某品牌的可乐中,观察到铁钉表面有气泡产生,容器底部沉有固体物质。取出铁钉后用水清洗,铁钉恢复光亮。(1)、Ⅰ.容器底部固体成分探究。【实验探究1】取出容器底部剩余的固体物质,用水清洗后干燥,分成甲、乙两份备用。
实验操作
实验现象
解释与结论
①用磁铁靠近固体物质甲
固体物质(填“能”或“不能”)被吸引
固体物质中不含铁单质
②将固体物质甲放入20%的盐酸中
固体逐渐消失,溶液变成黄色
固体物质主要是氧化铁,化学反应方程式为。
(2)、Ⅱ.溶液中逸出气体成分探究。【猜想假设】气体中除了可乐本身含有的CO2外,可能还有H2。
【查阅资料】无水硫酸铜为白色固体,遇水变蓝。
【实验探究2】将逸出气体依次通过图的组合装置。

①NaOH溶液的作用是。
②实验过程中观察到现象,证明逸出气体中含有氢气。
(3)、Ⅲ.深入探究【提出问题】铁钉表面已变光亮,而容器底部有大量铁锈剩余的原因是什么?
【猜想假设】①可乐太少,酸性物质量不足。②可乐酸性弱,与铁锈反应太慢。
【实验探究3】取可乐与锈铁钉反应后的剩余液,测得溶液仍然呈酸性,猜想①不成立。
【查阅资料】3%的稀盐酸pH约为1,某品牌可乐的pH值为3.39。质量分数为3%的稀盐酸比该品牌可乐的酸性(选填“弱”或“强”)。
【实验探究4】取另一份固体物质乙放入3%的稀盐酸中,振荡,观察无明显现象。
【实验结论】对比【实验探究1】和【实验探究4】的不同反应现象可得出:化学反应速率与反应物的有关。猜想②成立。
五、计算题
-
22. 氯化铜是重要的化工原料,可用作催化剂、杀虫剂等。为测定某氯化铜溶液中溶质的质量分数,小组同学取100g氯化铜溶液于烧杯中,逐滴加入溶质质量分数为16%的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。请回答下列问题:
 (1)、若实验室现有溶质质量分数为32%氢氧化钠溶液100g,欲配制成溶质质量分数为16%氢氧化钠溶液,需加入水的质量是g。(2)、计算氯化铜溶液中溶质的质量分数。(写出计算过程)
(1)、若实验室现有溶质质量分数为32%氢氧化钠溶液100g,欲配制成溶质质量分数为16%氢氧化钠溶液,需加入水的质量是g。(2)、计算氯化铜溶液中溶质的质量分数。(写出计算过程)
-