江苏省南京市、盐城市2022届高三年级第二次模拟考试化学试题
试卷更新日期:2022-03-29 类型:高考模拟
一、单选题
-
1. 2021年12月9日,我国宇航员在中国空间站直播了泡腾片水球实验。泡腾片中含有柠檬酸(结构如图所示)和碳酸钠等,溶于水产生气泡。下列说法不正确的是( )
 A、柠檬酸属于有机物 B、碳酸钠溶液呈碱性 C、产生的气体为 D、碳酸钠与柠檬酸发生了氧化还原反应2. 反应可用于制备火箭推进剂的燃料。下列有关说法正确的是( )A、的结构式为
A、柠檬酸属于有机物 B、碳酸钠溶液呈碱性 C、产生的气体为 D、碳酸钠与柠檬酸发生了氧化还原反应2. 反应可用于制备火箭推进剂的燃料。下列有关说法正确的是( )A、的结构式为 B、中子数为8的氮原子可表示为
C、O基态原子的价层电子排布式为
D、NaCl的电子式为
3. 二氧化氯()是一种黄绿色气体,易溶于水,在水中的溶解度约为的5倍,其水溶液在较高温度与光照下会生成与。是一种极易爆炸的强氧化性气体,下列有关物质的性质和用途具有对应关系的是( )A、能溶于水,可用于工业制盐酸 B、有强氧化性,可用于水体杀菌消毒 C、HClO不稳定,可用于棉、麻漂白 D、溶液呈酸性,可用于蚀刻电路板上的铜4. 实验室制备的反应为 , 下列有关实验室制备的实验原理和装置不能达到实验目的的是( )
B、中子数为8的氮原子可表示为
C、O基态原子的价层电子排布式为
D、NaCl的电子式为
3. 二氧化氯()是一种黄绿色气体,易溶于水,在水中的溶解度约为的5倍,其水溶液在较高温度与光照下会生成与。是一种极易爆炸的强氧化性气体,下列有关物质的性质和用途具有对应关系的是( )A、能溶于水,可用于工业制盐酸 B、有强氧化性,可用于水体杀菌消毒 C、HClO不稳定,可用于棉、麻漂白 D、溶液呈酸性,可用于蚀刻电路板上的铜4. 实验室制备的反应为 , 下列有关实验室制备的实验原理和装置不能达到实验目的的是( ) A、用装置甲获取 B、用装置乙制备 C、用装置丙吸收 D、用装置丁处理尾气5. 二氧化氯()是一种黄绿色气体,易溶于水,在水中的溶解度约为的5倍,其水溶液在较高温度与光照下会生成与。是一种极易爆炸的强氧化性气体,实验室制备的反应为。下列关于、和的说法正确的是( )A、属于共价化合物 B、中含有非极性键 C、的空间构型为平面三角形 D、与的键角相等6. 二氧化氯()是一种黄绿色气体,易溶于水,在水中的溶解度约为的5倍,其水溶液在较高温度与光照下会生成与。是一种极易爆炸的强氧化性气体,实验室制备的反应为。在指定条件下,下列选项所示的物质间转化能实现的是( )A、 B、浓HCl(aq) C、HClO(aq) D、NaClO(aq)7. 短周期元素X、Y、Z、W的原子序数依次增大。X、Y、Z是同一周期的非金属元素。化合物WZ的晶体为离子晶体,W的二价阳离子与Z的阴离子具有相同的电子层结构。为非极性分子。Y、Z氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。下列说法正确的是( )A、第一电离能: B、原子半径: C、电负性: D、X的最高价氧化物对应水化物的酸性比Y的弱8. 可用作杀虫剂,其制备步骤如下。
A、用装置甲获取 B、用装置乙制备 C、用装置丙吸收 D、用装置丁处理尾气5. 二氧化氯()是一种黄绿色气体,易溶于水,在水中的溶解度约为的5倍,其水溶液在较高温度与光照下会生成与。是一种极易爆炸的强氧化性气体,实验室制备的反应为。下列关于、和的说法正确的是( )A、属于共价化合物 B、中含有非极性键 C、的空间构型为平面三角形 D、与的键角相等6. 二氧化氯()是一种黄绿色气体,易溶于水,在水中的溶解度约为的5倍,其水溶液在较高温度与光照下会生成与。是一种极易爆炸的强氧化性气体,实验室制备的反应为。在指定条件下,下列选项所示的物质间转化能实现的是( )A、 B、浓HCl(aq) C、HClO(aq) D、NaClO(aq)7. 短周期元素X、Y、Z、W的原子序数依次增大。X、Y、Z是同一周期的非金属元素。化合物WZ的晶体为离子晶体,W的二价阳离子与Z的阴离子具有相同的电子层结构。为非极性分子。Y、Z氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。下列说法正确的是( )A、第一电离能: B、原子半径: C、电负性: D、X的最高价氧化物对应水化物的酸性比Y的弱8. 可用作杀虫剂,其制备步骤如下。步骤1:向足量铜粉与一定量稀的混合物中通入热空气,当铜粉不再溶解时,过滤得滤液。
步骤2:向步骤1所得滤液中边搅拌边滴加氨水,沉淀先增加后减少。当沉淀完全溶解时,停止滴加氨水。
步骤3:向步骤2所得溶液中加入95%乙醇,析出深蓝色晶体。
下列说法正确的是( )
A、步骤1发生反应的离子方程式为 B、步骤2所得溶液中大量存在的离子有、、、 C、步骤3加入95%乙醇的目的是降低的溶解量 D、中有12个配位键9. 氮化硅()是一种重要的结构陶瓷材料。用石英砂和原料气(含和少量)制备的操作流程如下(粗硅中含少量Fe、Cu的单质及化合物):
下列叙述不正确的是( )
A、“还原”主要被氧化为 B、“高温氮化”反应的化学方程式为 C、“操作X”可将原料气通过灼热的铜粉 D、“稀酸Y”可选用稀硝酸10. 化合物Y是一种药物中间体,其合成路线中的一步反应如下:
下列说法正确的是( )
A、X分子中所有原子均处于同一平面 B、X、Y分子中含有的官能团种类相同 C、X→Y发生了取代反应 D、等物质的量的X与Y分别与足量溴水反应,消耗的物质的量相同11. 热电厂尾气经处理得到较纯的 , 可用于原电池法生产硫酸,其工作原理如图所示。电池工作时,下列说法不正确的是( ) A、电极b为正极 B、溶液中由a极区向b极区迁移 C、电极a的电极反应式: D、a极消耗与b极消耗两者物质的量相等12. 室温下,通过下列实验探究Na2S溶液的性质。
A、电极b为正极 B、溶液中由a极区向b极区迁移 C、电极a的电极反应式: D、a极消耗与b极消耗两者物质的量相等12. 室温下,通过下列实验探究Na2S溶液的性质。实验
实验操作和现象
1
用pH试纸测定0.1mol·L-1Na2S溶液的pH,测得pH约为13
2
向0.1mol·L-1Na2S溶液中加入过量0.2mol·L-1AgNO3溶液,产生黑色沉淀
3
向0.1mol·L-1Na2S溶液中通入过量H2S,测得溶液pH约为9
4
向0.1mol·L-1Na2S溶液中滴加几滴0.05mol·L-1HCl,观察不到实验现象
下列有关说法正确的是( )
A、0.1mol-L-1Na2S溶液中存在 B、实验2反应静置后的上层清液中有 C、实验3得到的溶液中有 D、实验4说明H2S的酸性比HCl的酸性强13. 我国提出了2030年前碳达峰、2060年前碳中和的“双碳”目标。二氧化碳催化加氢合成是一种实现“双碳”目标的有效方法,其主要反应的热化学方程式为反应Ⅰ:
反应II:
下列说法正确的是( )
 A、1个固态晶胞(如上图)中含14个分子 B、反应 C、用E表示键能,反应I的 D、能与水互溶,主要原因是与分子间形成氢键14. 我国提出了2030年前碳达峰、2060年前碳中和的“双碳”目标。二氧化碳催化加氢合成是一种实现“双碳”目标的有效方法,其主要反应的热化学方程式为
A、1个固态晶胞(如上图)中含14个分子 B、反应 C、用E表示键能,反应I的 D、能与水互溶,主要原因是与分子间形成氢键14. 我国提出了2030年前碳达峰、2060年前碳中和的“双碳”目标。二氧化碳催化加氢合成是一种实现“双碳”目标的有效方法,其主要反应的热化学方程式为反应Ⅰ:
反应Ⅱ:
恒压下,时,甲醇产率随温度的变化如图所示(分子筛膜能选择性分离出)。下列关于该实验的说法不正确的是( )
 A、甲醇平衡产率随温度升高而降低的主要原因:温度升高,反应I平衡逆向移动 B、采用分子筛膜时的适宜反应温度:210℃ C、M→N点甲醇产率增大的原因:温度升高,反应I平衡常数增大 D、X点甲醇产率高于Y点的主要原因:分子筛膜可从反应体系中分离出 , 有利于反应I正向进行
A、甲醇平衡产率随温度升高而降低的主要原因:温度升高,反应I平衡逆向移动 B、采用分子筛膜时的适宜反应温度:210℃ C、M→N点甲醇产率增大的原因:温度升高,反应I平衡常数增大 D、X点甲醇产率高于Y点的主要原因:分子筛膜可从反应体系中分离出 , 有利于反应I正向进行二、填空题
-
15. 我国学者分别使用和作催化剂对燃煤烟气脱硝脱硫进行了研究。(1)、催化剂制备。在60〜100℃条件下,向足量NaOH溶液中通入一段时间,再加入适量新制溶液,充分反应后得到混合物X;向混合物X中加入溶液,充分反应后经磁铁吸附、洗涤、真空干燥,制得催化剂。
①通入的目的是。
②混合物X与反应生成和 , 该反应的化学方程式为。
(2)、催化剂性能研究。如图-1所示,当其他条件一定时,分别在无催化剂、作催化剂、作催化剂的条件下,测定浓度对模拟烟气(含一定比例的NO、、、)中NO和脱除率的影响,NO脱除率与浓度的关系如图-2所示。
已知·OH能将NO、氧化。·OH产生机理如下。
反应I:(慢反应)
反应II:(快反应)
①与作催化剂相比,相同条件下作催化剂时NO脱除率更高,其原因是。
②NO部分被氧化成。被NaOH溶液吸收生成两种含氧酸钠盐,该反应的离子方程式为。
③实验表明•OH氧化的速率比氧化NO速率慢。但在无催化剂、作催化剂、作催化剂的条件下,测得脱除率几乎均为100%的原因是。
16. F是一种治疗心脑血管疾病药物的中间体,其合成路线如下(表示苯基): (1)、C分子中采取杂化的碳原子数目是。(2)、D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:。
(1)、C分子中采取杂化的碳原子数目是。(2)、D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:。①能发生银镜反应和水解反应。
②分子中有5种不同化学环境的氢原子。
③每个苯环上只含1种官能团。
(3)、的反应需经历的过程,中间体X的分子式为。X→F的反应类型为。(4)、E—F的反应中有一种分子式为的副产物生成,该副产物的结构简式为。(5)、已知: , 写出以 和
和 为原料制备
为原料制备 的合成路线(无机溶剂和有机溶剂任用,合成路线流程图示例见本题题干)。 17. 以废锰酸锂电池为原料,回收、精铜的实验流程如下:
的合成路线(无机溶剂和有机溶剂任用,合成路线流程图示例见本题题干)。 17. 以废锰酸锂电池为原料,回收、精铜的实验流程如下: (1)、“浸取”在如图所示装置中进行。
(1)、“浸取”在如图所示装置中进行。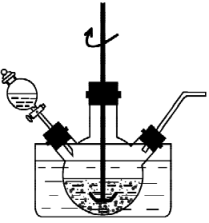
①将一定量“和石墨混合粉末”与溶液、溶液中的一种配成悬浊液,加入到三颈烧瓶中,75℃下通过滴液漏斗缓慢滴加另一种溶液。滴液漏斗中的溶液是。
②转化为的化学方程式为。
③保持温度、反应物和溶剂的量不变,能提高Mn元素浸出率的措施有。
(2)、补充以“铜箔和铝箔”为原料制备精铜的实验方案:;将所得精铜用蒸馏水洗净,干燥。实验中须使用的试剂溶液、不锈钢片、混合溶液,除常用仪器外须使用的仪器:直流电源。
(3)、通过下列方法测定的纯度:准确称取0.4000g样品,加入25.00mL溶液和适量硫酸,加热至完全反应(发生反应为),用标准溶液滴定过量的至终点,消耗标准溶液20.00mL(滴定反应为)。计算样品中的质量分数(写出计算过程)。18. 乙醇用途广泛且需求量大,寻求制备乙醇的新方法是研究的热点。(1)、醋酸甲酯催化加氢制备乙醇涉及的主要反应如下:I.
II.
III.
将的混合气体置于密闭容器中,在2.0MPa和不同温度下反应达到平衡时,的转化率和的选择性[]如图所示。

①若 , 则500K下反应达到平衡时生成的物质的量为mol。
②673〜723K平衡转化率几乎不变,其原因是。
(2)、以KOH溶液为电解质溶液,在阴极(铜板)转化为的机理如图所示。( 表示氢原子吸附在电极表面,也可用表示,其他物种以此类推;部分物种未画出)。
表示氢原子吸附在电极表面,也可用表示,其他物种以此类推;部分物种未画出)。

①在阴极上生成的电极反应式为。
②转化为的过程可描述为。
③与阴极使用铜板相比,阴极使用含的铜板可加快生成的速率,其原因可能是。