山东省临沂市2021年中考二模化学试题
试卷更新日期:2022-03-25 类型:中考模拟
一、单选题
-
1. 下列变化属于化学变化的是( )A、甘蔗榨汁 B、自行车胎爆裂 C、炭包吸附异味 D、鲜奶制成酸奶2. 把少量生活中的物质分别放入水中,充分搅拌,可以得到溶液的是( )A、面粉 B、牛奶 C、蔗糖 D、植物油3. 这是萌萌同学的一次化学用语练习的部分内容,其中正确的是( )A、氢气:He2 B、两个五氧化二磷分子:2P2O5 C、N2:两个氮原子 D、2Fe2+:两个铁离子4. 规范的实验操作是保证实验成功的关键。下列实捡操作正确的是( )A、量取液体
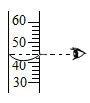 B、测定溶液的pH值
B、测定溶液的pH值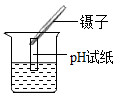 C、倾倒液体
C、倾倒液体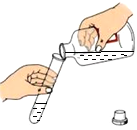 D、点燃酒精灯
D、点燃酒精灯 5. 按如图所示装置,玻璃棒末端固定一团喷有酚酞溶液的脱脂棉Y。先加入物质X,再塞上带玻璃棒的橡胶塞。片刻后,能观察到喷有酚酞溶液的脱脂棉Y变红,则物质X可能是( )
5. 按如图所示装置,玻璃棒末端固定一团喷有酚酞溶液的脱脂棉Y。先加入物质X,再塞上带玻璃棒的橡胶塞。片刻后,能观察到喷有酚酞溶液的脱脂棉Y变红,则物质X可能是( )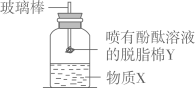 A、浓盐酸 B、浓氨水 C、浓醋酸 D、浓氢氧化钠溶液6. 抗癌新药紫衫醇的化学式为C47H51NO4 , 下列说法正确的是( )A、紫衫醇属于有机高分子化合物 B、紫衫醇由C,H,O,N四种元素组成 C、紫衫醇中氢元素的质量分数最大 D、紫衫醇中氢、氧元素的质量比为1:47. 下列对物质的分类不正确的是( )A、
A、浓盐酸 B、浓氨水 C、浓醋酸 D、浓氢氧化钠溶液6. 抗癌新药紫衫醇的化学式为C47H51NO4 , 下列说法正确的是( )A、紫衫醇属于有机高分子化合物 B、紫衫醇由C,H,O,N四种元素组成 C、紫衫醇中氢元素的质量分数最大 D、紫衫醇中氢、氧元素的质量比为1:47. 下列对物质的分类不正确的是( )A、 单质
B、
单质
B、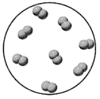 化合物
C、
化合物
C、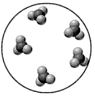 化合物
D、
化合物
D、 混合物
8. “宏观辨识与微观探析”是化学学科的核心素养之一。下列说法中,不正确的是( )A、水和过氧化氢化学性质不同——构成二者的分子不同 B、教室内消毒后,消毒水气味弥漫四周——分子在不停地运动 C、压瘪的乒乓球在热水中能够鼓起来——温度升高,分子变大 D、酸溶液具有相似的化学性质——酸溶液中都含有大量的氢离子9. 下表为四种食物的近似pH,你认为胃酸过多的患者不宜多吃的食物是( )
混合物
8. “宏观辨识与微观探析”是化学学科的核心素养之一。下列说法中,不正确的是( )A、水和过氧化氢化学性质不同——构成二者的分子不同 B、教室内消毒后,消毒水气味弥漫四周——分子在不停地运动 C、压瘪的乒乓球在热水中能够鼓起来——温度升高,分子变大 D、酸溶液具有相似的化学性质——酸溶液中都含有大量的氢离子9. 下表为四种食物的近似pH,你认为胃酸过多的患者不宜多吃的食物是( )食物
苹果汁
豆浆
玉米粥
鸡蛋清
pH
2.9-3.3
7.4-7.9
6.8-8.0
7.6-8.0
A、苹果汁 B、豆浆 C、玉米粥 D、鸡蛋清10. 下列物质混合,能发生反应且反应后溶液质量减少的是( )A、铜丝与稀硫酸 B、稀硫酸与NaOH溶液 C、铁锈与稀硫酸 D、铜丝与AgNO3溶液11. 下列对实验现象的描述符合事实的是( )A、NH4NO3固体溶于水中,溶液温度降低 B、无色酚酞溶液滴入稀盐酸中,溶液变红 C、CO通过灼热的Fe2O3 , 黑色固体变成红色 D、电解水,正、负极产生的气体体积比约为2∶112. 安全问题与人类生活、生产息息相关。下列说法正确的是( )A、油库、面粉加工厂等场所必须严禁烟火 B、在有明火的区域内可以喷洒含酒精的消毒剂 C、霉变大米中含有黄曲霉素,煮熟仍可食用 D、夜间发现家庭内燃气泄漏,应立即开灯检查13. 证据推理是化学学科核心素养的重要内容,下列推理正确的是( )A、同种元素的质子数相同,所以质子数相同的微粒一定是同种元素 B、化合物由不同种元素组成,所以由不同种元素组成的纯净物一定是化合物 C、中和反应是有盐和水生成的反应,所以有盐和水生成的反应一定是中和反应 D、燃烧都伴随有发光、放热现象,所以有发光、放热现象的变化一定是燃烧14. 下列有关说法不正确的是( )A、古代用墨书写的字画能够保存很长时间不变色,是因为在常温下碳化学性质不活泼 B、二氧化碳使湿润的紫色石蕊纸花变红,是因为二氧化碳能与水反应生成碳酸 C、扶贫工作组在某村利用沼气(主要成分是甲烷)发电,是将化学能转化为电能 D、一氧化碳和二氧化碳都是由碳元素和氧元素组成,所以它们的化学性质相同15. 芯片是电脑、智能家电的核心部件,它是以高纯度的单质硅(Si)为材料制成的。硅及其氧化物能发生如下反应:①
②
③
④
下列说法不正确的是( )
A、反应③属于置换反应 B、上述反应中共生成三种可燃性气体 C、Na2SiO3中Si为+4价 D、Si和SiO2在一定条件下可以相互转化16. 河道两旁有甲、乙两厂,它们排放的工业废水中共含有H+、Na+、Ba2+、Cl-、SO、CO六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,甲厂废水中的离子是( )A、H+、Na+、Ba2+ B、H+、Ba2+、Cl- C、Na+、SO、CO D、H+、SO、CO17. 如图所示的图象能正确反映对应变化关系的是( )A、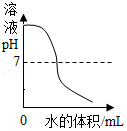 向一定浓度的NaOH溶液中加水稀释
B、
向一定浓度的NaOH溶液中加水稀释
B、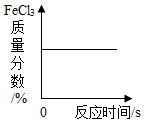 FeCl3催化H2O2溶液的分解
C、
FeCl3催化H2O2溶液的分解
C、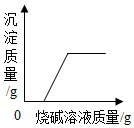 向硫酸和硫酸铜的混合溶液中逐滴加入烧碱溶液至过量
D、
向硫酸和硫酸铜的混合溶液中逐滴加入烧碱溶液至过量
D、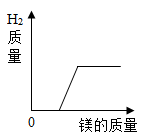 向一定量的稀盐酸中,加入足量的金属铁,产生的氢气的质量
18. 除去下列物质中的少量杂质,所选用试剂及实验操作均正确的是()
向一定量的稀盐酸中,加入足量的金属铁,产生的氢气的质量
18. 除去下列物质中的少量杂质,所选用试剂及实验操作均正确的是()选项
物质(括号内为杂质)
所用试剂及只要实验操作
A
氯化钠(氯化镁)
加水溶解、过滤,蒸发
B
硝酸钠溶液(硫酸钠)
加入适量氯化钡溶液,过滤
C
氯化钙溶液(盐酸)
加入过量的碳酸钙,过滤
D
氧气(氮气)
缓慢通过灼热的铜网
A、A B、B C、C D、D二、填空题
-
19. 化学与人类生活、生产活动息息相关,根据所学化学知识完成下列问题:(1)、用洗涤剂洗去餐具上的油污会产生现象。(2)、“共享电动车”方便市民绿色出行,有效缓解了城市交通压力,减少了大气污染,成为现代城市的又一道靓丽“风景”。为防止电动车钢制车架与空气中的、(用化学式表示)等接触而生锈,通常在车架表面进行喷漆处理。(3)、市售“自热米饭”的自加热原理:饭盒夹层中的水与生石灰接触,反应放出大量热。该反应的化学方程式为。(4)、我国铁的年产量世界第一,工业上炼铁利用一氧化碳来还原赤铁矿(主要成分氧化铁),请用化学方程式表示这一原理。20. 近期,三星堆遗址考古新发现6座“祭祀坑”,现已出土了巨青铜面具、青铜神树、象牙等重要文物,三星堆遗址的重大考古发现,向世界展示了中华传统文化所蕴含的丰富宝藏和巨大魅力。(1)、青铜属于(填“合金”“氧化物”“化合物”之一)。(2)、铜质的器皿长期暴露在潮湿的空气中会长出一层绿色的铜锈,铜锈的主要成分是碱式碳酸铜【Cu2(OH)2CO3】。从元素守恒的角度分析,你认为铜的锈蚀是单质铜与下列哪些物质共同作用的结果____(填序号)。A、O2、N2、H2O B、O2、CO2、N2 C、O2、H2O、CO221. 近年来,我国科研人员在“甲烷二氧化碳重整和Ni基催化剂”的研究方面取得突破。如图是甲烷与二氧化碳反应的微观示意图。
 (1)、写出该反应的化学方程式。(2)、该反应利用两种温室气体,兼具环保和经济价值;反应难点之一是破坏甲烷分子、二氧化碳分子的稳定结构,分为(填微粒化学符号)并重新组合。22. 下图是给水通电的简易实验装置。则A中试管中产生的气体是 ,检验B试管内气体的方法是 ,装置中发生反应的化学方程式是 。
(1)、写出该反应的化学方程式。(2)、该反应利用两种温室气体,兼具环保和经济价值;反应难点之一是破坏甲烷分子、二氧化碳分子的稳定结构,分为(填微粒化学符号)并重新组合。22. 下图是给水通电的简易实验装置。则A中试管中产生的气体是 ,检验B试管内气体的方法是 ,装置中发生反应的化学方程式是 。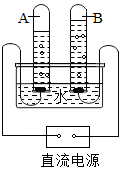 23. 2021年2月10日19时52分,中国首次火星探测任务“天问一号”探则器成功进入环火轨道,成为中国第一颗人造火星卫星。试回答下列可题:(1)、“天问一号”由长征五号遥四运载火箭发射升空,长征五号火箭采用液氢、液氧作推进剂。试写出氢气与氧气发生反应的化学方程式。(2)、“天问一号”计划在2021年5月至6月择机着陆火星,释放火星车。火星车主要采用太阳能电池板发电,太阳能电池的作用是将能转化为电能。(3)、“天问一号”釆用了我国自主研制的高性能碳化硅增强铝基复合材料。工业上制取碳化硅的化学反应方程式为: , 则X的化学式为。(4)、“天问一号”使用工程塑料、玻璃钢等作为隔热材料,用二硫化钼(MoS2)固体润滑剂等作为运动部件的润滑材料。已知MoS2中硫元素的化合价为-2价,则其中钼元素(Mo)的化合价为。24. 根据下列所提供的粒子结构示意图回答问题。
23. 2021年2月10日19时52分,中国首次火星探测任务“天问一号”探则器成功进入环火轨道,成为中国第一颗人造火星卫星。试回答下列可题:(1)、“天问一号”由长征五号遥四运载火箭发射升空,长征五号火箭采用液氢、液氧作推进剂。试写出氢气与氧气发生反应的化学方程式。(2)、“天问一号”计划在2021年5月至6月择机着陆火星,释放火星车。火星车主要采用太阳能电池板发电,太阳能电池的作用是将能转化为电能。(3)、“天问一号”釆用了我国自主研制的高性能碳化硅增强铝基复合材料。工业上制取碳化硅的化学反应方程式为: , 则X的化学式为。(4)、“天问一号”使用工程塑料、玻璃钢等作为隔热材料,用二硫化钼(MoS2)固体润滑剂等作为运动部件的润滑材料。已知MoS2中硫元素的化合价为-2价,则其中钼元素(Mo)的化合价为。24. 根据下列所提供的粒子结构示意图回答问题。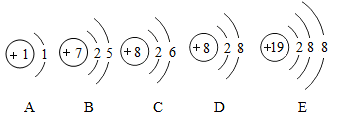 (1)、五种粒子对应的元素中属于同种元素的是(填序号)。(2)、粒子E所对应的元素位于元素周期表的第周期。(3)、A,B,C所对应的三种元素能组成一种常见的盐,该盐的化学式为 , 此盐做氮肥时不可与熟石灰共用原因(用化学方程式表示)。25. A、B、C三种固体物质(均不含结晶水)的溶解度曲线如图所示,请回答:
(1)、五种粒子对应的元素中属于同种元素的是(填序号)。(2)、粒子E所对应的元素位于元素周期表的第周期。(3)、A,B,C所对应的三种元素能组成一种常见的盐,该盐的化学式为 , 此盐做氮肥时不可与熟石灰共用原因(用化学方程式表示)。25. A、B、C三种固体物质(均不含结晶水)的溶解度曲线如图所示,请回答: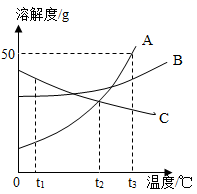
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是。
②当温度在t2~t3℃之间时,A物质与B物质(填“能”或“不能”)配制溶质质量分数相同的饱和溶液。
③将A、B、C三种物质的饱和溶液分别由t2℃升温到t3℃,所得溶液中溶质的质量分数最大的物质是。
④t3℃时将75gA的饱和溶液稀释成20%的溶液需加g水。
26. 将一定质量的锌粒投入到含有Cu(NO3)2和Fe(NO3)2的混合溶液中,充分反应后过滤,若滤液呈无色;(1)、则滤渣中一定含有。(2)、滤液中一定含有的溶质阳离子是。(3)、请写出锌和硝酸铜反应的化学方程式。三、综合题
-
27. 工业烟气脱硫就是将烟气中含有的二氧化硫除去。一种采用“双碱法”脱硫的工业流程示意图如下:
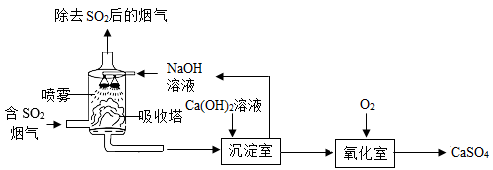 (1)、吸收塔中,用NaOH溶液吸收SO2 , 生成和H2O。NaOH溶液喷成雾状能充分吸收SO2的原因是。(2)、沉淀室中,发生反应的化学方程式为。(3)、氧化室中,化学反应的基本类型是反应。(4)、上述流程中,可以循环利用的物质是 , 有利于节约成本。28. 以下是实验制取气体的常用装置,请据图完成下列问题。
(1)、吸收塔中,用NaOH溶液吸收SO2 , 生成和H2O。NaOH溶液喷成雾状能充分吸收SO2的原因是。(2)、沉淀室中,发生反应的化学方程式为。(3)、氧化室中,化学反应的基本类型是反应。(4)、上述流程中,可以循环利用的物质是 , 有利于节约成本。28. 以下是实验制取气体的常用装置,请据图完成下列问题。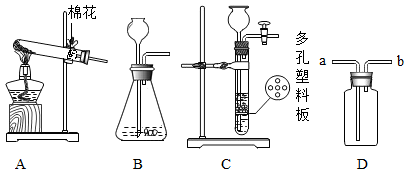 (1)、用A装置制取氧气,写出该反应的化学方程式。(2)、用C装置制取二氧化碳比用B装置的突出优点是。(3)、若用D装置检验二氧化碳,瓶内发生反应的化学方程式是。(4)、实验室可用次氯酸钠固体粉末和浓盐酸在常温下反应制取氯气,氯气的密度比空气大、有毒,可与水反应生成酸。据此你认为实捡室制取较多量的氯气时,最好选用的发生装置是。29. 某教师在进行“常见的碱”的教学时做了以下演示实验:取少量纯净的氢氧化钠固体于50mL干燥的烧杯中,置于电子天平上。一段时间后,氢氧化钠固体表面出现了液体,天平示数增加。取下烧杯,将其放置在空气中。一周后,向烧杯中加适量水配制成溶液,取少量烧杯中的溶液于试管中,滴加足量稀盐酸,观察到有气泡冒出。(1)、(交流与解释)
(1)、用A装置制取氧气,写出该反应的化学方程式。(2)、用C装置制取二氧化碳比用B装置的突出优点是。(3)、若用D装置检验二氧化碳,瓶内发生反应的化学方程式是。(4)、实验室可用次氯酸钠固体粉末和浓盐酸在常温下反应制取氯气,氯气的密度比空气大、有毒,可与水反应生成酸。据此你认为实捡室制取较多量的氯气时,最好选用的发生装置是。29. 某教师在进行“常见的碱”的教学时做了以下演示实验:取少量纯净的氢氧化钠固体于50mL干燥的烧杯中,置于电子天平上。一段时间后,氢氧化钠固体表面出现了液体,天平示数增加。取下烧杯,将其放置在空气中。一周后,向烧杯中加适量水配制成溶液,取少量烧杯中的溶液于试管中,滴加足量稀盐酸,观察到有气泡冒出。(1)、(交流与解释)①氢氧化钠固体表面出现液体是因为氢氧化钠吸收空气中的水分而潮解。
②电子天平示数增加的原因除了吸收水分以外,还有另一个原因是(用化学方程式表示)。
(2)、教师安排兴趣小组同学对烧杯中的溶液是否还含有氢氧化钠进行了以下探究。(作出猜想)猜想一:有氢氧化钠
猜想二:没有氢氧化钠
(查阅资料)BaCl2溶液、NaNO3溶液、Ba(NO3)2溶液均呈中性。
(进行实验)小明同学取少量烧杯中的溶液于试管中,滴入几滴无色酚酞,观察到溶液变红,小明同学认为猜想一成立。
(交流与评价)小玲同学认为小明同学的结论不一定正确,原因是。于是,小玲同学继续进行探究。
(3)、(进行实验)实验操作
实验现象
实验结论
小玲同学在小明同学所做实验后的溶液中,滴入足量的Ba(NO3)2溶液
猜想一成立
(4)、(反思与拓展)①根据氢氧化钠固体易潮解的性质,可用氢氧化钠固体作某些气体的。
②另取少量烧杯中的溶液进行以下实验,也能证明猜想一成立的是(填序号)。
A 先加足量稀盐酸,再滴加紫色石蕊溶液
B 先加足量BaCl2溶液,静置,取上层清液,再滴加CuCl2溶液
C 先加足量Ca(OH)2溶液,静置,取上层清液,再滴加酚酞溶液
D 先加足量Ba(NO3)2溶液,静置,取上层清液,再滴加FeCl3溶液
四、计算题
-
30. 戊二醛(C5H8O2)是新一代消毒剂,在防控新冠疫情的过程中被广泛使用。回答下列问题:(1)、戊二醛的相对分子质量为。(2)、戊二醛中含碳的质量分数为。31. 我国化学家侯德榜创立了侯氏制碱法,为世界制碱工业作出了突出贡献。在实际生产的产品碳酸钠中会混有少量的氯化钠,现有该样品混合物20.4g,将其放入一洁净的烧杯中,向其中逐滴滴入7.3%的稀盐酸,放出的气体质量与滴加稀盐酸质量的关系如下图所示。请回答下列问题:
 (1)、当滴加稀盐酸至图中B点时,烧杯中溶液的pH7(“<”、“>”或“=”)。(2)、该样品混合物中碳酸钠的质量是g。(3)、当滴加稀盐酸至图中A点时,烧杯中所得溶液为不饱和溶液,请计算此时溶液中的溶质质量分数。(写出计算过程,计算结果保留至0.1%)
(1)、当滴加稀盐酸至图中B点时,烧杯中溶液的pH7(“<”、“>”或“=”)。(2)、该样品混合物中碳酸钠的质量是g。(3)、当滴加稀盐酸至图中A点时,烧杯中所得溶液为不饱和溶液,请计算此时溶液中的溶质质量分数。(写出计算过程,计算结果保留至0.1%)