山东省济宁市曲阜市2021年中考二模化学试题
试卷更新日期:2022-03-25 类型:中考模拟
一、单选题
-
1. 生活中的下列做法,利用了化学变化的是( )A、用牙膏去除茶渍 B、用电吹风机吹干头发 C、用灼烧的方法区分羊毛和涤纶 D、用汽油清洗手上的油渍2. 下列有关物质的性质与用途不具有对应关系的是( )A、铁粉可以与空气中的氧气和水反应 铁粉可做食品保鲜剂 B、水分解时吸收热量 水可用作灭火剂 C、镁能在空气中燃烧发出耀眼的白光 镁用于制作照明弹 D、氦气密度仅大于氢气,且性质很稳定 氦气可用作飞艇的填充气3. 元素观、微粒观是化学的重要观念。下列有关元素和微粒的说据不正确的是( )A、分子、原子和离子都是构成物质的粒子 B、元素的原子序数与该元素原子核电荷数在数值上相同 C、水是由氢原子和氧原子构成的化合物 D、在物质发生化学变化时,原子的种类不变,元素的种类也不会改变4. 下列物质的分类,正确的一组是( )A、Cu、N、O3都属于单质 B、HNO3、H2SO3、NH4HCO3都属于酸 C、MgO、KIO3、Ca(HCO3)2都属于盐 D、CH4、C2H2、CH3CH2OH都属于有机物5. 下列化学方程式及对应的基本反应类型都正确的是( )A、2Al+3O2Al2O3 化合反应 B、2KMnO4KMnO4+MnO2+O2↑ 分解反应 C、2NaOH+ BaCl2=2NaCl+ Ba(OH)2↓ 复分解反应 D、2CO+ Fe2O32Fe+2CO2 置换反应6. 下列操作能达到目的是( )A、稀释浓硫酸时,将水沿容器璧慢慢注入浓硫酸中,并不断搅拌 B、溶解食盐时,用玻璃棒搅拌以增大氯化钠的溶解度 C、将带火星的木条伸入集气瓶中检验氧气已经集满 D、蒸发操作中,当蒸发皿中出现较多固体时,停止加热7. 某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是( )
 A、M的溶解度曲线为a曲线 B、升温可以使N的饱和溶液变浑浊 C、M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大 D、如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N8. 化学是一门以实验为基础的科学。下列实验设计能达到实验目的的是( )
A、M的溶解度曲线为a曲线 B、升温可以使N的饱和溶液变浑浊 C、M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大 D、如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N8. 化学是一门以实验为基础的科学。下列实验设计能达到实验目的的是( )选项
实验目的
实验设计
A.
分离NaCl和KNO3的固体混合物
将混合物先加水制成热饱和溶液,再冷却
B.
除去FeCl2溶液中少量 CuCl2
加入足量的Fe粉,过滤
C.
制备MgSO4
将Mg(OH)2和CuSO4溶液混合后过滤
D.
检验某溶液中是否含有
滴加BaCl2溶液,观察是否有沉淀产生
A、A B、B C、C D、D9. 向等质量的镁粉和铁粉中分别逐滴加入同浓度的稀盐酸至过量,酸溶液的质量与生成盐的质量如下图所示,请根据题干和图像信息判断,下列说法正确的是( )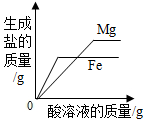
①镁粉消耗稀盐酸的质量多
②参加反应的稀盐酸的质量相等
③金属铁比金属镁相对原子质量大
④铁粉与稀盐酸反应比镁粉快
A、①③ B、①④ C、②③ D、③④10. 某固体由Ba2+、Cu2+、Na+、Cl-、CO、SO中的几种离子构成,取一定质量的该固体样品,进行如下实验:①将固体溶于水得无色透明溶液,加入足量BaCl2溶液,过滤后得到5克白色沉淀;②在沉淀中加入过量稀硝酸,仍有3克白色沉淀;③在滤液中滴加AgNO3溶液,产生白色沉淀。则该固体中一定含有( )A、Na+、CO、SO B、Na+、Ba2+、Cl- C、Cl-、CO、SO D、Cu2+、CO、SO二、填空题
-
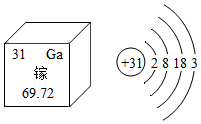
11. 按要求用适当的数字和化学符号回答下面问题:(1)、2个氨分子;(2)、一种金属氧化物;(3)、+2价的镁元素;(4)、氯酸钾溶液中的阴离子。12. 金属镓的性质与铝相似,镓在元素周期表中的相关信息及原子结构示意图如图,请回答下列问题:(1)、镓元素的相对原子质量。(2)、镓原子的最外层电子数为个。(3)、根据原子结构示意图,可知镓原子的最外层电子在反应中容易失去,请写出金属镓与稀硫酸反应的化学方程式。
 13. 化肥和农药的使用,使人类实现了由传统农业到现代农业的跨越。化肥和农药对粮食增产有着非常重要的作用,在世界范围内,化肥对粮食增产的贡献率已超过40%。根据所含主要植物营养元素的不同,化肥可分为氮肥、磷肥、钾肥和复合肥料等。铵态氮肥与碱性物质混用会使肥效降低。不同的化肥对农作物生长的作用不同。(1)、下列几种化肥中,属于复合肥的是( )
13. 化肥和农药的使用,使人类实现了由传统农业到现代农业的跨越。化肥和农药对粮食增产有着非常重要的作用,在世界范围内,化肥对粮食增产的贡献率已超过40%。根据所含主要植物营养元素的不同,化肥可分为氮肥、磷肥、钾肥和复合肥料等。铵态氮肥与碱性物质混用会使肥效降低。不同的化肥对农作物生长的作用不同。(1)、下列几种化肥中,属于复合肥的是( )①NH4NO3 ②K2SO4 ③KNO3 ④CO(NH2)2 ⑤NH4H2PO4
(2)、现有NH4NO3和K2SO4两种化肥,写出鉴别它们的方法,发生化学反应的,写出化学反应方程式。三、综合题
-
14. MgSO4·7H2O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO2和MgCO3 , 还含有少量FeCO3)为原料制备MgSO4·7H2O的主要流程如下图:

已知:SiO2既不溶于水也不溶于稀硫酸。请回答下列问题:
(1)、“操作a”的名称是。(2)、MgCO3溶于稀硫酸的化学方程式为。(3)、“溶液A”中加入H2O2溶液的目的是把Fe2+转化为Fe3+ , 则溶液B中一定含有溶质为。15. 某固体混合物可能含有FeCl3、CaCO3、Na2CO3、KOH中的一种或两种,为了确定该混合物的成分,进行如下实验:步骤I:取少量固体于烧杯中,加水,搅拌,固体全部溶解,得到无色溶液A。
步骤Ⅱ:取少量溶液A于试管中,滴加过量MgCl2溶液,有白色沉淀产生;再加入过量稀盐酸,沉淀消失,有气泡产生。
(1)、步骤Ⅱ中产生的气泡是(填化学式)。(2)、根据上述实验推断该混合物的成分,肯定含有的是 , 可能含有的是。(3)、若进一步确定混合物组成,依次用到的试剂是。16.(1)、某化学兴趣小组在实验室发现一瓶混入Na2 CO3的NaOH固体。于是他们对该固体中Na2 CO3的含量进行探究。[查阅资料]
Ⅰ、碱石灰是氢氧化钠与氧化钙的固体混合物。
Ⅱ、无水硫酸铜是一种白色固体,遇水会变成蓝色。
[设计实验]同学们用图1所示装置测定反应后生成CO2的质量(装置气密性良好,浓硫酸、碱石灰均足量)。称取一定质量的样品于锥形瓶中,通入一段时间空气后,向样品中滴加稀硫酸,待样品反应完全,继续通入一段时间空气后,测出生成CO2的质量,计算。

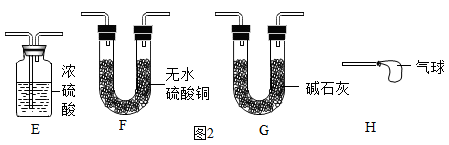
①图1中,装置A中反应化学方程式为(写出一个即可);浓硫酸的作用是。待样品反应完全,继续通入一段时间空气,目的是。为测出生成CO2的质量,需要在样品反应前后分别称量装置(填裝置序号)的质量。
②小红同学认为图1装置设计还存在一个明显敏陷,可增加图2中的装置进行改进,改进后整套装置的连接顺序为(按气流方向填装置序号)。
③小青同学认为图1中如果没有D装置,测得该固体中Na2 CO3的含量会偏大,原因是。
[反思与评价]设计实验方案应使实验简便、误差小。
(2)、现有一包黑色固体粉末,可能含有炭粉、CuO、Fe3O4中的两种或者三种,某化学兴趣小组通过实验探究其成分。[查阅资料]Fe3O4为黑色粉末,能与盐酸反应,生成FeCl2和FeCl3 , 含有Fe3+的盐溶液遇到硫氰化钾(KSCN)溶液时变成红色。
[实验探究]取一定量的固体于试管中,加足量的盐酸,充分反应后有部分固体溶解,则黑色固体中一定含有。过滤,得到滤液A,并对滤液A的成分进行如下探究:
实验操作
实验现象
实验结论
实验1:取一定量滤液A于试管中,插入银白色铁丝
铁丝上无红色固体析出
该固体物质一定没有
实验2:
滤液A中一定还含有的物质是氯化铁
通过实验判断该固体物质一定还含有Fe3O4 , 写出Fe3O4与盐酸反应的化学方程式:。
四、计算题