广西河池市2021年中考化学试题
试卷更新日期:2022-03-10 类型:中考真卷
一、单选题
-
1. 下列变化过程中主要发生物理变化的是( )A、光合作用 B、食物腐败 C、湿衣晒干 D、纸张燃烧2. 在空气的成分中,体积分数约占21%的是( )A、氮气 B、二氧化碳 C、氧气 D、稀有气体3. 2021年3月我国北方地区遭遇了近10年来最严重的沙尘暴天气,对空气造成了污染。沙尘暴含有的主要污染物是( )A、二氧化硫 B、一氧化碳 C、二氧化氮 D、可吸入颗粒物4. 正确的实验操作是实验成功的重要保证。下列操作中正确的是( )A、加热液体
 B、称量固体
B、称量固体 C、倾倒液体
C、倾倒液体 D、点燃酒精灯
D、点燃酒精灯 5. 在公园里行走,常能闻到各种花的香味,主要原因是( )A、分子总在不断运动 B、分子的体积变大 C、分子的数目变多 D、分子之间的间隔变小6. 下列有关实验现象描述正确的是( )A、铁丝在空气中剧烈燃烧,火星四射 B、红磷在空气中燃烧冒出大量的白色烟雾 C、木炭在氧气中燃烧发出白光,生成二氧化碳气体 D、硫在氧气中燃烧发出蓝紫色火焰7. 下列四种物质中,属于酸的是( )A、H2O2 B、NH4Cl C、Mg(OH)2 D、HNO38. 每年的5月31日是世界无烟日。吸烟有害健康,香烟的烟气中有几百种有毒物质,其中极易与血液中的血红蛋白结合,使人中毒的是( )A、焦油 B、尼古丁 C、一氧化碳 D、二氧化碳9. 下列四种物质中,所含硫元素的化合价最高的是( )A、S B、H2S C、SO3 D、H2SO310. 下列现象不能用质量守恒定律解释的是( )A、石蜡熔化前后,其质量不变 B、铁钉和硫酸铜溶液反应,反应前后物质的总质量不变 C、木材在空气中燃烧后化为灰烬,灰烬的质量比木材的质量减小 D、铜丝在空气中加热,生成物的质量比原来铜丝的质量增大11. 下列各组中的两种物质混合,充分搅拌后,不能得到溶液的是( )A、碘和汽油 B、碘和酒精 C、高锰酸钾和汽油 D、高锰酸钾和水12. 如图为四种原子的结构示意图,其中化学性质相似的一组是( )
5. 在公园里行走,常能闻到各种花的香味,主要原因是( )A、分子总在不断运动 B、分子的体积变大 C、分子的数目变多 D、分子之间的间隔变小6. 下列有关实验现象描述正确的是( )A、铁丝在空气中剧烈燃烧,火星四射 B、红磷在空气中燃烧冒出大量的白色烟雾 C、木炭在氧气中燃烧发出白光,生成二氧化碳气体 D、硫在氧气中燃烧发出蓝紫色火焰7. 下列四种物质中,属于酸的是( )A、H2O2 B、NH4Cl C、Mg(OH)2 D、HNO38. 每年的5月31日是世界无烟日。吸烟有害健康,香烟的烟气中有几百种有毒物质,其中极易与血液中的血红蛋白结合,使人中毒的是( )A、焦油 B、尼古丁 C、一氧化碳 D、二氧化碳9. 下列四种物质中,所含硫元素的化合价最高的是( )A、S B、H2S C、SO3 D、H2SO310. 下列现象不能用质量守恒定律解释的是( )A、石蜡熔化前后,其质量不变 B、铁钉和硫酸铜溶液反应,反应前后物质的总质量不变 C、木材在空气中燃烧后化为灰烬,灰烬的质量比木材的质量减小 D、铜丝在空气中加热,生成物的质量比原来铜丝的质量增大11. 下列各组中的两种物质混合,充分搅拌后,不能得到溶液的是( )A、碘和汽油 B、碘和酒精 C、高锰酸钾和汽油 D、高锰酸钾和水12. 如图为四种原子的结构示意图,其中化学性质相似的一组是( )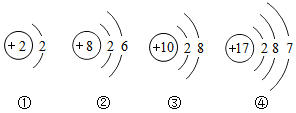 A、①和② B、①和③ C、②和③ D、③和④13. 下列用品中,主要由合成材料制成的是( )A、尼龙袜 B、纯棉裤 C、不锈钢碗 D、蚕丝被14. 某矿泉水的矿物质成分主要含钙、钾等。这里的“钙、钾”指的是( )A、原子 B、分子 C、元素 D、单质15. 制作包子、蛋糕所用发酵粉的主要成分含有碳酸氢钠。碳酸氢钠的俗称是( )A、小苏打 B、苏打 C、苛性钠 D、火碱16. 如图是某化学反应的微观示意图,其中相同的球代表同种原子。下列说法正确的是( )
A、①和② B、①和③ C、②和③ D、③和④13. 下列用品中,主要由合成材料制成的是( )A、尼龙袜 B、纯棉裤 C、不锈钢碗 D、蚕丝被14. 某矿泉水的矿物质成分主要含钙、钾等。这里的“钙、钾”指的是( )A、原子 B、分子 C、元素 D、单质15. 制作包子、蛋糕所用发酵粉的主要成分含有碳酸氢钠。碳酸氢钠的俗称是( )A、小苏打 B、苏打 C、苛性钠 D、火碱16. 如图是某化学反应的微观示意图,其中相同的球代表同种原子。下列说法正确的是( ) A、生成物含有四种物质 B、该反应属于置换反应 C、参加反应两种物质的微粒个数比为1∶1 D、反应前后分子种类部分改变,原子种类均改变17. 将一定量的锌粉加入到盛有MgSO4和CuSO4混合溶液的烧杯中,充分反应后过滤,向滤渣中滴入稀盐酸,有气泡产生。下列说法正确的是( )A、滤渣中一定含有Mg和Cu,可能含有Zn B、滤渣中一定含有Zn和Cu,可能含有Mg C、滤液中一定含有ZnSO4和MgSO4 , 一定不含CuSO4 D、滤液中一定含有ZnSO4和MgSO4 , 可能含有CuSO418. 下列推理正确的是( )A、青少年缺钙会患佝偻病,所以青少年一定要无限量吃补钙剂 B、碱溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定是碱溶液 C、催化剂在反应前后质量不变,则反应前后质量不变的物质一定是催化剂 D、单质只含一种元素,所以只含一种元素的纯净物一定是单质19. 在pH=2的溶液中,下列离子能大量共存的是( )A、Ba2+、K+、OH-、 B、Na+、Cu2+、Cl-、 C、K+、、、Cl- D、Zn2+、Na+、、20. 现有NaOH和BaCl2的混合溶液,向其中逐滴加入稀硫酸,生成沉淀质量与加入稀硫酸质量的变化关系如图所示。下列说法不正确的是( )
A、生成物含有四种物质 B、该反应属于置换反应 C、参加反应两种物质的微粒个数比为1∶1 D、反应前后分子种类部分改变,原子种类均改变17. 将一定量的锌粉加入到盛有MgSO4和CuSO4混合溶液的烧杯中,充分反应后过滤,向滤渣中滴入稀盐酸,有气泡产生。下列说法正确的是( )A、滤渣中一定含有Mg和Cu,可能含有Zn B、滤渣中一定含有Zn和Cu,可能含有Mg C、滤液中一定含有ZnSO4和MgSO4 , 一定不含CuSO4 D、滤液中一定含有ZnSO4和MgSO4 , 可能含有CuSO418. 下列推理正确的是( )A、青少年缺钙会患佝偻病,所以青少年一定要无限量吃补钙剂 B、碱溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定是碱溶液 C、催化剂在反应前后质量不变,则反应前后质量不变的物质一定是催化剂 D、单质只含一种元素,所以只含一种元素的纯净物一定是单质19. 在pH=2的溶液中,下列离子能大量共存的是( )A、Ba2+、K+、OH-、 B、Na+、Cu2+、Cl-、 C、K+、、、Cl- D、Zn2+、Na+、、20. 现有NaOH和BaCl2的混合溶液,向其中逐滴加入稀硫酸,生成沉淀质量与加入稀硫酸质量的变化关系如图所示。下列说法不正确的是( ) A、滴至a点时,溶液中可能只有一个化学反应进行 B、滴至b点时,溶液中一定不含BaCl2 C、滴至b点时,溶液中的pH一定等于7 D、滴至c点时,溶液的pH可能等于7,也可能大于7或小于7
A、滴至a点时,溶液中可能只有一个化学反应进行 B、滴至b点时,溶液中一定不含BaCl2 C、滴至b点时,溶液中的pH一定等于7 D、滴至c点时,溶液的pH可能等于7,也可能大于7或小于7二、填空题
-
21. 请用化学符号填空。(1)、碳元素 ;(2)、2个磷原子 ;(3)、2个水分子 ;(4)、亚铁离子 ;(5)、酒精 。22. 请用物质的序号填空:
①氮气 ②氯化钠 ③活性炭 ④石墨 ⑤明矾
(1)、用作冰箱除味剂的是;(2)、可作保护气的是;(3)、可用于制铅笔芯的是;(4)、净化水时可作絮凝剂的是;(5)、家庭厨房常用的调味品是。23. 化学科学的发展增进了人类对资源和能源的认识和利用,促进了社会的发展。请回答下列问题:(1)、铜丝、铝丝常用作导线,是因为它们具有良好的延展性和。(2)、高铁让人们出行更加便捷,高铁建设中架设钢铁桥梁所用的钢材,其表面刷漆可以有效防止铁与空气中的和水同时接触而生锈。(3)、常用作保险丝的武德合金其熔点比组成它的纯金属的熔点。(4)、石油、天然气属于(填“可再生”或“不可再生”)能源。其中天然气的主要成分是。(5)、为了山更青天更蓝,我们应该提倡使用清洁能源。以下属于清洁能源的是(填序号)。①太阳能 ②煤 ③风能
24. “发展杂交水稻,造福世界人民”是袁隆平院士毕生最大的追求。(1)、大米富含六大营养素中的。(2)、水稻适宜在接近中性的土壤里生长。小丽同学用玻璃棒蘸取某块农田土壤待测液滴在上,与标准比色卡比较得出pH=4。如果要种植水稻,可用来中和改良该土壤。(3)、水稻的种植常施用化肥,为了增强水稻抗病虫害和抗倒伏能力,需要施加的化肥种类是肥。(4)、为防止污染空气,稻草不能就地焚烧。若不慎有稻草燃烧起来可以用水扑灭,其主要灭火原理是。25. 如图是甲、乙两种固体物质的溶解度曲线。请回答下列问题: (1)、甲、乙两种物质的溶解度受温度影响较小的是。(2)、在℃时,甲、乙两物质的溶解度相等。(3)、t2℃时,要使40g甲物质完全溶解至少需要水的质量为g。(4)、t2℃时,将70g甲的饱和溶液降温到t1℃,析出甲固体物质的质量为g。(5)、t2℃时,甲物质在a、b两点对应的溶液溶质质量分数关系为:ab(填“=”、“>”或“<”)。
(1)、甲、乙两种物质的溶解度受温度影响较小的是。(2)、在℃时,甲、乙两物质的溶解度相等。(3)、t2℃时,要使40g甲物质完全溶解至少需要水的质量为g。(4)、t2℃时,将70g甲的饱和溶液降温到t1℃,析出甲固体物质的质量为g。(5)、t2℃时,甲物质在a、b两点对应的溶液溶质质量分数关系为:ab(填“=”、“>”或“<”)。三、综合题
-
26. 氯化钙在工业上有广泛的用途。工业上以石灰石(含有SiO2、Fe2O3等杂质)为原料,生产氯化钙的流程如图所示。(注:SiO2不溶于水也不与酸反应)

请回答下列问题:
(1)、操作Ⅰ、Ⅱ的名称是 , 此操作在实验室里需要用到多种仪器,其中玻璃棒的作用是。(2)、调节pH至中性是为了除去溶液2中的(填离子名称)。(3)、SiO2中硅、氧元素的质量比为(填最简整数比)。(4)、写出氧化铁与稀盐酸反应的化学方程式。27. A~H为初中化学常见的物质,其中A为酸,C为纯碱,F为黑色固体,H是既不溶于水也不溶于酸且含有两种元素的白色沉淀。它们之间的关系如图所示(图中“—”表示反应关系,“→”表示转化关系,反应条件、部分反应物和生成物已略)。请回答下列问题: (1)、写出C、H物质的化学式:C;H。(2)、G的物质类别不属于(填“氧化物”或“碱”)。(3)、写出B→H反应的化学方程式。(4)、D与E的反应属于基本反应类型中的。28. 请根据如图回答问题:
(1)、写出C、H物质的化学式:C;H。(2)、G的物质类别不属于(填“氧化物”或“碱”)。(3)、写出B→H反应的化学方程式。(4)、D与E的反应属于基本反应类型中的。28. 请根据如图回答问题: (1)、写出标有序号仪器的名称:①;②。(2)、实验室用高锰酸钾固体制取氧气的化学方程式为;若要收集干燥的氧气,应选用装置(填“A”、“B”或“C”)。(3)、装置D可以用来测量生成CO2的体积,其中在水面上放一层植物油的目的是。(4)、收集CO2时,用燃着的木条来验满,是利用CO2的化学性质。(5)、NH3是一种碱性气体,干燥时不能选用作干燥剂(填“浓硫酸”或“生石灰”)。29. 某化学兴趣小组同学向盛有KOH溶液的烧杯中通入足量的CO2时,未看到明显的实验现象。(1)、同学们对KOH与CO2能否反应进行如下实验探究。
(1)、写出标有序号仪器的名称:①;②。(2)、实验室用高锰酸钾固体制取氧气的化学方程式为;若要收集干燥的氧气,应选用装置(填“A”、“B”或“C”)。(3)、装置D可以用来测量生成CO2的体积,其中在水面上放一层植物油的目的是。(4)、收集CO2时,用燃着的木条来验满,是利用CO2的化学性质。(5)、NH3是一种碱性气体,干燥时不能选用作干燥剂(填“浓硫酸”或“生石灰”)。29. 某化学兴趣小组同学向盛有KOH溶液的烧杯中通入足量的CO2时,未看到明显的实验现象。(1)、同学们对KOH与CO2能否反应进行如下实验探究。实验操作
实验现象
实验结论
甲同学取烧杯中的少量液体置于试管中,滴加稀盐酸
KOH能与CO2反应
乙同学另取烧杯中的少量液体置于试管中,滴加硝酸钙溶液
有白色沉淀生成
请写出乙同学的试管中反应的化学方程式。
(2)、实验结束后,甲、乙两位同学将试管中的物质同时倒入同一个洁净的烧杯中,充分搅拌后静置,观察到烧杯内上层是无色溶液,下层有白色沉淀。小组同学将烧杯中的物质进行了过滤,并对滤液的成分进行探究。【提出问题】滤液中的溶质是什么呢?
【作出猜想】猜想一:KCl和KNO3
猜想二:KCl、KNO3和Ca(NO3)2
猜想三:KCl、KNO3和HCl
猜想四:。
(3)、【交流讨论】小组同学讨论后一致认为可以直接排除猜想 , 理由是。(4)、【实验验证】为验证滤液中溶质的成分,小组同学取烧杯中的少量滤液置于试管中,滴加氯化钙溶液,观察到有白色沉淀产生,则猜想正确。(5)、【反思拓展】在分析化学反应后溶液中溶质的成分时,除考虑生成物外还需考虑。四、计算题
-
30. 小亮同学为了测定某铜锌合金样品中锌的质量分数,往盛有200g稀硫酸的烧杯中依次加入该样品粉末(杂质不与硫酸反应),充分反应后,测得部分数据如下表:(反应的化学方程式为:)
实验次数
第一次
第二次
第三次
第四次
铜锌合金样品质量/g
10
10
10
10
烧杯中物质总质量/g
209.8
X
229.4
239.4
请回答:
(1)、表中X的数值为;(2)、该铜锌合金样品中锌的质量分数为;(3)、求所用稀硫酸的溶质质量分数(写出计算过程,结果精确到0.1%)。