山东省烟台市芝罘区(五四制)2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-02-28 类型:期末考试
一、单选题
-
1. 青少年的健康问题日益引起人们重视。某同学某天中午的食谱:米饭、回锅肉、炸鸡块、牛奶,从营养均衡的角度分析,还需要补充的食物是( )A、蒸蛋 B、清蒸鱼 C、炒芹菜 D、馒头2. 人体健康离不开化学。下列叙述不正确的是( )A、摄入过多油脂易引发肥胖和心脑血管疾病,因此不能食用过量油脂类食物 B、用甲醛浸泡水产品,会破坏蛋白质结构,使其变质,因此甲醛对人体健康有严重危害 C、青少年因缺钙会患佝偻病和发育不良,可食用奶制品等含钙丰富的食物 D、吸烟有害健康,但吸电子烟对健康无害3. 北斗系统的全面建成彰显了中国航天的力量。在航天科技中运用了大量金属材料,下列有关金属材料的说法正确的是( )A、纯金属的熔点一般比它们组成合金的熔点更低 B、金属单质在常温下都是固体 C、金属变成合金后,内部的组成和结构发生变化 D、合金中一定只含金属元素4. 汽车尾气是城市空气主要污染源,每年9月22日是世界“无车日”。汽车使用燃料通常为汽油或柴油(主要含C、H元素,基本不含N元素),燃料与吸入的空气在发动机内反应,产生的尾气中含有CO、NO等有害气体。目前汽车尾气处理系统中可安装催化转化器,尾气中的CO和NO在催化剂的作用下发生反应:2CO+2NON2+2CO2。下列相关说法不正确的是( )A、尾气处理时CO发生了还原反应 B、尾气外理反应前后分子的数目发生了改变 C、由上述资料推知氮气和氧气在一定条件下也能反应 D、减少尾气污染还可通过改进发动机的燃烧方式使燃料充分燃烧5. 近日,《写真地理》杂志上一篇“熟鸡蛋返生孵小鸡”的论文在网上引发热议,下列说法不正确的是( )A、鸡蛋中蛋清的主要成分是蛋白质 B、人体摄入的蛋白质在胃肠道里与水反应生成氨基酸,氨基酸全部被氧化放出能量供人体活动所需 C、鸡蛋煮熟后,因加热破坏了蛋白质的结构,导致蛋白质的性质发生了改变 D、“熟鸡蛋返生孵小鸡”明显违背科学常识,是伪科学6. 下列关于溶液的叙述正确的是( )A、任何溶液中只可能含有一种溶质 B、溶液一定是均一、稳定的混合物 C、氯化钠的饱和溶液是质量分数最大的溶液 D、一定温度下,硝酸钾的饱和溶液加水稀释后,溶解度减小7. 农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如下图所示。下列说法不正确的是( )
 A、实验操作顺序为④②①⑤③ B、②中需称量NaCl的质量为16.0g C、选用100mL量筒量取所需水的体积 D、用量筒量取水时仰视读数所得溶液的溶质质量分数偏大8. 下列物质长时间露置于空气中,质量会减轻的是(不考虑水分蒸发)( )A、固体氢氧化钠 B、浓硫酸 C、石灰水 D、浓盐酸9. 及时对知识进行分类归纳,是一种重要的学习方法。下面是小洁同学以连线方式对相关主题知识进行归纳的情况,其中完全正确的是( )
A、实验操作顺序为④②①⑤③ B、②中需称量NaCl的质量为16.0g C、选用100mL量筒量取所需水的体积 D、用量筒量取水时仰视读数所得溶液的溶质质量分数偏大8. 下列物质长时间露置于空气中,质量会减轻的是(不考虑水分蒸发)( )A、固体氢氧化钠 B、浓硫酸 C、石灰水 D、浓盐酸9. 及时对知识进行分类归纳,是一种重要的学习方法。下面是小洁同学以连线方式对相关主题知识进行归纳的情况,其中完全正确的是( )A.化学与健康
人体缺氟—会引起龋齿
人体缺锌—会影响人体发育
B.物质的性质与用途
氢氧化钠能中和酸—可治疗胃酸过多
食盐有咸味—可用作调味品
C.安全常识
误服少量重金属溶液—立即喝鲜牛奶
发霉的花生米—可以洗洗食用
D.化学与能源
天然气、风能、太阳能—可以再生的绿色能源
干电池—化学能转化为电能的装置
A、A B、B C、C D、D10. 除去下列各物质中的少量杂质,所选用的试剂和方法均正确的是( )编号
物质
杂质
试剂
除杂操作方法
A
CuO
C(木炭)
足量稀盐酸
过滤、洗涤、干燥
B
CaCl2溶液
HCl
过量CaCO3粉末
过滤
C
CO2
CO
O2
点燃
D
NaNO3溶液
NaCl
过量AgNO3溶液
过滤
A、A B、B C、C D、D11. 归纳推理是化学学习中常用的思维方法,下列推理正确的是( )A、酸性溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的溶液一定呈酸性 B、中和反应生成盐和水,所以生成盐和水的反应都是中和反应 C、常温下,pH<7的溶液显酸性,因此pH<7的雨水一定都是酸雨 D、碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐12. 将一定质量的锌粉、铁粉混合物加入到CuSO4溶液中,充分反应后过滤,得到滤渣和滤液,下列有关分析不正确的是( )A、若滤液为无色,则可以证明锌的金属活动性大于铜 B、若滤液为有色溶液,则滤液中至少含有2种金属离子 C、若向滤渣中加入稀盐酸没有气泡产生,则滤液中可能含有三种溶质 D、若向滤渣中加入稀盐酸有气泡产生,则滤渣中一定含有铜、铁、锌13. 图像能直观体现化学中的各种变化关系,加深对化学知识的理解。下列图像能正确表示对应叙述的有( )A、向氢氧化钠溶液中加水稀释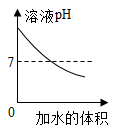 B、向一定量的盐酸和硫酸钠的混合溶液中逐滴加入氢氧化钡溶液
B、向一定量的盐酸和硫酸钠的混合溶液中逐滴加入氢氧化钡溶液  C、电解水生成氢气和氧气的质量与反应时间的关系
C、电解水生成氢气和氧气的质量与反应时间的关系 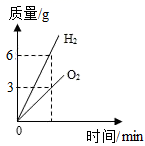 D、向等质量的Zn、Fe中滴加等浓度等质量的稀盐酸
D、向等质量的Zn、Fe中滴加等浓度等质量的稀盐酸  14. 将20g镁、铁的金属混合物加入到一定质量的稀硫酸中,恰好完全反应后,经测定溶液质量增加了19g,将反应后的溶液蒸干,得到固体的质量为( )A、39g B、60g C、68g D、73g
14. 将20g镁、铁的金属混合物加入到一定质量的稀硫酸中,恰好完全反应后,经测定溶液质量增加了19g,将反应后的溶液蒸干,得到固体的质量为( )A、39g B、60g C、68g D、73g二、多选题
-
15. 如图是a、b、c三种固体物质的溶解度曲线,下列分析正确的是( )
 A、t1℃时a、c两物质溶液中溶质的质量分数相等 B、t2℃时,物质a的100g饱和溶液中含有25g物质a C、t2℃时,分别将a、b、c的饱和溶液降温至t1℃,溶质质量分数关系是b>a>c D、t2℃时向50g水中加入15g物质b充分搅拌,所得溶液质量一定小于65g
A、t1℃时a、c两物质溶液中溶质的质量分数相等 B、t2℃时,物质a的100g饱和溶液中含有25g物质a C、t2℃时,分别将a、b、c的饱和溶液降温至t1℃,溶质质量分数关系是b>a>c D、t2℃时向50g水中加入15g物质b充分搅拌,所得溶液质量一定小于65g三、填空题
-
16. “杂交水稻之父”袁隆平先生,为解决世界粮食问题做出了卓越的贡献。(1)、稻谷被加工成大米。从营养角度考虑,大米能给人类提供的主要营养素为____(填序号)。A、蛋白质 B、糖类 C、油脂 D、无机盐(2)、在水稻生长过程中,现部分水稻有叶片发黄和倒伏现象,需要及时施加的一种肥料是____(填序号)。A、KCl B、NH4NO3 C、KNO3 D、NH4H2PO4(3)、在农业生产中,改良酸性土壤(硫酸型酸雨所致),通常加入(写物质俗称),以中和其酸性,反应的化学方程式为。(4)、使用硝酸铵肥料时,不能与熟石灰混合使用,原因是 (用化学方程式解释)。该肥料包装袋的主要成分是聚氯乙烯塑料,该包装袋属于材料(填“金属材料”或“无机非金属材料”或“有机高分子材料”或“复合材料”);该包装袋随意丢弃会带来的环境问题是(答案合理即可)。该硝酸铵化肥包装袋上注明含氮量为33.25%,则该肥料的纯度是(杂质不含氮元素)。
四、综合题
-
17. 氯化钠是必不可少的生活用品,更是重要的化工原料。(1)、工业上用反渗透膜法淡化海水,其原理是利用海水中各成分的不同分离出淡水。分离淡水后剩余的溶液,可以进行海水晒盐,海水晒盐是通过(填“蒸发结晶”或“降温结晶”)的方法获取食盐。(2)、在工业生产中,可以利用海水晒盐后的苦卤制镁,下图是从海水中提取镁的简单流程。

反应①的化学方程式是。反应②的属于反应(基本反应类型)。海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同。
(3)、氯化钠是生活中常见的盐,为除去某粗盐水中的MgCl2、Na2SO4、CaCl2杂质,得到NaCl溶液,某化学小组设计了如下实验方案。
①操作1相当于实验室中的操作;
②加入过量试剂1的目的是;
③沉淀3是(用化学式表示);
④加稀盐酸除去的离子是(填离子符号)。
(4)、抗日战争期间,我国著名制碱专家侯德榜打破西方国家对制碱技术的垄断,创立“侯氏制碱法”,利用氯化钠制取纯碱。
①氨气通入饱和食盐水中,可制成饱和氨盐水(氨气极易溶于水)。氨盐水比食盐水更容易吸收二氧化碳的原因是。
②图中得到碳酸氢钠晶体反应的方程式是。
③该流程中的副产品是 , 能够循环利用的物质有(答一种,水除外)。
18. 铜是人类认识并应用最早的金属之一,我国有着使用铜器的悠久历史。(1)、铜制导线,利用了铜的物理性质是 , 青铜古称“吉金”是金属冶铸史上最早出现的合金,青铜的硬度比纯铜(填“大”或“小”)。(2)、生活中铜制品长期露置在潮湿空气中会锈蚀,生成“铜绿”【化学式为Cu2(OH)2CO3】。为从某锈蚀的铜样品中回收铜并制得硫酸锌,取该铜样品(除含有铜、锌和铜绿外,不含其它物质),进行如下操作,请回答下列问题:【查阅资料】Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O

①气体a的成分是(填化学式,下同),固体M是。
②加入固体M后的反应现象是(答完整)。
③写出Ⅲ中发生反应的化学方程式 , 该反应的反应类型是。
19. 为探究某化工厂固体废物的成分,以便回收有用物质,除掉有害物质。已知固体废物可能含有NaCl、KCl、Na2CO3、K2SO4、NH4NO3、MgSO4、FeCl3中的一种或几种,通过以下探究回答下列问题。探究一:取固体废物,加入过量NaOH溶液加热,得到无色溶液A和一种能使红色石蕊试纸变蓝的气体甲。
探究二:另取固体废物,加水溶解,加入适量硝酸钡溶液,得到无色溶液B和白色沉淀,向沉淀中加入足量稀盐酸,沉淀全部溶解,得到气体乙。
探究三:另取固体废物,74.5g加足量的水溶解,加入足量的稀硝酸后,再加入足量的硝酸银溶液,反应后过滤,将沉淀洗涤干燥后称量143.5g。
(1)、气体甲的化学式为。(2)、生成气体乙的化学方程式为。(3)、由探究一、探究二可以获得的结论是:原固体废物中一定存在的物质有。一定不存在的物质是 , 可能存在的物质是。(4)、探究三中,稀硝酸的作用是 , 由探究三可以得到的结论是。20. 某实验小组为探究酸的化学性质,同学们完成了如下图所示的实验。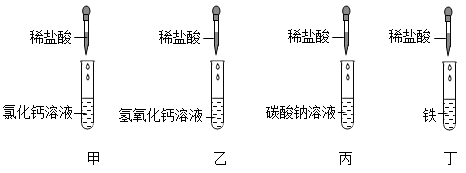 (1)、图甲两种物质不发生复分解反应的原因是。(2)、图乙中,要证明两种物质发生化学反应,最好加入的指示剂是 , 该反应的微观实质是。(3)、图丙反应的现象是。(4)、图丁反应的化学方程式是。(5)、实验完后,同学们将甲乙丙三支试管的液体倒入大烧杯中,滴入酚酞试液后,得到无色溶液,对于无色溶液的成分(酚酞除外),同学们提出了以下猜想:
(1)、图甲两种物质不发生复分解反应的原因是。(2)、图乙中,要证明两种物质发生化学反应,最好加入的指示剂是 , 该反应的微观实质是。(3)、图丙反应的现象是。(4)、图丁反应的化学方程式是。(5)、实验完后,同学们将甲乙丙三支试管的液体倒入大烧杯中,滴入酚酞试液后,得到无色溶液,对于无色溶液的成分(酚酞除外),同学们提出了以下猜想:猜想一:氯化钠、氯化钙、
猜想二:氯化钠、氯化钙、稀盐酸
猜想三:氯化钠、氯化钙、氢氧化钠
猜想四:氯化钠、氯化钙、碳酸钠
【讨论】小明认为猜想三不正确,理由是。小红认为猜想四不正确,她的理由之一是(用化学方程式表示)。
(6)、【实验】小明取少量液体于试管中,加入硝酸银溶液,产生白色沉淀,证明猜想二成立。小红对此提出了疑义,她的理由是。小红设计了实验证明了猜想二正确。实验步骤是取少量氢氧化铜固体于试管中,加入少量滤液,观察到的实验现象是 , 证明猜想二成立。五、科学探究题
-
21. 今天是化学实验室开放日,小明带着一包脱氧剂和一包食品干燥剂走进实验室,和小组同学一起开始了令人兴奋地探究之旅(忽略实验过程中空气的影响)。
【查阅资料】脱氧剂成分是铁粉、碳粉、碳酸钠、氯化钠;食品干燥剂的成分是生石灰。
(1)、探究活动一:脱氧剂脱氧原理【进行实验】
①取适量脱氧剂于大试管中,加足量的水振荡,充分溶解后过滤,得到滤液A和滤渣甲;
②向滤渣甲中加入足量稀盐酸,观察到有气泡产生,得到黄色溶液,溶液底部有黑色不溶物。
【得出结论】脱氧剂脱氧的原理是铁粉与发生了化学反应,生成铁锈。铁锈的主要成分是氧化铁,写出得到黄色溶液的化学方程式。
(2)、探究活动二:探究食品干燥剂是否变质【进行实验】①取一包干燥剂放入小烧杯中,加入适量的水,充分搅拌后,用手触摸烧杯外壁,发烫,过滤,得到滤液B和滤渣乙;
②向滤渣乙中加入足量的稀盐酸,可观察到固体全部溶解,有气泡产生。
【得出结论】该干燥剂(选填“完全”或“部分”或“没有”)变质。
(3)、探究活动三:探究溶液混合后溶质的成分小组同学将上述实验中的滤液A和滤液B倒入废液缸中,观察到有白色沉淀生成,过滤后得到滤液C,他们对C中溶质的成分进行了探究。
【提出猜想】
猜想一:;精想二:NaCl、NaOH、Na2CO3;猜想三:NaCl、NaOH、Ca(OH)2
【进行实验】小明按照自己设计的方案进行了如下实验:
实验步骤
实验现象
实验结论
①取少量滤液C于试管中,加入足量的氯化钡溶液
无明显现象
猜想不正确
②继续向步骤①所得溶液中通入二氧化碳
有白色沉淀生成
猜想三正确
【反思评价】小组同学经过讨论,一致认为根据步骤②的现象不足以证明猜想三是正确的,理由是。
(4)、小明经过认真思考后,对步骤②进行了修改,并做了下面的实验,最终得出了正确的结论,记录如下。请你完善实验报告。实验步骤
实验现象
实验结论
有白色沉淀生成
猜想三正确
22. 化学兴趣小组的同学对乙醇燃烧后的产物进行了探究。【提出问题】乙醇燃烧后的产物是什么?
【查阅资料】无水硫酸铜为白色粉末,遇水会变蓝。
(1)、【做出猜想】猜想一:产物中含有CO、H2O; 猜想二:产物中含有CO2、H2O;猜想三:产物中含有。
(2)、【进行实验】同学们设计了如图的实验:检查装置气密性后,将乙醇燃烧的产物依次通过如图所示的装置进行验证。(部分夹持固定装置省略,B、D、G装置中均为澄清的石灰水)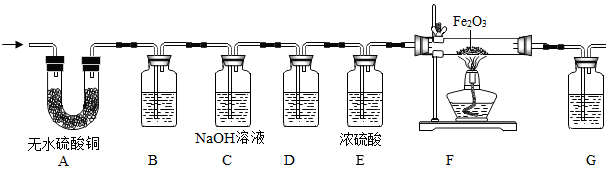
实验前,待 , 再点燃装置F中的酒精灯对固体进行加热。
(3)、装置C的作用是 , 装置D的作用是。(4)、【解释与结论】经过实验,同学们认为猜想三成立,则实验中能观察到的现象有(请回答完整);装置F中发生反应的化学方程式为。(5)、【反思与评价】乙同学发现该实验的设计中有一个明显缺陷,该缺陷是。实验结束后,由于小丽同学的操作步骤不当造成了硬质玻璃管破裂。为了避免此事故再次发生,同学们对该装置进行了改进,你认为他们的改进是。六、计算题
-
23. 实验室开放日,同学们用稀盐酸和石灰石反应制取二氧化碳(石灰石中的杂质既不溶于水也不和酸反应),反应结束后,同学们对反应后溶液的成分进行了如下探究:取反应后的溶液50g于烧杯中,逐滴滴入碳酸钠溶液,产生的气体总质量、沉淀总质量与滴入碳酸钠溶液总质量的关系如下表所示:
碳酸钠溶液总质量/g
25.0
50.0
75.0
100.0
125.0
150.0
175.0
200.0
气体总质量/g
1.1
2.2
2.2
2.2
2.2
2.2
2.2
2.2
沉淀总质量/g
0
0
2.5
5.0
m
n
9.0
9.0
 (1)、所取的反应后50g溶液中溶质是。(2)、表中n=。(3)、如图中w点的横坐标是。(4)、所用碳酸钠溶液溶质的质量分数是?(写出计算过程)
(1)、所取的反应后50g溶液中溶质是。(2)、表中n=。(3)、如图中w点的横坐标是。(4)、所用碳酸钠溶液溶质的质量分数是?(写出计算过程)
-
-