江西省吉安市峡江县2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-02-28 类型:期末考试
一、单选题
-
1. 古诗词是中华民族的文化瑰宝,下列古诗词中对划线对象变化的描述属于化学变化的是( )A、一味黑时犹有骨,十分红处便成灰。([清]徐宗干《咏炭》) B、河上姹女(水银),灵而最神,得火则飞 , 不见埃尘。([汉]魏伯阳《参同契》) C、臣心一片磁针石,不指南方不肯休。([宋]文天祥《扬子江》) D、落红(落花)不是无情物 , 化作春泥更护花。([清]龚自珍《己亥杂诗》)2. 世卫组织(WHO)发表声明称,地塞米松(C22H29FO3)可挽救新冠肺炎重症患者生命。下列说法正确的是( )A、地塞米松属于氧化物 B、地塞米松由4种元素组成 C、地塞米松中氢元素的质量分数最大 D、地塞米松中碳元素与氧元素的质量比为22:53. 高温超导物质(Y2Ba4Cu6O13)是以YmOn、BaO和CuO为原料,经研磨烧结而成,此过程中所有元素的化合价均不变,则Y元素的化合价是( )A、+3 B、+2 C、+4 D、+54. 煤气中添加少量有特殊臭味的乙硫醇(C2H5SH),可以提醒人们预防煤气泄露。乙硫醇在煤气燃烧过程中也可充分燃烧,其反应方程式为2C2H5SH+9O2 4CO2+6H2O+2X,则 X 的化学式为:( )A、SO2 B、SO3 C、CO D、H2SO4。5. 下列各图所示装置的气密性检查中,漏气的是( )A、
 B、
B、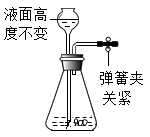 C、
C、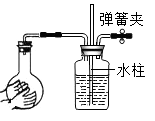 D、
D、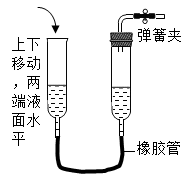 6. 为除去物质中的杂质(括号内为杂质),下列说法不正确的是( )
6. 为除去物质中的杂质(括号内为杂质),下列说法不正确的是( )物 质
选 用 试 剂 及 操 作 方 法
A
Cu粉(Fe)
加入足量的稀硫酸,在充分反应后过滤,干燥
B
CO(CO2)
通入足量的氢氧化钠溶液,充分反应后干燥
C
N2(O2)
灼热的铜网
D
FeSO4溶液(CuSO4)
加入过量的锌粉,充分反应后过滤
A、A B、B C、C D、D7. 如图为治理汽车尾气反应的微观示意图,下列有关说法正确的是( )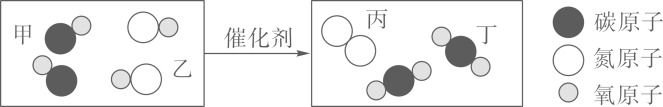 A、图中只有两种氧化物 B、该反应属于置换反应 C、相对分子质量最大的是NO D、生成丙和丁的质量比为7:228. 在一个密闭容器中,有a、b、c、d四种物质,反应前各物质的质量关系如下图刻度纸所示(例如:d的质量为2g)。
A、图中只有两种氧化物 B、该反应属于置换反应 C、相对分子质量最大的是NO D、生成丙和丁的质量比为7:228. 在一个密闭容器中,有a、b、c、d四种物质,反应前各物质的质量关系如下图刻度纸所示(例如:d的质量为2g)。 在一定条件下发生反应,反应结束后,再次测得各物质的质量变化,并通过刻度的移动来表示,且记录在同一张刻度纸上:刻度线Ⅰ向右移动9格;刻度线Ⅱ向左移动8格;刻度线Ⅲ向左移动8格。下列说法正确的是( )A、反应结束后c的质量为14g B、该反应可能为置换反应 C、a、b变化的质量比一定为9:17 D、a、d的相对分子质量之比一定为9:89. A,B,C三种物质各15 g,当它们相互充分反应后,生成30 g新物质D。若再增加10 g C,它们又继续反应到完成时,A与C恰好消耗完毕。则参加反应的A与B的质量比是( )A、2∶3 B、2∶1 C、3∶2 D、1∶110. 下列实验设计能达到实验目的的是( )
在一定条件下发生反应,反应结束后,再次测得各物质的质量变化,并通过刻度的移动来表示,且记录在同一张刻度纸上:刻度线Ⅰ向右移动9格;刻度线Ⅱ向左移动8格;刻度线Ⅲ向左移动8格。下列说法正确的是( )A、反应结束后c的质量为14g B、该反应可能为置换反应 C、a、b变化的质量比一定为9:17 D、a、d的相对分子质量之比一定为9:89. A,B,C三种物质各15 g,当它们相互充分反应后,生成30 g新物质D。若再增加10 g C,它们又继续反应到完成时,A与C恰好消耗完毕。则参加反应的A与B的质量比是( )A、2∶3 B、2∶1 C、3∶2 D、1∶110. 下列实验设计能达到实验目的的是( )选项
A
B
C
D
实验
目的
红磷燃烧测定空气中氧气的含量
验证面粉在一定条件下能爆炸
证明CH4燃烧生成二氧化碳和水
验证质量守恒定律
实验
设计



 A、A B、B C、C D、D
A、A B、B C、C D、D二、选择填充题
-
11. 用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是

A.甲中逸出的气体只含CO2
B.乙中液体变红,说明此时溶液显酸性
C.加热后红色不褪去,说明碳酸受热不分解
D.欲达到实验目的,可将盐酸改为
12. 利用如图所示实验装置模拟工业炼铁。下列说法正确的是
A.实验时应先点燃酒精灯后通CO
B.可用NaOH溶液吸收尾气中的CO
C.充分加热,a处固体由红色变为黑色
D.b处可用检验生成的CO2
13. 某实验小组在探究金属的化学性质时,得到金属与酸反应制取氢气的质量关系(见图),请根据图象信息判断,下列说法正确的是。
A 四种金属与酸反应的速率:Al>Mg>Fe>Zn
B 四种金属的活动性顺序:Mg>Al>Zn>Fe
C 同质量的四种金属与足量酸反应得到氢气的质量:Mg>Al>Fe>Zn
D 同质量的Al、Mg、Fe、Zn四种金属与足量酸反应得到氢气的质量比:。
三、填空题
-
14. 请用合适的化学用语填空:(1)、“西气东输”的“气”是指。(2)、2个氢原子。(3)、氟的原子结构示意图为
 , 氟离子的符号为 , 则单氟磷酸钠(Na2PO3F)中磷元素的化合价为。 (4)、保持二氧化硫化学性质的最小微粒。(5)、由氧和铝两种元素组成的化合物的化学式。15. 建立宏观、微观和符号之间的相互联系是化学学科的特点。请根据信息回答下列问题:
, 氟离子的符号为 , 则单氟磷酸钠(Na2PO3F)中磷元素的化合价为。 (4)、保持二氧化硫化学性质的最小微粒。(5)、由氧和铝两种元素组成的化合物的化学式。15. 建立宏观、微观和符号之间的相互联系是化学学科的特点。请根据信息回答下列问题:
 (1)、图甲为粒子之间的转化关系图,其中①表示的是。(2)、图乙中D为某粒子的结构示意图,当X=时,该粒子是原子。(3)、由A、B形成的化合物的化学式为。16. 氯化铁(FeCl3)能腐蚀铜,工业依此生产镀铜线路板的流程如下、试回答:
(1)、图甲为粒子之间的转化关系图,其中①表示的是。(2)、图乙中D为某粒子的结构示意图,当X=时,该粒子是原子。(3)、由A、B形成的化合物的化学式为。16. 氯化铁(FeCl3)能腐蚀铜,工业依此生产镀铜线路板的流程如下、试回答: (1)、步骤②中发生了两个反应:2FeCl3+Fe=3FeCl2和。(2)、滤渣中有 , 步骤③中发生反应的化学方程式是。(3)、步骤③中,当加入稀盐酸,观察到时,说明滤渣只剩铜。(4)、步骤②③所得滤液中的FeCl2可与一种双原子分子的单质发生化合反应生成FeCl3 , 实现循环使用。该单质的化学式为。17. A﹣J都是初中化学常见的物质。其中B、E、H、J是单质。其余的均为化合物。气体C可用于灭火。它们相互间的转化关系如图所示(部分反应物、生成物及反应条件已略去)。
(1)、步骤②中发生了两个反应:2FeCl3+Fe=3FeCl2和。(2)、滤渣中有 , 步骤③中发生反应的化学方程式是。(3)、步骤③中,当加入稀盐酸,观察到时,说明滤渣只剩铜。(4)、步骤②③所得滤液中的FeCl2可与一种双原子分子的单质发生化合反应生成FeCl3 , 实现循环使用。该单质的化学式为。17. A﹣J都是初中化学常见的物质。其中B、E、H、J是单质。其余的均为化合物。气体C可用于灭火。它们相互间的转化关系如图所示(部分反应物、生成物及反应条件已略去)。
请回答下列问题:
(1)、写出物质B的化学式:。(2)、反应①的其基本反应类型是。(3)、写出反应②的化学方程式:。(4)、“H红色固体J”的转化化学方程式:。18. 化学兴趣小组的同学欲用如图装置制取常见气体,请回答问题:
 (1)、写出图中有标号的仪器的名称:①。(2)、选用如图部分仪器和单孔橡皮塞(选填“能”或“不能”)完成用高锰酸钾制取氧气的实验,理由是。(3)、若用A、B和F组成气体发生装置,它可以用来制取的气体有(写出一种即可),该反应的化学方程式为。(4)、已知,乙炔是一种难溶于水、密度比空气略小的气体。实验室常用块状的电石(主要成分CaC2)和水在常温下反应制取乙炔(C2H2),同时生成氢氧化钙。该反应比较剧烈,且反应放出大量的热,若操作不当,会使反应容器发生炸裂。写出实验室制取乙炔的化学方程式。为了保证实验安全,你认为应该选用上述仪器中的(选填装置序号)等仪器组成发生装置; 若用G图装置来收集乙炔气体,则气体应从(填“e”或“f”)端通入。
(1)、写出图中有标号的仪器的名称:①。(2)、选用如图部分仪器和单孔橡皮塞(选填“能”或“不能”)完成用高锰酸钾制取氧气的实验,理由是。(3)、若用A、B和F组成气体发生装置,它可以用来制取的气体有(写出一种即可),该反应的化学方程式为。(4)、已知,乙炔是一种难溶于水、密度比空气略小的气体。实验室常用块状的电石(主要成分CaC2)和水在常温下反应制取乙炔(C2H2),同时生成氢氧化钙。该反应比较剧烈,且反应放出大量的热,若操作不当,会使反应容器发生炸裂。写出实验室制取乙炔的化学方程式。为了保证实验安全,你认为应该选用上述仪器中的(选填装置序号)等仪器组成发生装置; 若用G图装置来收集乙炔气体,则气体应从(填“e”或“f”)端通入。四、科学探究题
-
19. 碳还原氧化铜的实验装置如图甲、乙所示。
(提出问题)碳燃烧时可能生成CO2也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?
(1)、(作出猜想)猜想I:CO; 猜想Ⅱ:CO2; 猜想Ⅲ:。(2)、(设计方案)实验装置如图乙所示。打开K,缓缓通入干燥的氮气一段时间,关闭K,点燃酒精喷灯和酒精灯,充分反应后,熄灭酒精喷灯和酒精灯,打开K,再通入一段时间氮气。

方案一:从定性观察角度判断
实验时装置A处的现象是。
(3)、若B中无明显现象,D处的气体能点燃,则猜想(填序号)成立。(4)、方案二:从定量计算角度判断:取一定量碳粉和4g氧化铜的混合物进行实验,并测定表格中的四个数据:反应前的质量
反应后的质量
A(玻璃管+固体)
m1
m2
B+C(广口瓶+混合液)
m3
m4
若猜想Ⅱ成立,则理论上(m4-m3)(m1-m2)(填“>”“<”或“=”)。
(5)、若猜想Ⅲ成立且CuO全部转化成Cu,则参加反应的碳粉的质量m的取值范围是。(6)、(交流反思)实验开始前缓缓通入氮气的目的是。五、计算题
-
20. 某市石灰石资源丰富,某石灰厂为了测定某石灰石样品中CaCO3的质量分数,往盛有300g稀盐酸的烧杯中依次加入粉碎后的石灰石样品(杂质不与盐酸反应),充分反应后,实验数据记录如下:
实验次数
第一次
第二次
第三次
第四次
石灰石样品/g
25
15
10
5
烧杯中物质总质量/g
316.2
326.8
m
341.8
(1)、CaCO3中钙、碳、氧三种元素的质量比为多少;(写最简比)(2)、表中m=;(3)、求该石灰石样品中CaCO3的质量分数。(写出计算过程)
-