湖北省荆州市江陵县2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-02-28 类型:期末考试
一、单选题
-
1. 下列活动中没有发生化学变化的是( )A、烤肉 B、剪纸 C、酿酒 D、呼吸2. 下列物质是化合物的是( )A、铁粉 B、牛奶 C、石油 D、氯酸钾3. 下列灭火方法不正确的是( )A、油锅着火——用锅盖盖灭 B、森林着火——砍伐树木形成隔离带 C、酒精灯着火——用湿抹布盖灭 D、汽车油箱着火——用水浇灭4. 从微粒的角度分析,下列解释不正确的是( )A、水烧开后易把壶盖顶起——分子变大 B、花园里百花盛开,香气四溢——分子在不停运动 C、一氧化碳和二氧化碳的化学性质不同——分子不同 D、金刚石和石墨物理性质的差异很大——碳原子排列方式不同5. 下列实验操作正确的是( )A、取用高锰酸钾粉末
 B、点燃酒精灯
B、点燃酒精灯 C、检查气密性
C、检查气密性 D、加入大理石
D、加入大理石 6. 下列说法不正确的是( )A、氮气常用作保护气是因为氮气的化学性质不活泼 B、二氧化碳可以做气体肥料 C、天然气作燃料是利用了甲烷的助燃性 D、自热火锅的热量主要来自于氧化钙与水反应放出的热量7. 核污水中的氚是指核内有1个质子和2个中子的氢原子,下列示意图能符合题意表示氚原子结构的是( )
6. 下列说法不正确的是( )A、氮气常用作保护气是因为氮气的化学性质不活泼 B、二氧化碳可以做气体肥料 C、天然气作燃料是利用了甲烷的助燃性 D、自热火锅的热量主要来自于氧化钙与水反应放出的热量7. 核污水中的氚是指核内有1个质子和2个中子的氢原子,下列示意图能符合题意表示氚原子结构的是( ) A、
A、 B、
B、 C、
C、 D、
D、 8. 向硫酸铜溶液中加入一定质量的铝粉,充分反应后过滤,得蓝色滤液,并将滤渣晾干(不考虑操作中的损失)。下列说法正确的是( )A、滤液中只含有硫酸铝 B、滤渣的质量等于Al粉的质量 C、向滤渣中滴加稀盐酸,无气泡产生 D、发生反应的化学方程式为Al+CuSO4=Cu+AlSO49. 下列实验不能达到实验目的的是( )A、测定空气里氧气的含量
8. 向硫酸铜溶液中加入一定质量的铝粉,充分反应后过滤,得蓝色滤液,并将滤渣晾干(不考虑操作中的损失)。下列说法正确的是( )A、滤液中只含有硫酸铝 B、滤渣的质量等于Al粉的质量 C、向滤渣中滴加稀盐酸,无气泡产生 D、发生反应的化学方程式为Al+CuSO4=Cu+AlSO49. 下列实验不能达到实验目的的是( )A、测定空气里氧气的含量 B、证明铁、铜、银金属活动性
B、证明铁、铜、银金属活动性 C、探究铁生锈需要氧气
C、探究铁生锈需要氧气 D、证明燃烧需要氧气
D、证明燃烧需要氧气 10. 丙烷是液化石油气的主要成分之一,下列有关叙述正确的是( )
10. 丙烷是液化石油气的主要成分之一,下列有关叙述正确的是( ) A、丙烷的化学式为C3H6 B、丙烷由碳、氢原子构成 C、丙烷中氢元素的质量分数最大 D、丙烷中碳、氢元素质量比为9:211. 一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示,下列说法正确的是( )
A、丙烷的化学式为C3H6 B、丙烷由碳、氢原子构成 C、丙烷中氢元素的质量分数最大 D、丙烷中碳、氢元素质量比为9:211. 一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示,下列说法正确的是( )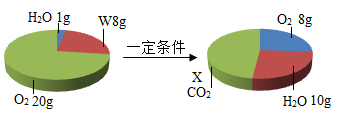 A、X为22 g B、W由碳、氢两种元素组成 C、8g W中氧元素的质量为4g D、该反应属于化合反应12. 某些含磷洗涤剂含有Na5P3O10,会使水中藻类等浮游生物过量繁殖而造成水体污染.Na5P3O10中磷元素的化合价是( )
A、X为22 g B、W由碳、氢两种元素组成 C、8g W中氧元素的质量为4g D、该反应属于化合反应12. 某些含磷洗涤剂含有Na5P3O10,会使水中藻类等浮游生物过量繁殖而造成水体污染.Na5P3O10中磷元素的化合价是( )
A、-2 B、+1 C、+4 D、+5二、填空题
-
13. 用化学用语填空:(1)、2个硅原子;(2)、a个氢氧根离子;(3)、七氧化二锰;(4)、构成氯化钠的粒子。14. 通过“碳捕捉”(捕捉空气中的二氧化碳)和“碳封存”(将二氧化碳封存起来)可以减少二氧化碳的排放,缓解全球气候变暖。(1)、碳捕捉
①脱碳法:煤燃烧前将水蒸气通过炽热的煤层,发生的反应之一为CO+H2OCO2+(请将化学方程式补充完整),然后在高压下将CO2进行分离捕集。
②吸收法:用石灰水进行化学吸收,该反应的化学方程式为。
(2)、碳封存①地质封存:将二氧化碳封存在地质层800m以下,使二氧化碳处于高密度的液态或超临界状态(气态和液态的共同体),用分子的观点解释这一过程。
②海洋封存:将捕获的二氧化碳直接注入深海,二氧化碳和水反应可以生成(写出物质的化学式)。
15. 某自来水的水源地是一个大型水库,小华同学开展了一次净化水的实践活动。请回答下列问题:(1)、对所取水样进行过滤,除了滤纸和如图提供选择的仪器外还需要的一种玻璃仪器是。 (2)、向滤液中加入活性炭,利用其性除去异味,再次过滤。(3)、为了检验所得滤液是否为硬水,取样加入 , 根据产生泡沫的多少进行判断。(4)、将所得滤液蒸馏得到蒸馏水,用如图所示装置电解水,请在方框内完成水电解过程的微观示意图。
(2)、向滤液中加入活性炭,利用其性除去异味,再次过滤。(3)、为了检验所得滤液是否为硬水,取样加入 , 根据产生泡沫的多少进行判断。(4)、将所得滤液蒸馏得到蒸馏水,用如图所示装置电解水,请在方框内完成水电解过程的微观示意图。
 16. 如图是氟元素在元素周期表中的信息和5种微粒的结构示意图,请回答:
16. 如图是氟元素在元素周期表中的信息和5种微粒的结构示意图,请回答: (1)、5种微粒共属于种元素;(2)、C所表示的元素位于元素周期表的第周期;(3)、C与E形成化合物的化学式为;(4)、氟原子的中子数为。
(1)、5种微粒共属于种元素;(2)、C所表示的元素位于元素周期表的第周期;(3)、C与E形成化合物的化学式为;(4)、氟原子的中子数为。三、综合题
-
17. A、B、C、D、E、X、Y均为初中化学常见物质,A和X为单质,B、C、Y为氧化物,Y为黑色物质,D不溶于水。请回答下列问题。
 (1)、X的化学式为。(2)、物质D和物质E的组成元素中含有相同的元素(填元素符号)。(3)、实验室用物质B和物质Y反应可以得到铜,该反应发生时观察到的现象为。(4)、反应③的化学方程式为。18. 实验室有如图下列装置,请根据要求回答问题:
(1)、X的化学式为。(2)、物质D和物质E的组成元素中含有相同的元素(填元素符号)。(3)、实验室用物质B和物质Y反应可以得到铜,该反应发生时观察到的现象为。(4)、反应③的化学方程式为。18. 实验室有如图下列装置,请根据要求回答问题:
 (1)、写出有标号仪器的名称:①。(2)、若用高锰酸钾制取氧气,选择的装置为 , 发生反应的化学方程式为。(3)、若用装置G收集二氧化碳气体,则二氧化碳从导管口(填“a”或“b”)进入。19. 某同学为了探究氧化铜(难溶于水)是否能作过氧化氢分解制取氧气的催化剂,设计实验如下:(1)、[实验一]实验目的:探究氧化铜是否能改变过氧化氢分解的速率。
(1)、写出有标号仪器的名称:①。(2)、若用高锰酸钾制取氧气,选择的装置为 , 发生反应的化学方程式为。(3)、若用装置G收集二氧化碳气体,则二氧化碳从导管口(填“a”或“b”)进入。19. 某同学为了探究氧化铜(难溶于水)是否能作过氧化氢分解制取氧气的催化剂,设计实验如下:(1)、[实验一]实验目的:探究氧化铜是否能改变过氧化氢分解的速率。①在试管中加入2mL 5%的过氧化氢溶液,将带火星的木条伸入试管中,观察现象。
带火星的木条没有明显变化
②取1g氧化铜粉末放入
带火星的木条复燃
结论:氧化铜能加快过氧化氢的分解速率。
(2)、[实验二]实验目的:。实验步骤
实验现象
待实验一第1步的试管中没有气泡时,重新加入2mL5%过氧化氢溶液,观察现象。
结论:氧化铜的化学性质在化学反应前后没有发生改变。
(3)、[实验三]实验目的:探究氧化铜的质量在化学反应前后有没有改变。在实验后,该同学将反应剩余物过滤、洗涤、干燥,再称量,得到黑色固体质量为1 g。
结论:氧化铜的在化学反应前后没有发生改变。
(4)、[实验结论]综上所述,证明了氧化铜是过氧化氢分解的催化剂。请写出该实验中过氧化氢分解反应的化学方程式:某同学画出如图,表示有、无催化剂时,生成物质量与反应时间的关系图,你认为是否正确?(填“正确”或“不正确”)

四、计算题
-
20. 某高钙片的使用说明书部分内容如图所示。取10片高钙片研磨成粉末,放入烧杯中,往烧杯中注入100g稀盐酸充分反应(稀盐酸足量,且高钙片中除碳酸钙外,其他成分不与稀盐酸反应生成气体),测得烧杯中物质的质量(m)与反应时间(t)之间的关系如图所示。

 (1)、写出碳酸钙与稀盐酸反应的化学方程式。(2)、反应后生成二氧化碳的质量为g;(3)、请据此计算高钙片中碳酸钙的质量分数?
(1)、写出碳酸钙与稀盐酸反应的化学方程式。(2)、反应后生成二氧化碳的质量为g;(3)、请据此计算高钙片中碳酸钙的质量分数?