湖北省黄石市大冶市2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-02-28 类型:期末考试
一、单选题
-
1. 下列物质的用途由它的物理性质决定的是( )A、液氧气于发射火箭 B、包装食品时充氮气以防腐 C、液氮用作制冷剂 D、氮气用于填充灯泡以延长寿命2. 近几年来,部分大城市出现雾霾天气,下列情况可能引起大气污染的是( )
①煤的燃烧;②工业废气的排放;③.动植物的呼吸;④.汽车尾气的排放。
A、①②④ B、②③④ C、①③④ D、①②③3. 规范操作是科学实验的基本要求。图所示的实验操作中正确的是( )A、 滴加液体
B、
滴加液体
B、 液体加热
C、
液体加热
C、 闻气味
D、
闻气味
D、 液体读数
4. 下表的探究实验中,“对问题的回答”属于“实验方案设计”的是( )
液体读数
4. 下表的探究实验中,“对问题的回答”属于“实验方案设计”的是( )选项
问 题
对问题的回答
A
吹灭蜡烛时产生的白烟是什么?
主要成分是未燃烧的石蜡蒸汽形成的固体小颗粒
B
火焰为什么会向上?
热气流上升,形成对流,还可补充氧气
C
蜡烛火焰温度哪层最高?
外焰氧气浓度大,反应剧烈,温度高
D
蜡烛燃烧后的产物是什么?
用干燥烧杯罩在火焰上方,观察;稍后迅速将烧杯倒置,倒入适量澄清石灰水,振荡,观察
A、A B、B C、C D、D5. 下列实验装置中不能用来测定空气中氧气含量的是( )A、 B、
B、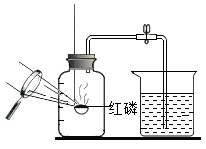 C、
C、 D、
D、 6. 每年3月2日为世界水日,下列有关说的说法正确的是( )A、软水一定为纯净物 B、电解水时负极和正极产生的气体的质量比约为2:1 C、自来水的净化过程为沉降、过滤、吸附、杀菌 D、用氢气燃烧的方法可证明水由氢原子和氧原子组成的7. 下列物质中含氧分子的是( )A、空气 B、氯酸钾 C、过氧化氢 D、高锰酸钾8. 真空包装食品进入高原地区,包装袋往往会鼓起,这是因为包装袋内的气体分子()A、质量增大 B、间隔增大 C、体积增大 D、个数增多9. 我国“辽宁号”航母甲板上涂有耐高温、耐磨的碳化硅(SiC)涂层,碳化硅的结构类似于金刚石的结构,则构成碳化硅的粒子是( )A、分子 B、原子 C、离子 D、中子10. 某纯净物在氧气中完全燃烧只生成二氧化碳和水。由此推知该纯净物中( )A、一定含有碳、氢、氧元素 B、一定含有碳、氢元素,可能含有氧元素 C、只含碳、氢元素,不含氧元素 D、无法确定11. 铝在一百多年里产量得到大幅度的提高,并被广泛地使用,原因之一就是铝的抗腐蚀性能好。铝具有良好抗腐蚀性能的原因是( )A、铝的化学性质不活泼 B、铝不与酸、碱反应 C、铝常温下不与氧气反应 D、铝表面生成一层致密的氧化铝保护膜12. 推理是一种重要的学习方法。下列推理中正确的是( )A、氧化物中含有氧元素,则含氧元素的物质一定为氧化物 B、单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质 C、原子核是由质子和中子构成的,故所有的原子核内都有质子和中子 D、同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率
6. 每年3月2日为世界水日,下列有关说的说法正确的是( )A、软水一定为纯净物 B、电解水时负极和正极产生的气体的质量比约为2:1 C、自来水的净化过程为沉降、过滤、吸附、杀菌 D、用氢气燃烧的方法可证明水由氢原子和氧原子组成的7. 下列物质中含氧分子的是( )A、空气 B、氯酸钾 C、过氧化氢 D、高锰酸钾8. 真空包装食品进入高原地区,包装袋往往会鼓起,这是因为包装袋内的气体分子()A、质量增大 B、间隔增大 C、体积增大 D、个数增多9. 我国“辽宁号”航母甲板上涂有耐高温、耐磨的碳化硅(SiC)涂层,碳化硅的结构类似于金刚石的结构,则构成碳化硅的粒子是( )A、分子 B、原子 C、离子 D、中子10. 某纯净物在氧气中完全燃烧只生成二氧化碳和水。由此推知该纯净物中( )A、一定含有碳、氢、氧元素 B、一定含有碳、氢元素,可能含有氧元素 C、只含碳、氢元素,不含氧元素 D、无法确定11. 铝在一百多年里产量得到大幅度的提高,并被广泛地使用,原因之一就是铝的抗腐蚀性能好。铝具有良好抗腐蚀性能的原因是( )A、铝的化学性质不活泼 B、铝不与酸、碱反应 C、铝常温下不与氧气反应 D、铝表面生成一层致密的氧化铝保护膜12. 推理是一种重要的学习方法。下列推理中正确的是( )A、氧化物中含有氧元素,则含氧元素的物质一定为氧化物 B、单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质 C、原子核是由质子和中子构成的,故所有的原子核内都有质子和中子 D、同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率二、科普阅读题
-
13. 阅读下面科普短文,回答问题:
炼草成油不是梦
化石能源的大量使用会产生大量CO2 , 同时产生一些有污染的烟气,威胁全球生态。为了有效改善生态,有的国家利用富含纤维素的草本植物、可食用作物(包括玉米、大豆、甘蔗)为原料,制造草油。用可食用作物制造生物燃料是最简单可行的,但是并非长久之计,因为没有足够的耕地来满足发达国家对液态燃油的需求。其实,可转化为草油的原料有很多,从木材废料到农业废弃物,再到“能源生物”,这些原料耕作成本低、产量大,而且这些植物都能够在农田的边际土地上快速生长,它们的种植不会千扰和危及粮食作物的生长,放眼全球,每年可利用上述物质能转化的生物燃料相当于340亿—1600亿桶原油,已超过全球每年30亿桶原油的消耗量。纤维素类草本植物能转化成任何类型的燃料,如乙醇、普通汽油、柴油甚至航空燃油。2011年,第一个商业化生物燃料炼制厂已建成。人类历史上的能源新纪元—草油时代就要到来。
(1)、化石能源是。A纯净物 B混合物
(2)、“炼草成油”属于变化。A化学 B物理
草油的使用有效缓解温室效应。
A能 B不能
(3)、纤维素类草本植物能转化为乙醇,乙醇属于能源。A可再生 B不可再生
(4)、推动草油业的发展,可提高周边农户的收入,说说你的建议:(写一条)。三、填空题
-
14. 元素周期表是学习和研究化学的重要工具,请分析图中的信息并回答下列问题。
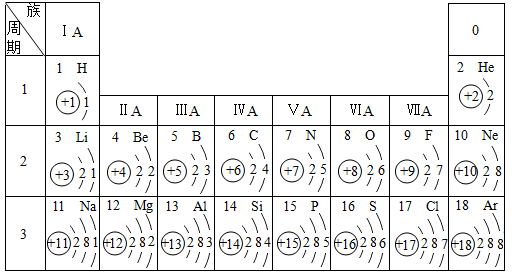 (1)、表中不同元素最本质区别是不同。(2)、原子序数为3的元素属于(填“金属”或“非金属”)元素。(3)、氮元素和磷元素的化学性质相似,是因为氮原子和磷原子的相同。(4)、由原子序数为11、17二种元素组成的化学式是。(5)、下列四种粒子的结构示意图中,表示金属离子的是。
(1)、表中不同元素最本质区别是不同。(2)、原子序数为3的元素属于(填“金属”或“非金属”)元素。(3)、氮元素和磷元素的化学性质相似,是因为氮原子和磷原子的相同。(4)、由原子序数为11、17二种元素组成的化学式是。(5)、下列四种粒子的结构示意图中,表示金属离子的是。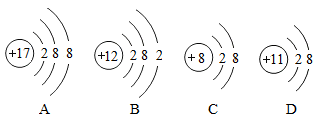
四、综合题
-
15. 化学是建立在实验基础上的自然学科。
 (1)、用如图甲所示的装置探究燃烧的条件,发现铜片上的红磷和热水中的白磷都不燃烧,铜片上的白磷燃烧。
(1)、用如图甲所示的装置探究燃烧的条件,发现铜片上的红磷和热水中的白磷都不燃烧,铜片上的白磷燃烧。①由铜片上的白磷燃烧和红磷不燃烧对比,得出燃烧的条件之一是:。铜片能点燃白磷是利用了铜片的性。
②试验完毕后,将烧杯中的热水慢慢倒出,发现白磷刚刚露出水面,白磷立即剧烈燃烧,解释原因:。
(2)、结合图乙有关实验,回答问题:硫在氧气中燃烧时集气瓶内预先加入少量水的原因是;燃烧的现象是。16. 如图为实验室制取并收集气体的装置图,回答下列问题。
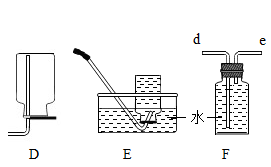 (1)、a仪器的名称是。(2)、实验室用纯净物制取氧气的化学方程式是。(3)、若用F装置收集并测量氧气的体积,应在(填“d”或“e”)端连接量筒。(4)、用B装置制取二氧化碳便于控制反应的发生与停止,制取时应将大理石放在(填“b”或“c”)。(5)、实验室常用加热高锰酸钾固体制取氧气,现对一定量的高锰酸钾固体进行加热,加热过程中涉及的相关量随时间变化的图像正确的是。
(1)、a仪器的名称是。(2)、实验室用纯净物制取氧气的化学方程式是。(3)、若用F装置收集并测量氧气的体积,应在(填“d”或“e”)端连接量筒。(4)、用B装置制取二氧化碳便于控制反应的发生与停止,制取时应将大理石放在(填“b”或“c”)。(5)、实验室常用加热高锰酸钾固体制取氧气,现对一定量的高锰酸钾固体进行加热,加热过程中涉及的相关量随时间变化的图像正确的是。

五、科学探究题
-
17. 过氧化钠的化学式为Na2O2在工业上常用作漂白剂、消毒剂、氧化剂等。某化学小组将少量过氧化钠粉末加入盛水的试管中,看到有大量气泡产生。
【提出问题】
过氧化钠与水反应生成的气体是什么物质?
(1)、【作出猜想】猜想Ⅰ:生成H2
猜想Ⅱ:生成O2
猜想Ⅲ:生成CO2
大家一致认为猜想Ⅲ不正确,理由是。
(2)、【实验验证】实验
实验现象
实验结论
用试管收集生成的气体,堵住试管口,移近酒精灯火焰,点燃
无明显现象
用试管收集生成的气体,将带火星的木条伸入试管内
猜想Ⅱ成立
(3)、【查阅资料】过氧化钠与水反应,除了产生气体,还有氢氧化钠生成。写出该反应的化学方程式:。
(4)、【拓展延伸】过氧化钠保存时应注意的问题是。
18. 在探究金属化学性质实验课中,各小组做了如下实验:实验编号
1
2
3
4
实验操作




实验后,同学们按老师要求将废液都倒在指定的大烧杯中,小科猜想该烧杯中的废液可能有硫酸铜、硫酸锌、硫酸亚铁⋯,应该可以从中提炼出铁和铜。经思考后,他设计了如图所示的实验,并设法使滤液甲和乙所含的溶质相同。
 (1)、实验中所加的过量金属粉末是(写名称),则固体C是(写化学式)。(2)、操作③的名称是。(3)、试写出①中的一个反应原理。(4)、探究Zn、Fe、Cu三种金属的活动性顺序,下列试剂的选择方案可行的是____。A.Zn、FeSO4溶液、CuSO4溶液A、Zn、FeSO4溶液、Cu B、ZnSO4溶液、Fe、CuSO4溶液 C、ZnSO4溶液、FeSO4溶液、Cu
(1)、实验中所加的过量金属粉末是(写名称),则固体C是(写化学式)。(2)、操作③的名称是。(3)、试写出①中的一个反应原理。(4)、探究Zn、Fe、Cu三种金属的活动性顺序,下列试剂的选择方案可行的是____。A.Zn、FeSO4溶液、CuSO4溶液A、Zn、FeSO4溶液、Cu B、ZnSO4溶液、Fe、CuSO4溶液 C、ZnSO4溶液、FeSO4溶液、Cu六、计算题
-
19. 实验室有一瓶含杂质的氯酸钾。某兴趣小组利用该药品和二氧化锰制取氧气(杂质不参加反应)。实验数据记录如下:

请回答下列问题:
(1)、a=。(2)、受热分解的氯酸钾的质量为(精确到0.1g)。
-
-