2021-2022人教版九年级化学 第八单元 金属和金属材料 单元测试卷
试卷更新日期:2022-02-24 类型:单元试卷
一、单选题
-
1. 下列有关金属材料的说法正确的是( )A、黄铜片比纯铜片硬度小 B、焊锡的熔点比纯锡的熔点低 C、钢的含碳量比生铁的含碳量高 D、沙漠地区的铁制品比沿海地区的铁制品更易被锈蚀2. 中国高铁在短短的几十年从“跟跑”到“领跑”,成为我国科学技术自主创新的一面旗帜,“有一种骄傲叫做中国高铁”,在骄傲的同时看看你对其中蕴含的化学知识了解多少!下列说法错误的是( )
 A、高铁的普及拉近了城市的距离,带动了沿途经济的发展 B、铺设高铁的轨道,常常用到韧性好、硬度大的不锈钢 C、高铁的建造使用了大量的合金,合金属于金属材料 D、高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是:该反应属于置换反应。3. 下列各组数据比较,其中正确的是( )A、熔点:焊锡>锡 B、地壳中元素含量:铝<铁 C、导电性:银>铝 D、目前世界年产量:铝>铁4. 下列叙述错误的是( )A、生铁中的含碳量小于钢中的含碳量 B、在我国东北地区,露天的铁夏天比冬天更容易生锈 C、回收利用金属可以节约金属资源和能源 D、在空气中铝的抗腐蚀性比铁强5. 据文献报道:一种特殊的铜纳米颗粒具有与金、银极其相似的反应情性,可替代黄金做精密电子元器件,下列对该铜纳米颗粒的判断,正确的是( )A、能与盐酸反应产生氢气 B、具有良好的导电性 C、能与硫酸亚铁发生反应 D、在空气中容易锈蚀6. 科学精神与社会责任,是化学学科素养更高层面的价值追求。化学实践小组的同学欲探究镁、铁、铜三种金属的活动性顺序,下列实验方案可行的是( )A、Fe、Cu、MgSO4溶液 B、FeSO4溶液、Cu、MgSO4溶液 C、Fe、CuSO4溶液、MgSO4溶液 D、Fe、Mg、CuSO4溶液7. 金属材料在生产、生活中有着广泛的应用。下列生活用品所使用的主要材料,属于金属材料的是( )A、汽车轮胎 B、塑料油桶 C、玻璃啤酒瓶 D、不锈钢餐具8. 化学实验是我们应用化学知识、拓展化学思维和培养化学素养的重要途径。下列实验能达到实验目的的是( )A、探究燃烧条件
A、高铁的普及拉近了城市的距离,带动了沿途经济的发展 B、铺设高铁的轨道,常常用到韧性好、硬度大的不锈钢 C、高铁的建造使用了大量的合金,合金属于金属材料 D、高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是:该反应属于置换反应。3. 下列各组数据比较,其中正确的是( )A、熔点:焊锡>锡 B、地壳中元素含量:铝<铁 C、导电性:银>铝 D、目前世界年产量:铝>铁4. 下列叙述错误的是( )A、生铁中的含碳量小于钢中的含碳量 B、在我国东北地区,露天的铁夏天比冬天更容易生锈 C、回收利用金属可以节约金属资源和能源 D、在空气中铝的抗腐蚀性比铁强5. 据文献报道:一种特殊的铜纳米颗粒具有与金、银极其相似的反应情性,可替代黄金做精密电子元器件,下列对该铜纳米颗粒的判断,正确的是( )A、能与盐酸反应产生氢气 B、具有良好的导电性 C、能与硫酸亚铁发生反应 D、在空气中容易锈蚀6. 科学精神与社会责任,是化学学科素养更高层面的价值追求。化学实践小组的同学欲探究镁、铁、铜三种金属的活动性顺序,下列实验方案可行的是( )A、Fe、Cu、MgSO4溶液 B、FeSO4溶液、Cu、MgSO4溶液 C、Fe、CuSO4溶液、MgSO4溶液 D、Fe、Mg、CuSO4溶液7. 金属材料在生产、生活中有着广泛的应用。下列生活用品所使用的主要材料,属于金属材料的是( )A、汽车轮胎 B、塑料油桶 C、玻璃啤酒瓶 D、不锈钢餐具8. 化学实验是我们应用化学知识、拓展化学思维和培养化学素养的重要途径。下列实验能达到实验目的的是( )A、探究燃烧条件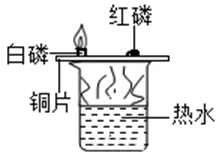 B、探究质量守恒定律
B、探究质量守恒定律 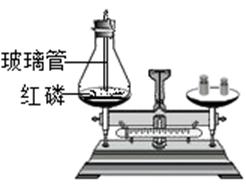 C、探究铁钉生锈条件
C、探究铁钉生锈条件 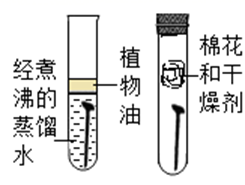 D、探究金属和合金的硬度
D、探究金属和合金的硬度 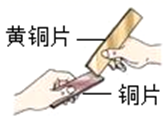 9. 为验证铁、铜、银的金属活动性顺序,某同学设计了以下四组实验。下列说法错误的是( )
9. 为验证铁、铜、银的金属活动性顺序,某同学设计了以下四组实验。下列说法错误的是( )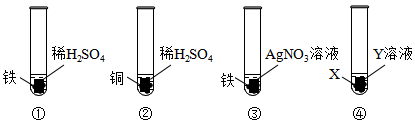 A、通过实验①、②,能验证金属活动性:Fe>Cu B、通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag C、实验④中X为Cu,Y为FeSO4溶液,能验证金属活动性:Fe>Cu D、实验④中X为Cu,Y为AgNO3溶液,能验证金属活动性:Cu>Ag10. 已知金属锰在金属活动性顺序中位于铝和锌之间.下列化学反应不能发生的是( )A、Mn+2HCl=MnCl2+H2↑ B、Mg+MnSO4=MgSO4+Mn C、Fe+MnSO4=FeSO4+Mn D、Mn+CuSO4=MnSO4+Cu11. 在AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完全后过滤,不可能存在的情况是( )A、滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+ B、滤纸上有Ag、Cu,滤液中有Zn2+、Fe2+ C、滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Fe2+ D、滤纸上有Ag、Cu、Fe、Zn,滤液中有Zn2+、Fe2+12. 在FeCl2和CuCl2的混合溶液中加入Zn粉。下列说法错误的是( )A、若反应完全后Zn有剩余,则溶液中有ZnCl2 , 无CuCl2 , 可能有FeCl2 B、若反应完全后Zn有剩余,则溶液中有ZnCl2 , 无CuCl2和FeCl2 C、若反应完全后Zn无剩余,溶液中若有CuCl2 , 则一定有FeCl2 D、若反应完全后Zn无剩余,溶液中若无CuCl2 , 则可能有FeCl213. 把A、B、C三种金属片分别加入稀硫酸中,A、B表面有气泡产生,C无变化;把A加入B的硫酸盐溶液中,A表面析出B。则这三种金属的活动性顺序为( )A、B>A>C B、A>B>C C、C>B>A D、A>C>B14. 向硫酸铜溶液中加入一定量镁和锌的混合粉末,充分反应后过滤,得到滤渣和滤液。向滤渣中加入稀盐酸,有气泡产生,则下列说法正确的是( )A、滤渣中一定含有镁和锌 B、滤渣中一定含有锌和铜 C、滤液中可能含有硫酸铜 D、滤液中一定含有硫酸镁和硫酸锌15. 在64.0g铁粉中先后加稀硫酸和CuSO4溶液,固体质量(g)与所加溶液质量的关系如图示。下列说法错误的是( )
A、通过实验①、②,能验证金属活动性:Fe>Cu B、通过实验①、②、③,能验证金属活动性:Fe>Cu>Ag C、实验④中X为Cu,Y为FeSO4溶液,能验证金属活动性:Fe>Cu D、实验④中X为Cu,Y为AgNO3溶液,能验证金属活动性:Cu>Ag10. 已知金属锰在金属活动性顺序中位于铝和锌之间.下列化学反应不能发生的是( )A、Mn+2HCl=MnCl2+H2↑ B、Mg+MnSO4=MgSO4+Mn C、Fe+MnSO4=FeSO4+Mn D、Mn+CuSO4=MnSO4+Cu11. 在AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完全后过滤,不可能存在的情况是( )A、滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+ B、滤纸上有Ag、Cu,滤液中有Zn2+、Fe2+ C、滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Fe2+ D、滤纸上有Ag、Cu、Fe、Zn,滤液中有Zn2+、Fe2+12. 在FeCl2和CuCl2的混合溶液中加入Zn粉。下列说法错误的是( )A、若反应完全后Zn有剩余,则溶液中有ZnCl2 , 无CuCl2 , 可能有FeCl2 B、若反应完全后Zn有剩余,则溶液中有ZnCl2 , 无CuCl2和FeCl2 C、若反应完全后Zn无剩余,溶液中若有CuCl2 , 则一定有FeCl2 D、若反应完全后Zn无剩余,溶液中若无CuCl2 , 则可能有FeCl213. 把A、B、C三种金属片分别加入稀硫酸中,A、B表面有气泡产生,C无变化;把A加入B的硫酸盐溶液中,A表面析出B。则这三种金属的活动性顺序为( )A、B>A>C B、A>B>C C、C>B>A D、A>C>B14. 向硫酸铜溶液中加入一定量镁和锌的混合粉末,充分反应后过滤,得到滤渣和滤液。向滤渣中加入稀盐酸,有气泡产生,则下列说法正确的是( )A、滤渣中一定含有镁和锌 B、滤渣中一定含有锌和铜 C、滤液中可能含有硫酸铜 D、滤液中一定含有硫酸镁和硫酸锌15. 在64.0g铁粉中先后加稀硫酸和CuSO4溶液,固体质量(g)与所加溶液质量的关系如图示。下列说法错误的是( )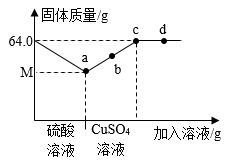 A、b点固体能完全溶于足量稀硫酸 B、d点对应溶液含两种溶质 C、M的值为56.0 D、a、c点对应溶液中FeSO4质量比为1∶8
A、b点固体能完全溶于足量稀硫酸 B、d点对应溶液含两种溶质 C、M的值为56.0 D、a、c点对应溶液中FeSO4质量比为1∶8二、填空题
-
16. 空气中含量较多且化学性质不活泼的气体是;地壳中含量居前两位的元素所形成化合物的化学式为;铁生锈实际上是铁与空气中的作用的结果。17. 在AgNO3和Al(NO3)3的混合溶液中加入一定量的铁粉和铜粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气泡产生,则滤出的固体中一定含有;滤液中一定含有的金属离子是;上述过程中所发生有关反应的化学方程式为(写出一个即可)。18. 铝的化学性质活泼,而铝制品却很耐腐蚀的原因是(用文字描述);现取一定量氧化铁和氧化铝的混合物加入含溶质19.6g的稀硫酸,恰好完全反应,则原混合物中氧元素的质量是g。
三、实验探究题
-
19. 某学习小组对铁锈蚀进行探究。
(提出问题)铁锈蚀与哪些因素有关?
(查阅资料)
①氯化钙固体可作干燥剂。
②一定条件下,碳可加快铁的锈蚀,但碳本身不参加反应。
(设计与实验)
(1)、实验一:定性探究铁锈蚀的因素取四枚相同的洁净无锈铁钉分别放入试管,进行图实验,现象如表1.
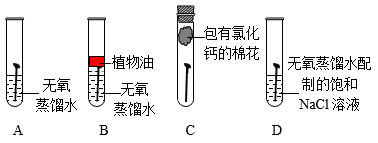
表1
试管
一周后现象
A
铁钉表面有一层铁锈
B
铁钉表面无明显变化
C
铁钉表面无明显变化
D
铁钉表面有较厚铁锈
对比A、B、C试管中实验现象,说明铁锈蚀主要是铁与发生化学反应。
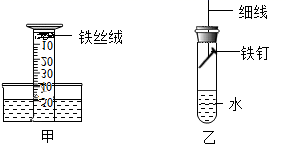
(2)、对比A、D试管中实验现象,说明铁锈蚀还与有关。(3)、铁锈蚀后应及时除锈的原因是。写出用盐酸除铁锈的化学方程式。(4)、实验二:影响铁的锈蚀速度的因素。该小组用图甲装置进行探究铁的锈蚀的实验(量筒内的铁丝绒的量充足),起始时量筒内水面处于50mL刻度处,之后水面缓慢上升。几天后水面最终处于约(填“40”或“10”)mL刻度处。
(5)、小强同学进行如下拓展探究实验:取铁钉用砂纸打磨,称其质量,按图乙安装装置,放置3天,再取出铁钉称量。在不同温度下重复上述实验,得到铁钉质量增加情况如下表。小强同学的实验是探究因素对铁钉锈蚀快慢的影响,结论是。温度/℃
10
20
30
40
50
铁钉质量增加/g
0.02
0.04
0.08
0.16
0.18
四、计算题
-
20. 为测定某铜、锌合金中铜的质量分数,兴趣小组同学称取10g合金于烧杯中,将40g稀盐酸分四次加入,充分反应,测得实验数据如下表所示:
第一次
第二次
第三次
第四次
加入稀盐酸的质量(g)
10
10
10
10
烧杯中剩余物的质量(g)
19.96
29.92
39.90
49.90
(1)、充分反应后产生气体的总质量g。(2)、该铜、锌合金中铜的质量分数为多少?(写出计算过程)
-