2021-2022人教版九年级化学 第八单元 课题3 金属资源的利用和保护 课时提高训练
试卷更新日期:2022-02-24 类型:同步测试
一、单选题
-
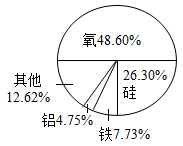
1. 地壳中含量最多的元素是( )A、O B、Fe C、Si D、Al2. 垃圾分类势在必行,废铜烂铁应归属于哪一类( )A、有害垃圾 B、厨余垃圾 C、其他垃圾 D、可回收垃圾3. 下列物质由地壳中含量最多的金属元素、非金属元素和空气中含量最多的元素组成是( )A、CaCO3 B、Al2(SO4)3 C、Al(NO3)3 D、Fe(OH)34. 建立模型是学习化学的重要方法,下列模型正确的是( )A、地壳中元素含量模型
 B、物质组成及构成模型
B、物质组成及构成模型 C、物质分类
C、物质分类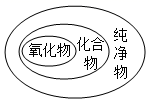 D、灭火方法的目的模型
D、灭火方法的目的模型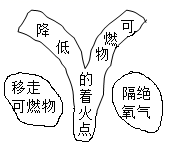 5. 下列关于资源的叙述正确的是( )A、钛和钛合金被认为是21世纪的重要金属材料 B、年产量最高的金属是铜 C、海水中含有100多种元素 D、世界上每年因腐蚀而报废的金属设备和材料相当于年产量的50%6. 某化学兴趣小组利用如图装置探究铁生锈的条件,一段时间后,只有一个集气瓶中的铁丝生锈,下列说法错误的是( )
5. 下列关于资源的叙述正确的是( )A、钛和钛合金被认为是21世纪的重要金属材料 B、年产量最高的金属是铜 C、海水中含有100多种元素 D、世界上每年因腐蚀而报废的金属设备和材料相当于年产量的50%6. 某化学兴趣小组利用如图装置探究铁生锈的条件,一段时间后,只有一个集气瓶中的铁丝生锈,下列说法错误的是( )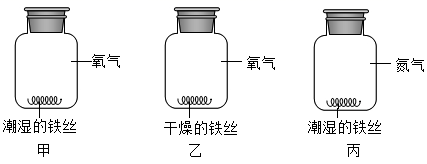 A、甲瓶中的铁丝生锈 B、对比甲和乙的现象,可知铁生锈需要水 C、对比甲和丙的现象,可知隔绝氧气可以防止铁生锈 D、对比乙和丙的现象,可知铁生锈需要水和氧气7. 芯片是中美经贸摩擦的焦点之一、如图所示为制造芯片主要材料高纯硅的生产流程(反应条件已略去)。下列说法正确的是( )
A、甲瓶中的铁丝生锈 B、对比甲和乙的现象,可知铁生锈需要水 C、对比甲和丙的现象,可知隔绝氧气可以防止铁生锈 D、对比乙和丙的现象,可知铁生锈需要水和氧气7. 芯片是中美经贸摩擦的焦点之一、如图所示为制造芯片主要材料高纯硅的生产流程(反应条件已略去)。下列说法正确的是( )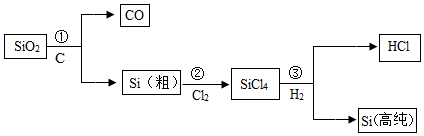 A、只有反应③是置换反应 B、SiCl4中Si的化合价为+4 C、Si是地壳中含量最高的非金属元素 D、该过程的尾气可直接排放到环境中8. 下列有关对自行车的做法不合理的是( )A、车架表面喷涂油漆 B、钢圈表面镀防护金属 C、露天放置,日晒雨淋 D、链条表面涂机油9. 硅(Si)是信息技术的关键材料,工业制硅的反应之一是 。下列说法正确的是( )A、Si是地壳中含量最多的元素 B、X的化学式为H4Cl4 C、SiCl4中硅元素的化合价是-4价 D、该反应中只有氯元素的化合价未发生改变10. 工业上利用黄铁矿(主要成分是FeS2)煅烧的产物冶炼铁和生产硫酸,其反应方程如下:
A、只有反应③是置换反应 B、SiCl4中Si的化合价为+4 C、Si是地壳中含量最高的非金属元素 D、该过程的尾气可直接排放到环境中8. 下列有关对自行车的做法不合理的是( )A、车架表面喷涂油漆 B、钢圈表面镀防护金属 C、露天放置,日晒雨淋 D、链条表面涂机油9. 硅(Si)是信息技术的关键材料,工业制硅的反应之一是 。下列说法正确的是( )A、Si是地壳中含量最多的元素 B、X的化学式为H4Cl4 C、SiCl4中硅元素的化合价是-4价 D、该反应中只有氯元素的化合价未发生改变10. 工业上利用黄铁矿(主要成分是FeS2)煅烧的产物冶炼铁和生产硫酸,其反应方程如下:① ②
③ ④
下列说法错误的是( )
A、反应①②③均需要较高的温度 B、反应③④属于化合反应 C、①③④中硫元素化合价均发生了变化 D、只有①②③发生了氧化反应11. 它曾被认为是带有神秘性的最珍贵的金属,被埃及人称为“天石”,其元素的含量在地壳中占第四位。现代化学中“天石”的元素名称和元素符号是( )A、锡Sn B、铁 Fe C、硅Si D、铝Al12. 为测定某石灰石样品中碳酸钙的质量分数,取一定质量的石灰石样品于烧杯中,将20g稀盐酸分4次加入样品中,充分反应后经过滤、干燥、称重,得实验数据如下:第一次
第二次
第三次
第四次
稀盐酸的用量/g
5.0
5.0
5.0
5.0
剩余固体的质量/g
1.5
1.0
0.5
0.3
已知石灰石中的杂质既不与盐酸反应,也不溶解于水。下列说法错误的是( )
A、第三次实验后碳酸钙无剩余 B、第三次实验后盐酸无剩余 C、实验中所取样品质量为2g D、样品中碳酸钙的质量分数是85%13. 如图中是地壳中各元素质量分数的统计图, 图中B表示元素的是( )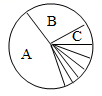 A、氧元素 B、铝元素 C、铁元素 D、硅元素14. 《天工开物》对钢铁冶炼过程有如下记载。有关说法正确的是( )A、“垦土拾锭”:铁元素是地壳中含量最高的金属元素
A、氧元素 B、铝元素 C、铁元素 D、硅元素14. 《天工开物》对钢铁冶炼过程有如下记载。有关说法正确的是( )A、“垦土拾锭”:铁元素是地壳中含量最高的金属元素 B、“淘洗铁砂”:铁矿石(主要成分为Fe2O3)能溶于水
B、“淘洗铁砂”:铁矿石(主要成分为Fe2O3)能溶于水  C、“生熟炼铁”:冶炼铁过程中发生了化学变化
C、“生熟炼铁”:冶炼铁过程中发生了化学变化  D、“锤锻成钢”:生铁高温锻打成钢,碳元素含量升高
D、“锤锻成钢”:生铁高温锻打成钢,碳元素含量升高  15. 为测定某石灰石样品中碳酸钙的质量分数,取2.0g石灰石样品于烧杯中,将20g稀盐酸分4次加入样品中,充分反应后经过滤、干燥、称重,得实验数据如下:
15. 为测定某石灰石样品中碳酸钙的质量分数,取2.0g石灰石样品于烧杯中,将20g稀盐酸分4次加入样品中,充分反应后经过滤、干燥、称重,得实验数据如下:第一次
第二次
第三次
第四次
稀盐酸的用量/g
5.0
5.0
5.0
5.0
剩余固体的质量/g
1.5
1.0
0.5
0.3
已知石灰石中的杂质既不与盐酸反应,也不溶解于水。下列说法正确的是( )
A、第三次实验后碳酸钙无剩余 B、第四次实验后盐酸无剩余 C、盐酸中HCl的质量分数是3.65% D、样品中碳酸钙的质量分数是85%二、填空题
-
16. 铁生锈实际上是铁与空气中的作用的结果,将黄铜片和纯铜片相互刻画时有明显划痕的是。17. 铁属于材料,铁生锈主要是铁与空气中的、(填化学式)反应,请写出一种防止铁生锈的方法:。18. 2021年4月23日,在人民海军72岁生日这天,海军三型主战舰艇——长征18号艇、大连舰、海南舰在海南三亚同时加入战斗序列。舰船的外壳材料是高强度钢。将生铁冶炼成钢时,组成中发生改变的是。舰船外壳常年浸泡在海水中,容易生锈,为防止生锈,常在舰船底部焊接一些比铁的活泼性稍强的金属,如(写一种)。



三、实验探究题
-
19. 在高温下,铁与水蒸气能发生反应生成一种常见的铁的氧化物和一种气体。
资料:①无水氯化钙具有吸水性:
②常见铁的氧化物有关信息如表:
常见铁的氧化物
FeO
Fe2O3
Fe3O4
颜色、状态
黑色粉末
红棕色粉末
黑色粉末
能否被磁铁吸引
否
否
能
③四氧化三铁能与稀盐酸反应:。
(1)、Ⅰ、探究“铁与水蒸气”反应的气体产物【实验探究】取适量的铁粉与湿棉花(棉花的成分不参加反应)于反应装置A中。按下图所示进行实验,试管内放一团湿棉花的目的是;实验时棉花没有燃烧,其原因是;观察到C处管口有淡蓝色火焰,烧杯内壁有水雾。说明产生的气体是。
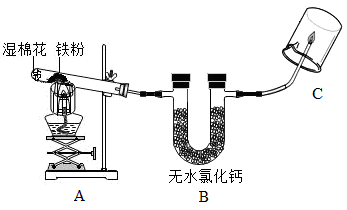 (2)、Ⅱ、探究“铁与水蒸气”反应后剩余固体的成分及含量
(2)、Ⅱ、探究“铁与水蒸气”反应后剩余固体的成分及含量【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想1:剩余固体是;
猜想2:剩余固体是Fe和Fe3O4。
(3)、【实验验证】甲同学取样品于烧杯中,加入足量的稀盐酸,观察到(填实验现象),溶液由无色变为黄绿色,说明猜想2正确。(4)、【实验结论】铁和水蒸气反应的化学方程式为。(5)、【含量测定】乙同学取A装置中剩余黑色固体50g,与足量的CO反应后,所得固体质量为43.6g,则剩余黑色固体中Fe3O4的质量分数为。四、计算题
-
20.(1)、小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%。现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁96%的生铁的质量是(结果保留整数)?
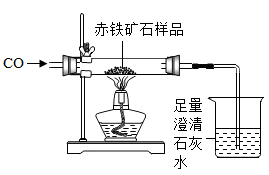 (2)、在利用上图装置进行实验时,小强得到如下两组数据(杂质不参加反应):
(2)、在利用上图装置进行实验时,小强得到如下两组数据(杂质不参加反应):反应前
氧化铁完全反应后
A组
玻璃管和赤铁矿石样品的质量m1g
玻璃管和固体物质的质量m2g
B组
烧杯和澄清石灰水的质量m3g
烧杯和烧杯中物质的质量m4g
①m1-m2表示的质量
②你认为他应该选用(填“A”或“B”)组数据来计算赤铁矿石中氧化铁的质量分数。结合装置图回答他不能选用另一组数据计算的原因为。
-