2021-2022人教版九年级化学 第八单元 课题2 金属的化学性质 课时提高训练
试卷更新日期:2022-02-24 类型:同步测试
一、单选题
-
1. 2021年3月,三星堆考古发掘惊艳了整个世界。三星堆遗址已出土金面具残片、巨青铜面具、青铜神树等重要文物,并通过测量碳-14(碳-14原子的中子数为8)含量测定年代。下列有关说法正确的是( )A、金残片熠熠夺目说明金的化学性质稳定 B、青铜合金在物质分类上属于化合物 C、青铜合金熔点比铜高、硬度比铜低 D、碳-14原子的核外电子数为142. 下列金属,常温下一般不能与稀盐酸发生置换反应的是( )A、镁 B、锌 C、铁 D、铜3. 据文献报道:一种特殊的铜纳米颗粒具有与金、银极其相似的反应惰性,可替代黄金做精密电子元器件。下列对该铜纳米颗粒的判断,正确的是( )A、能与盐酸反应产生氢气 B、在空气中容易锈蚀 C、能与硫酸亚铁发生置换反应 D、具有良好的导电性4. 将铁片分别放入下列溶液中充分反应,反应后溶液质量减少的物质是( )A、H2SO4 B、MgSO4 C、ZnCl2 D、CuSO45. 生活中有许多俗语。下列有关说法,从化学的角度理解错误的是( )A、“满架蔷薇一院香”的原因是分子不断运动 B、“真金不怕火炼”说明金的熔点很高 C、“百炼成钢”与“只要功夫深,铁杵磨成针”蕴含的化学原理不相同 D、“火要空心”说的是增大与空气的接触面积,能使可燃物燃烧更充分6. 金属M与Cu(NO3)2溶液可发生反应: 下列叙述错误的( )A、反应进行后,M表面有红色固体析出 B、M一定能发生这个反应: C、若M为镁,恰好完全反应后,溶液质量较反应前减少 D、金属M可能是铝7. 实验小组同学将铝片放入硫酸铜溶液中,出现红色固体,同时产生无色无味的气体。下列猜想不合理的是( )A、该气体是氢气 B、铝片表面的氧化铝与硫酸铜反应 C、硫酸铜溶液呈酸性 D、硫酸铜溶液中混有硫酸8. 西汉刘安曾记载“曾青得铁则化为铜”。这里的“铜”指的是( )A、铜单质 B、铜元素 C、氧化铜 D、铜原子9. 下列图像不能正确反映其变化过程的是( )A、
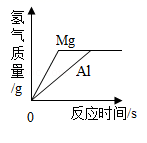 等质量等浓度的稀硫酸分别与足量的金属反应
B、
等质量等浓度的稀硫酸分别与足量的金属反应
B、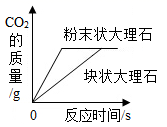 等质量的大理石分别与足量相同的稀盐酸反应
C、
等质量的大理石分别与足量相同的稀盐酸反应
C、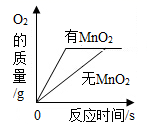 等质量等浓度的过氧化氢溶液分别在有、无MnO2的条件下反应
D、
等质量等浓度的过氧化氢溶液分别在有、无MnO2的条件下反应
D、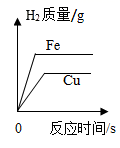 等质量的金属与足量相同的稀盐酸反应
10. 下列化学反应中,属于置换反应的是( )A、4P+5O2 2P2O5 B、Fe+CuSO4=FeSO4+Cu C、CaCO3 CaO+CO2↑ D、Na2CO3+Ca(OH)2=CaCO3↓+2NaOH11. 镁和铝分别与足量的稀盐酸反应,若生成氢气的质量相等,则参加反应的镁和铝的质量之比为( )A、3:2 B、4:3 C、1:1 D、1:212. 将铁粉和铜粉置于AgNO3和Zn(NO3)2混合溶液中,待反应完毕后,过滤所得金属中一定没有的是( )A、Ag和Cu B、Fe和Ag C、Zn D、Fe13. 科学探究中常用到推理的方法。根据下列实验事实推出的结论正确的是( )
等质量的金属与足量相同的稀盐酸反应
10. 下列化学反应中,属于置换反应的是( )A、4P+5O2 2P2O5 B、Fe+CuSO4=FeSO4+Cu C、CaCO3 CaO+CO2↑ D、Na2CO3+Ca(OH)2=CaCO3↓+2NaOH11. 镁和铝分别与足量的稀盐酸反应,若生成氢气的质量相等,则参加反应的镁和铝的质量之比为( )A、3:2 B、4:3 C、1:1 D、1:212. 将铁粉和铜粉置于AgNO3和Zn(NO3)2混合溶液中,待反应完毕后,过滤所得金属中一定没有的是( )A、Ag和Cu B、Fe和Ag C、Zn D、Fe13. 科学探究中常用到推理的方法。根据下列实验事实推出的结论正确的是( )选项
实验事实
实验结论
A
单质中只含一种元素
只含一种元素的物质一定是单质
B
镁、铝、铁都能与盐酸反应生成氢气
金属都能与酸反应生成氢气
C
CO、木炭、酒精、甲烷都可以燃烧
可燃物一定要含有碳元素
D
气体比液体更容易被压缩
气体分子之间的间隔比液体的大
A、A B、B C、C D、D14. 把等质量的X、Y、Z、M四种金属分别加入到等质量、等质量分数的足量稀盐酸中(反应关系如图甲),把金属M加入到足量的Y(NO3)2溶液中(反应关系如图乙)。据此判断四种金属的活动性顺序为( )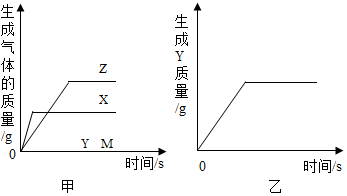 A、M>Y>Z>X B、X>Z>Y>M C、X>Z>M>Y D、Z>X>M>Y15. 想测定铜银混合物中银的含量。称取这种粉末10g,加入足量的硝酸银溶液充分反应后过滤,将所得固体洗涤、干燥后称量,质量为25.2g。计算混合物中银的含量( )A、84% B、68% C、36% D、75%
A、M>Y>Z>X B、X>Z>Y>M C、X>Z>M>Y D、Z>X>M>Y15. 想测定铜银混合物中银的含量。称取这种粉末10g,加入足量的硝酸银溶液充分反应后过滤,将所得固体洗涤、干燥后称量,质量为25.2g。计算混合物中银的含量( )A、84% B、68% C、36% D、75%二、填空题
-
16. 设计从废水中回收硫酸亚铁固体和铜的实验方案如下:
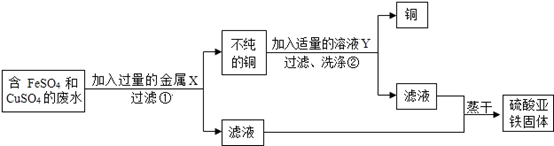
金属X是 , 写出上述实验方案中有关反应的化学方程式:①;②。
17. 请按要求填空:(1)、葡萄糖(C6H12O6)是一种重要的营养物质。其组成中氢元素和氧元素的质量整数比是。其在人体内被完全氧化的产物是(填化学式)。葡萄糖在酒化酶作用下可发生分解反应: ,x为(填数字)。(2)、我国航天领域正在建设中的天宫空间站,使用了大量的合金材料和复合材料。①天宫空间站使用的铁合金材料的硬度比纯铁的硬度(填“大”或“小”)。
②天宫空间站广泛使用了铝、铁、铜。现利用它们完成如下实验
a.将未打磨的铝片放入FeSO4溶液中,没有明显现象
b.将打磨的铝片放入FeSO4溶液中,铝片表面有明显变化。
c.将打磨的铁片放入CuSO4溶液中,铁片表面有新物质生成。
实验a中无现象的原因是。实验b中的化学方程式为。实验c中铁片足量充分反应后,溶液变为色。
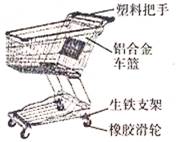
18. 我们在超市购物时,手推车是常用的工具。如图所标示的超市手推车各部件中,属于有机合成材料的是(答一种)。车篮一般用铝合金而不用纯铝制造。铝的化学性质很活泼,但车篮却很少出现腐蚀现象,原因是(用化学方程式表示,下同)。手推车的生铁支架在潮湿的空气中会生锈,用稀盐酸除铁锈(Fe2O3)的原理是。
三、实验探究题
-
19. 在学习金属的化学性质时,老师在课堂上给学生演示了如图实验:
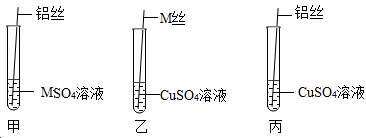 (1)、(给出资料)M是一种金属,MSO4溶液是无色液体。
(1)、(给出资料)M是一种金属,MSO4溶液是无色液体。(实验目的)探究M与铜、铝的活动性顺序。
(猜想与假设)
猜想一:Al>Cu>M;
猜想二:Al>M>Cu;
猜想三:。
(2)、(进行实验)第一步:老师取出M丝、铜丝、铝丝用砂纸进行打磨,目的是。
第二步:老师按照如图进行实验操作,要求同学填写如下表格:
实验操作
实验想象
实验结论
铝丝插入装有MSO4溶液的试管中图甲
铝丝表面出现一层黑色物质
M丝插入装有CuSO4溶液的试管中图乙
M丝表面出现一层红色物质,溶液的颜色
M>Cu
铝丝插入装有CuSO4溶液的试管中图丙
铝丝表面出现一层红色物质,颜色由蓝色变为无色
Al>Cu
(3)、(交流表达)根据表格,可判断猜想正确。写出试管丙中反应的化学方程式。
(4)、(评价与反思)经同学时论后大家认为该实验可以优化,去掉试管(填试管编号)中的实验,也可以得出正确的结论。
四、计算题
-
20. 硅钢是变压器、充电器中的核心材料,其主要成分是Fe和Si。某学生用硅钢样品做了如下实验:取2.8g硅钢样品,将40g稀硫酸分4次加入样品中(其中稀硫酸与硅及其它杂质不反应),充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
实验次数
一
二
三
四
稀硫酸的用量/g
10
10
10
10
剩余固体的质量/g
M
1.4
0.7
0.7
(1)、从以上数据可知,稀硫酸加入第次充分反应后,铁恰好完全反应。(2)、表格中M=。(3)、计算所用稀硫酸中溶质的质量分数。
-