2021-2022人教版九年级化学 第九单元 课题3 溶液的浓度 课时提高训练
试卷更新日期:2022-02-24 类型:同步测试
一、单选题
-
1. 下列关于100g溶质质量分数为10%的氯化钠溶液的理解,正确的是( )A、100g氯化钠溶液中溶解了10g氯化钠 B、溶液中氯化钠与水的质量比为1:10 C、溶液中氯化钠与溶液的质量比为1:9 D、将10g氯化钠溶解于100g水中配成的溶液2. 对于30%的KNO3溶液,下列说法正确的是( )A、溶液中溶质和溶剂的质量比为3:10 B、每100g水中溶解30gKNO3 C、某种条件下,可转化为悬浊液 D、若再加30g硝酸钾,则变为60%KNO3溶液3. 温度不变,对100mL氯化钠饱和溶液进行如下实验(如图所示):实验一,将烧杯甲中溶液转移出50mL到乙烧杯中,实验二,是把5g水和5g氯化钠分别加入在甲、乙烧杯中、则下列结论错误的是( )
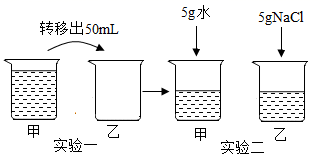 A、实验二后,甲中溶液的溶质质量分数减小 B、实验一后,甲和乙中溶液的溶质质量分数相等 C、实验二后,乙中溶液的溶质质量分数增大 D、实验二后,甲和乙中溶液所含溶质质量相等4. 已知20℃时CuSO4的溶解度为32g。20℃时,取一定质量某CuSO4溶液于烧杯中,按下图进行实验(整个过程中忽略溶剂损失),下列说法错误的是( )
A、实验二后,甲中溶液的溶质质量分数减小 B、实验一后,甲和乙中溶液的溶质质量分数相等 C、实验二后,乙中溶液的溶质质量分数增大 D、实验二后,甲和乙中溶液所含溶质质量相等4. 已知20℃时CuSO4的溶解度为32g。20℃时,取一定质量某CuSO4溶液于烧杯中,按下图进行实验(整个过程中忽略溶剂损失),下列说法错误的是( )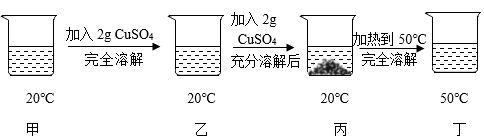 A、溶液中溶质质量分数的大小关系为丁>丙>甲 B、丙中溶液溶质与溶剂的质量比为8:25 C、丁溶液一定是饱和溶液 D、CuSO4 50℃时的溶解度比20℃时的大5. a、b、c三种固体物质的溶解度曲线如图所示。下列说法正确的是( )
A、溶液中溶质质量分数的大小关系为丁>丙>甲 B、丙中溶液溶质与溶剂的质量比为8:25 C、丁溶液一定是饱和溶液 D、CuSO4 50℃时的溶解度比20℃时的大5. a、b、c三种固体物质的溶解度曲线如图所示。下列说法正确的是( )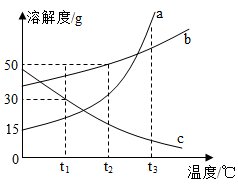 A、t1℃时,a物质的溶解度是30g B、t2℃时,b的饱和溶液中溶质的质量分数为50% C、t3℃时,各取15ga、b、c三种物质分别加入到50g水中充分溶解,能得到饱和溶液的是c D、t3℃时:a、b、c三种物质的饱和溶液均降温到t1℃,三种物质溶质质量分数大小关系为b>c>a6. 室温时,对100mL氯化钠饱和溶液作如下操作,最终甲、乙两烧杯中溶液( )
A、t1℃时,a物质的溶解度是30g B、t2℃时,b的饱和溶液中溶质的质量分数为50% C、t3℃时,各取15ga、b、c三种物质分别加入到50g水中充分溶解,能得到饱和溶液的是c D、t3℃时:a、b、c三种物质的饱和溶液均降温到t1℃,三种物质溶质质量分数大小关系为b>c>a6. 室温时,对100mL氯化钠饱和溶液作如下操作,最终甲、乙两烧杯中溶液( )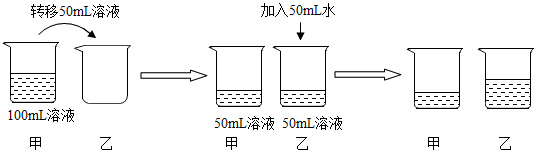 A、溶质质量相同 B、溶质质量分数相同 C、均为不饱和溶液 D、溶剂质量相同7. 下列说法错误的是( )A、用50 g溶质质量分数为10%的NaCl溶液配制溶质质量分数为5%的NaCl溶液需要加水20 g B、100 mL水和100 mL酒精混合后体积小于200 mL,说明分子间有间隔 C、饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液 D、汽油作溶剂可以去除衣物上的油污8. 如图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是( )
A、溶质质量相同 B、溶质质量分数相同 C、均为不饱和溶液 D、溶剂质量相同7. 下列说法错误的是( )A、用50 g溶质质量分数为10%的NaCl溶液配制溶质质量分数为5%的NaCl溶液需要加水20 g B、100 mL水和100 mL酒精混合后体积小于200 mL,说明分子间有间隔 C、饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液 D、汽油作溶剂可以去除衣物上的油污8. 如图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是( )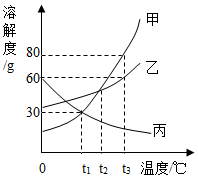 A、t3℃时,甲物质的溶解度为80 B、要将丙的不饱和溶液变为饱和溶液,可采用升高温度的方法 C、t1℃时,甲的饱和溶液的溶质质量分数为30% D、将 t1℃的甲、乙、丙的饱和溶液升温至 t3℃,溶质质量分数的大小关系为甲>乙>丙9. 甲、乙、丙三种固体物质的溶解度曲线如图所示,下列相关说法正确的是( )
A、t3℃时,甲物质的溶解度为80 B、要将丙的不饱和溶液变为饱和溶液,可采用升高温度的方法 C、t1℃时,甲的饱和溶液的溶质质量分数为30% D、将 t1℃的甲、乙、丙的饱和溶液升温至 t3℃,溶质质量分数的大小关系为甲>乙>丙9. 甲、乙、丙三种固体物质的溶解度曲线如图所示,下列相关说法正确的是( )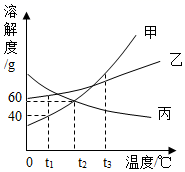 A、t2℃时甲和丙的溶解度都是60 B、t3℃时,甲、乙、丙三种物质的溶液中溶质质量分数一定是甲>乙>丙 C、将t3℃时甲和丙的饱和溶液降温到t2℃,两溶液的溶质质量分数相等 D、将t2℃时160g甲物质的饱和溶液降温到t1℃可析出20g固体(不含结晶水)10. 下列对“50℃,氯化铵的溶解度是50g”理解错误的是( )A、50℃,100g水中最多溶解50g氯化铵 B、氯化铵的溶解度何时都是50g C、50℃,氯化铵的饱和溶液中溶质溶剂之比是1:2 D、50℃,氯化铵的溶液中溶质的质量分数最大是33.3%11. 某小组同学在探究过程中,通过观察与实验,推理与判断,如不考虑水分蒸发,最后得出的结论正确的是( )
A、t2℃时甲和丙的溶解度都是60 B、t3℃时,甲、乙、丙三种物质的溶液中溶质质量分数一定是甲>乙>丙 C、将t3℃时甲和丙的饱和溶液降温到t2℃,两溶液的溶质质量分数相等 D、将t2℃时160g甲物质的饱和溶液降温到t1℃可析出20g固体(不含结晶水)10. 下列对“50℃,氯化铵的溶解度是50g”理解错误的是( )A、50℃,100g水中最多溶解50g氯化铵 B、氯化铵的溶解度何时都是50g C、50℃,氯化铵的饱和溶液中溶质溶剂之比是1:2 D、50℃,氯化铵的溶液中溶质的质量分数最大是33.3%11. 某小组同学在探究过程中,通过观察与实验,推理与判断,如不考虑水分蒸发,最后得出的结论正确的是( )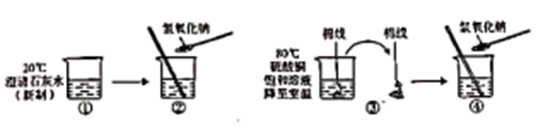
温度/℃
0
20
40
60
80
溶解度/g
熟石灰
0.18
0.16
0.14
0.11
0.09
硫酸铜晶体
14.3
20.7
28.5
40
55
A、①中溶液的溶质质量分数为16% B、②中加入氢氧化钠的过程中,有氢氧化钙析出 C、③中棉线上析出晶体的质量一定是34.3g D、④中加入氢氧化钠前、后均为硫酸铜饱和溶液12. 为探究硝酸钾的溶解性,进行了如图实验(见图Ⅰ),结合KNO3溶解度曲线(见图Ⅱ)判断,下列说法错误的是( )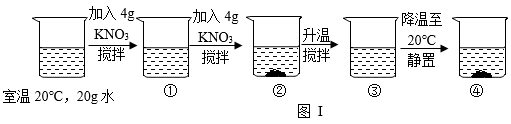
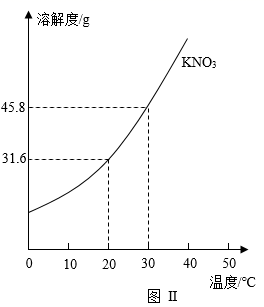 A、溶液②、溶液④一定是饱和溶液 B、溶液①、溶液③一定是不饱和溶液 C、溶液②、溶液③的质量:③>② D、溶液②、溶液③溶液④的溶质质量分数:③>②=④13. 不同温度下Ca(OH)2的溶解度如下表所示。下列说法正确的是( )
A、溶液②、溶液④一定是饱和溶液 B、溶液①、溶液③一定是不饱和溶液 C、溶液②、溶液③的质量:③>② D、溶液②、溶液③溶液④的溶质质量分数:③>②=④13. 不同温度下Ca(OH)2的溶解度如下表所示。下列说法正确的是( )温度/℃
20
40
60
溶解度/g
0.165
0.121
0.116
A、Ca(OH)2溶解度随温度升高而增大 B、20℃时,100g水最多溶解0.165gCa(OH)2 C、40℃时,Ca(OH)2饱和溶液的溶质质量分数为12.1% D、将20℃时Ca(OH)2的饱和溶液升温至60℃,可变为不饱和溶液14. 下表为硝酸钾和熟石灰两种物质的溶解度。则以下说法正确的是( )温度/℃
0
20
30
50
60
80
90
溶解度/g
KNO3
13.3
31.6
45.8
85.5
110
169
200
Ca(OH)2
0.185
0.165
0.153
0.138
0.116
0.094
0.085
A、两种物质溶解度受温度的影响都较大 B、30℃时,饱和硝酸钾溶液的溶质质量分数为45.8% C、60℃时将100g硝酸钾加到100g水中,充分搅拌后降温至20℃,析出68.4g固体 D、室温时,向饱和石灰水中加入少量生石灰,恢复到室温后,溶液溶质质量分数变大15. 海水中含有氯化钙,氯化钙的溶解度如下表。下列说法正确的是( )温度/℃
10
20
30
40
溶解度/g
65.0
74.5
100
116
A、氯化钙的溶解度随温度的升高而减小 B、10℃时,氯化钙的饱和溶液的溶质质量分数为65.0% C、30℃时,向100g氯化钙固体中加入50g水,充分搅拌后能得到150g氯化钙溶液 D、将40℃的氯化钙的饱和溶液降温至20℃,有晶体析出二、填空题
-
16. 过氧化氢是一种有效的防疫新冠病毒的消毒剂。现有一瓶新售的过氧化氢溶液,标签如图所示,若要配制1500g溶质的质量分数为3%的医用过氧化氢溶液,需用这种过氧化氢溶液的质量是g,需要加水g。(直接填写答案,无需写出计算过程)
 17. 海水淡化可采用膜分离技术。如图所示,对淡化膜右侧加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,并将分析结果填入下列空格。
17. 海水淡化可采用膜分离技术。如图所示,对淡化膜右侧加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,并将分析结果填入下列空格。
溶质的质量(填“变大”、“变小”、“不变”,下同);溶剂的质量;溶液的质量;溶质的质量分数。
18. A、B、C三种固体物质的溶解度曲线如图所示,请回答:当A中混有少量B时,可采用方法提纯A物质。t2℃时,将75 g A的饱和溶液稀释为20%的溶液,需加水的质量为g。t2℃时,将A、B、C三种物质的饱和溶液降温至t1 ℃,所得溶液溶质的质量分数由大到小的顺序为。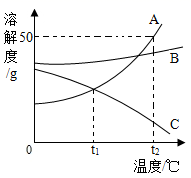
三、实验探究题
-
19. 实验小组同学在一定温度下进行硝酸钾的固体的溶解实验。(1)、(定性研究)同学们进行如下实验,发现1号试管中硝酸钾全部溶解,2号试管中固体没有完全溶解。由此获得的实验结论是 。要使2号试管中的固体全部溶解,可采取的方法有 、 。
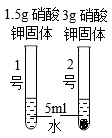 (2)、(定量研究)实验小组同学在一定温度下进行硝酸钾的固体溶液实验。实验数据如下。请根据数据进行分析。
(2)、(定量研究)实验小组同学在一定温度下进行硝酸钾的固体溶液实验。实验数据如下。请根据数据进行分析。实验序号
实验1
实验2
实验3
实验4
水的质量(g)
100
100
100
100
加入硝酸钾的质量(g)
80
100
120
140
溶液质量(g)
180
200
210
M
请计算实验2中硝酸钾的溶质质量分数是 。
(3)、现将实验2中的溶液稀释成20%的硝酸钾溶液,需要加水的质量为 g。(4)、请判断实验2中硝酸钾溶液是 溶液。(选填“饱和”或“不饱和”)。(5)、实验4中M的数值是 。四、计算题
-
20. 溶液在人类的生产、生活和科学研究中具有广泛的应用。请完成下列配置溶液的问题:(1)、农业生产中通常用溶质质量分数为10%—20%的氯化钠溶液来选种。
①现要配制120kg溶质质量分数为20%的氯化钠溶液,需要取用固体氯化钠kg。
②用60kg溶质质量分数为20%的氯化钠溶液,可稀释成12%的氯化钠溶液kg。
(2)、制作“叶脉书签”需要配制100g12%的NaOH溶液(水的密度为1g/mL),需要称量NaOH固体g,需要量取水mL。
-