四川省眉山市青神县2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-02-23 类型:期末考试
一、单选题
-
1. 实验室有一瓶标签残缺的白色粉末药品,有同学认为是氯酸钾。这属于科学探究中的( )A、猜想假设 B、设计实验 C、收集证据 D、得出结论2. 下列非物质文化遗产制作过程,主要利用化学变化的是( )A、竹编
 B、锡雕
B、锡雕 C、酿酒
C、酿酒 D、剪纸
D、剪纸 3. 关于原子序数为8的元素,下列说法正确的是( )A、元素符号为N B、属于金属元素 C、在地壳中含量最多 D、原子核外电子数为104. 下列仪器不能加热的是( )A、烧杯 B、试管 C、量筒 D、燃烧匙5. 下列有关物质的用途不正确的是( )A、
3. 关于原子序数为8的元素,下列说法正确的是( )A、元素符号为N B、属于金属元素 C、在地壳中含量最多 D、原子核外电子数为104. 下列仪器不能加热的是( )A、烧杯 B、试管 C、量筒 D、燃烧匙5. 下列有关物质的用途不正确的是( )A、 用木炭制墨汁
B、
用木炭制墨汁
B、 用压缩天然气做汽车燃料
C、
用压缩天然气做汽车燃料
C、 氧气用于医疗急救
D、
氧气用于医疗急救
D、 石墨做电极
6. 保护环境是我们每个公民的义务。下列做法中,不利于保护环境的是( )A、回收废旧电池 B、倡导绿色出行 C、减少农药使用 D、发展露天烧烤7. 打开香水瓶盖闻到浓郁的香水气味,说明( )A、分子在不停地运动 B、分子间有间隔 C、分子的体积很小 D、分子的质量很小8. 下图是甲、乙两种粒子的结构示意图。下列有关两种粒子的说法中,合理的是( )
石墨做电极
6. 保护环境是我们每个公民的义务。下列做法中,不利于保护环境的是( )A、回收废旧电池 B、倡导绿色出行 C、减少农药使用 D、发展露天烧烤7. 打开香水瓶盖闻到浓郁的香水气味,说明( )A、分子在不停地运动 B、分子间有间隔 C、分子的体积很小 D、分子的质量很小8. 下图是甲、乙两种粒子的结构示意图。下列有关两种粒子的说法中,合理的是( )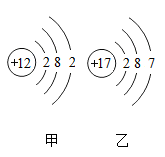 A、甲、乙两种粒子都不显电性 B、乙粒子在化学反应中易失去电子 C、甲粒子是金属阳离子 D、甲、乙两种粒子不能结合成化合物9. 11月4日,英国药品和保健产品监管局正式批准抗新冠病毒药物Molnupiravir(C13H19N3O7)上市,用于治疗轻度到中度新冠肺炎患者。人类迎来了全球首个新冠口服抗病毒药物,其效果全球拭目以待。下列关于此药叙述正确的是( )
A、甲、乙两种粒子都不显电性 B、乙粒子在化学反应中易失去电子 C、甲粒子是金属阳离子 D、甲、乙两种粒子不能结合成化合物9. 11月4日,英国药品和保健产品监管局正式批准抗新冠病毒药物Molnupiravir(C13H19N3O7)上市,用于治疗轻度到中度新冠肺炎患者。人类迎来了全球首个新冠口服抗病毒药物,其效果全球拭目以待。下列关于此药叙述正确的是( )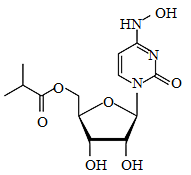 A、属于氧化物 B、氧元素的质量分数最大 C、由碳、氧和氢三种元素组成 D、每个分子都由碳、氧、氮和氢四种原子构成10. 如图为硫单质制备硫酸的简单流程图。下列说法正确的是( )
A、属于氧化物 B、氧元素的质量分数最大 C、由碳、氧和氢三种元素组成 D、每个分子都由碳、氧、氮和氢四种原子构成10. 如图为硫单质制备硫酸的简单流程图。下列说法正确的是( )
⑴硫颜色为黄色,俗称硫黄
⑵SO2、SO3和H2SO4都属于氧化物
⑶步骤 ①、②和③都属于化合反应
⑷此流程图缺少尾气的处理
⑸步骤①,反应发出淡蓝色火焰,生成带有刺激性气味的气体
A、(1)(2)(3) B、(1)(3)(4) C、(2)(3)(5) D、(3)(4)(5)11. 某小组利用如图装置进行创新实验。实验时,先加热炭粉,一段时间后将酒精灯移至CuO处加热。下列说法不正确的是( )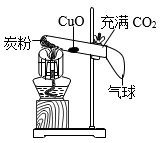 A、酒精灯加网罩是为了提高火焰温度 B、气球可以收集尾气,防止污染空气 C、反应过程中,黑色氧化铜变为红色固体 D、装置中发生反应:12. 利用下图,欲除去X气体中的杂质,对应的Y正确的是( )
A、酒精灯加网罩是为了提高火焰温度 B、气球可以收集尾气,防止污染空气 C、反应过程中,黑色氧化铜变为红色固体 D、装置中发生反应:12. 利用下图,欲除去X气体中的杂质,对应的Y正确的是( )
X杂质
Y
A
CO2(CO)
Cu
B
N2(O2)
Cu
C
CO(H2)
CuO
D
H2(H2O)
CuO
A、A B、B C、C D、D13. “嫦娥五号”月球采样返回,已测得月壤含CaAl2Si2O8以及可作为核聚变燃料的氦﹣3等物质。如图为氦在元素周期表中的部分信息。下列说法不正确的是( ) A、CaAl2Si2O8中,Si 的化合价为+4 B、CaAl2Si2O8中,Si、O两种元素的质量比为 7:16 C、氦﹣3原子的质子数与中子数之和为3,则其核外电子数为3 D、Ca、Al、Si、O和He的本质区别在于其原子核电荷数的不同14. 某兴趣小组为探究影响化学反应速率的因素,使用等量的同种钙片和白醋开展四组实验,分别测得产生的二氧化碳浓度随时间的变化曲线如图所示。选取CO2的浓度从0~8%为研究对象,下列实验结果的分析,不正确的是( )
A、CaAl2Si2O8中,Si 的化合价为+4 B、CaAl2Si2O8中,Si、O两种元素的质量比为 7:16 C、氦﹣3原子的质子数与中子数之和为3,则其核外电子数为3 D、Ca、Al、Si、O和He的本质区别在于其原子核电荷数的不同14. 某兴趣小组为探究影响化学反应速率的因素,使用等量的同种钙片和白醋开展四组实验,分别测得产生的二氧化碳浓度随时间的变化曲线如图所示。选取CO2的浓度从0~8%为研究对象,下列实验结果的分析,不正确的是( ) A、对比①③,温度越高,反应速率越快 B、对比②③,反应物接触面积越小,反应速率越慢 C、对比③④,反应物接触面积越大,反应速率越快 D、对比①②③④,④的反应速率最慢
A、对比①③,温度越高,反应速率越快 B、对比②③,反应物接触面积越小,反应速率越慢 C、对比③④,反应物接触面积越大,反应速率越快 D、对比①②③④,④的反应速率最慢二、填空题
-
15. 饮水安全是脱贫攻坚“两不愁、三保障、安全”的重要内容和指标,关乎百姓生命健康。(1)、2个水分子可表示为。(2)、在净化水的过程中常用来吸附水中的色素和异味。(3)、写出电解水的化学方程式。16. 我国提出2060年前实现碳中和,彰显了负责任大国的作为与担当。(1)、现阶段的能源结构仍以化石燃料为主,化石燃料包括煤、和天然气。(2)、下列燃料在O2中燃烧时,不会产生CO2的是______(填序号)。A、天然气 B、氢气 C、肼(N2H4)(3)、捕集、利用和封存CO2是实现碳中和的一种途径。矿物质碳化封存的反应之一是氧化镁与CO2反应生成碳酸镁,该反应的化学方程式为。
三、综合题
-
17. 如图为实验室制取气体并验证气体性质的部分装置(氢气可以用浓硫酸干燥,装置D中液体为浓硫酸)。请回答:
 (1)、用A装置制取氧气的化学方程式是。(2)、实验室制取二氧化碳所用的药品是。将B、E装置组合制取并验证二氧化碳的性质,验证后加热E试管中的液体,观察的到的现象是。(3)、实验室用锌粒和稀硫酸反应制取并收集干燥的氢气,请填写所选装置导管口字母的连接顺序。18.
(1)、用A装置制取氧气的化学方程式是。(2)、实验室制取二氧化碳所用的药品是。将B、E装置组合制取并验证二氧化碳的性质,验证后加热E试管中的液体,观察的到的现象是。(3)、实验室用锌粒和稀硫酸反应制取并收集干燥的氢气,请填写所选装置导管口字母的连接顺序。18.白磷、红磷都是可燃物,都可以在一定条件下燃烧.以下是利用它们的可燃性进行的三个实验,请分别回答问题.
 (1)、通过实验1可以探究燃烧的条件.烧杯中放有热水,a、b、c处分别放有药品,实验中只有a处的白磷燃烧.a与c对比;a与b对比,说明燃烧需要的条件是可燃物与氧气接触和 ,白磷燃烧的化学方程式为 .(2)、通过实验2可以测定 . 待集气瓶中的红磷熄灭,冷却后打开弹簧夹,当观察到 的现象时,可达到该实验目的.
(1)、通过实验1可以探究燃烧的条件.烧杯中放有热水,a、b、c处分别放有药品,实验中只有a处的白磷燃烧.a与c对比;a与b对比,说明燃烧需要的条件是可燃物与氧气接触和 ,白磷燃烧的化学方程式为 .(2)、通过实验2可以测定 . 待集气瓶中的红磷熄灭,冷却后打开弹簧夹,当观察到 的现象时,可达到该实验目的.
(3)、通过实验3可以验证质量守恒定律.实验前将白磷放入锥形瓶中,称量装置的总质量,引燃白磷,待反应后再称量装置总质量,发现托盘天平保持平衡.整个实验过程中气球会出现的现象是 .综合分析上述三个实验,以下说法正确的是 .(填①~⑥序号)
①实验1中的热水只起隔绝空气的作用 ②实验2中红磷可以换成木炭
③实验2若未达到实验目的,可能是由于装置气密性不好
④实验3中的气球起到了平衡瓶内外气体压强的作用
⑤实验3中的气球作用是收集产生的气体
⑥实验3锥形瓶内事先放少量细沙的作用是防止瓶底炸裂.
19. 某研究性学习小组对双氧水开展如下研究。 (1)、图1装置中反应的化学方程式为。(2)、小红同学将MnO2与水泥按一定比例混合,制作成小块状固体,加入图2装置中以方便实验结束回收二氧化锰。其中块状固体应放置在处(填“A”或“B”),其中二氧化锰的作用是。(3)、小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃。那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究。
(1)、图1装置中反应的化学方程式为。(2)、小红同学将MnO2与水泥按一定比例混合,制作成小块状固体,加入图2装置中以方便实验结束回收二氧化锰。其中块状固体应放置在处(填“A”或“B”),其中二氧化锰的作用是。(3)、小亮发现:收集的氧气占集气瓶容积的60%(空气占40%)时,能使带火星的木条复燃。那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?小亮对此展开探究。第一组实验:取5只集气瓶,编号为①、②、③、④、⑤,分别装入其总容积10%、20%、30%、40%、50%的水。用排水法收集氧气,恰好把5只集气瓶中的水排去。将带火星的木条依次插入①~⑤号瓶中,记录实验现象。
小亮在前一组实验的基础上又做了第二组和第三组实验。三组实验的数据和现象见表:
第一组
第二组
第三组
集气瓶编号
①
②
③
④
⑤
①
②
③
④
⑤
①
收集的O2占容积的体积分数(%)
10
20
30
40
50
31
33
35
37
39
34
带火星木条的状况
微亮
亮
很亮
复燃
复燃
很亮
很亮
复燃
复燃
复燃
很亮
请根据实验回答下列问题:
①收集的氧气占容积的体积分数最低为%时,可使带火星的木条复燃。
②本实验中使用带火星的木条验满氧气的方法是否可靠:(填“是”或“否”)。
③用带火星的木条直接检验双氧水受热分解产生的氧气时,往往难以复燃,这是因为在加热生成氧气的同时产生大量水蒸气所致,此时混合气体中氧气的体积分数随温度变化的曲线如图3所示。若只考虑氧气的体积分数对实验结果的影响,欲使带火星的木条复燃,应将加热双氧水的最高温度控制在℃。
四、计算题
-
20. 为测定某碳酸钙的质量分数,小明取100g盐酸放入烧杯中,然后放入碳酸钙样品12g(样品中杂质不与盐酸反应),反应充分进行,实验和实验数据如图。请计算:
 (1)、共制得气体g。(2)、碳酸钙的质量分数(请写出简明计算过程,结果保留一位小数)。
(1)、共制得气体g。(2)、碳酸钙的质量分数(请写出简明计算过程,结果保留一位小数)。