四川省资阳市2021-2022学年高二上学期期末考试化学试题
试卷更新日期:2022-02-21 类型:期末考试
一、单选题
-
1. 新能源的开发及应用是应对气候变化和优化能源结构的重要战略举措。下列选项不属于新能源的是( )A、太阳能 B、天然气 C、地热能 D、生物质能2. 下列物质中,由极性键构成的非极性分子是( )A、 B、 C、 D、3. 下列微粒的VSEPR模型与空间立体构型一致的是( )A、BF3 B、SO2 C、H2O D、SO4. 下列化学用语表达正确的是( )A、的结构式: B、甲醛分子的比例模型:
 C、基态碳原子的价电子排布图:
C、基态碳原子的价电子排布图: D、的电子式:
D、的电子式: 5. 下列有关性质的比较中,不正确的是( )A、离子半径: B、沸点: C、晶格能: D、共价键的健能:6. 反应 , 在密闭容器中达到平衡后,若要减小反应速率并提高的转化率,采取措施正确的是( )A、减小压强 B、再通入 C、降低温度 D、加入催化剂7. 下列说法正确的是( )A、铁元素位于元素周期表的ds区 B、石墨能导电,是因为晶体中含有金属键 C、中σ键和π键的数目比为6:1 D、所含元素中第一电离能最大的是O8. 下列事实能用勒夏特列原理解释的是( )A、工业上采用500℃比常温更有利于合成氨反应 B、对CO(g)+NO2(g)CO2(g)+NO(g)平衡体系加压,气体颜色变深 C、向K2Cr2O7溶液中滴加少量浓H2SO4 , 溶液橙色加深[] D、H2O2溶液中滴入FeCl3溶液后产生气泡速率变快9. 向CuSO4溶液中滴加氨水至过量,得到深蓝色透明溶液。下列叙述不正确的是( )A、反应过程中先生成蓝色沉淀,后沉淀溶解 B、溶液呈深蓝色是由于生成了[Cu(NH3)4]2+ C、反应的离子方程式为Cu2++4NH3·H2O=[Cu(NH3)4]2++4H2O D、若继续向深蓝色溶液中加入乙醇,将析出深蓝色晶体CuSO4·5H2O10. 下列事实的描述或化学用语表达不正确的是( )A、溶液与稀混合出现浑浊的离子方程式为: B、甲烷的燃烧热为890.3 , 则甲烷燃烧的热化学方程式为: C、稀溶液中, , 则稀与稀溶液反应生成1液态水,放出的热量大于57.3 D、反应在高温时能自发进行,则该反应的 ,11. 下列叙述正确的是( )A、吸热反应都必须在加热条件下才能发生 B、升高温度,可逆反应的正逆反应速率不一定同时增大 C、恒容下充入稀有气体可增大反应物分子间有效碰撞的频率 D、其他条件不变,X(g)+Y(g)Z(g)的投料比越大,Y的转化率越大12. 下列说法不正确的是( )A、金属键的本质是金属阳离子与自由电子间的相互作用 B、H2O的热稳定性大于H2S,这与H2O分子间易形成氢键无关 C、
5. 下列有关性质的比较中,不正确的是( )A、离子半径: B、沸点: C、晶格能: D、共价键的健能:6. 反应 , 在密闭容器中达到平衡后,若要减小反应速率并提高的转化率,采取措施正确的是( )A、减小压强 B、再通入 C、降低温度 D、加入催化剂7. 下列说法正确的是( )A、铁元素位于元素周期表的ds区 B、石墨能导电,是因为晶体中含有金属键 C、中σ键和π键的数目比为6:1 D、所含元素中第一电离能最大的是O8. 下列事实能用勒夏特列原理解释的是( )A、工业上采用500℃比常温更有利于合成氨反应 B、对CO(g)+NO2(g)CO2(g)+NO(g)平衡体系加压,气体颜色变深 C、向K2Cr2O7溶液中滴加少量浓H2SO4 , 溶液橙色加深[] D、H2O2溶液中滴入FeCl3溶液后产生气泡速率变快9. 向CuSO4溶液中滴加氨水至过量,得到深蓝色透明溶液。下列叙述不正确的是( )A、反应过程中先生成蓝色沉淀,后沉淀溶解 B、溶液呈深蓝色是由于生成了[Cu(NH3)4]2+ C、反应的离子方程式为Cu2++4NH3·H2O=[Cu(NH3)4]2++4H2O D、若继续向深蓝色溶液中加入乙醇,将析出深蓝色晶体CuSO4·5H2O10. 下列事实的描述或化学用语表达不正确的是( )A、溶液与稀混合出现浑浊的离子方程式为: B、甲烷的燃烧热为890.3 , 则甲烷燃烧的热化学方程式为: C、稀溶液中, , 则稀与稀溶液反应生成1液态水,放出的热量大于57.3 D、反应在高温时能自发进行,则该反应的 ,11. 下列叙述正确的是( )A、吸热反应都必须在加热条件下才能发生 B、升高温度,可逆反应的正逆反应速率不一定同时增大 C、恒容下充入稀有气体可增大反应物分子间有效碰撞的频率 D、其他条件不变,X(g)+Y(g)Z(g)的投料比越大,Y的转化率越大12. 下列说法不正确的是( )A、金属键的本质是金属阳离子与自由电子间的相互作用 B、H2O的热稳定性大于H2S,这与H2O分子间易形成氢键无关 C、 的沸点高于
的沸点高于 是因为其范德华力更大
D、离子键无方向性和饱和性,而共价键有方向性和饱和性
13. 表示阿伏加德罗常数的值,下列说法正确的是( )A、18g冰中含有的氢键数目为4 B、标况下与完全反应时转移的电子数目为2 C、32g环状(
是因为其范德华力更大
D、离子键无方向性和饱和性,而共价键有方向性和饱和性
13. 表示阿伏加德罗常数的值,下列说法正确的是( )A、18g冰中含有的氢键数目为4 B、标况下与完全反应时转移的电子数目为2 C、32g环状( )分子中含有的键数目为
D、12g金刚石与石墨烯(
)分子中含有的键数目为
D、12g金刚石与石墨烯( )的混合物中含有的碳原子数目为1.5
14. 下图表示有关化学反应过程与能量变化的关系,根据图像判断正确的是( )
)的混合物中含有的碳原子数目为1.5
14. 下图表示有关化学反应过程与能量变化的关系,根据图像判断正确的是( )

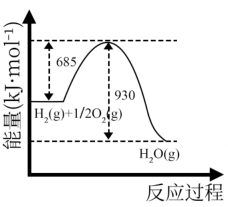
 A、根据图像Ⅰ,金刚石比石墨更稳定 B、根据图像Ⅱ, C、根据图像Ⅲ,的燃烧热为245 kJ∙mol−1 D、根据图像Ⅳ,b可能为使用催化剂的曲线15. 下列理论解释不符合实验事实的是( )
A、根据图像Ⅰ,金刚石比石墨更稳定 B、根据图像Ⅱ, C、根据图像Ⅲ,的燃烧热为245 kJ∙mol−1 D、根据图像Ⅳ,b可能为使用催化剂的曲线15. 下列理论解释不符合实验事实的是( )选项
实验事实
理论解释
A
的熔点高于
的相对分子质量更大
B
和都能溶于溶液
和在元素周期表中是对角线关系,性质相似
C
酸性:
中非羟基氧原子个数更多,中心原子的正电性更高
D
在苯中的溶解度比在水中大
和苯都是非极性分子,而是极性分子
A、A B、B C、C D、D16. 下列叙述不正确的是( )A、氯化钠晶胞中阴阳离子的配位数都为6 B、由非金属元素构成的化合物都是共价化合物 C、区分晶体和非晶体最可靠的科学方法是X-射线衍射实验 D、干冰晶胞中,每个分子周围距离最近且相等的分子有12个17. 一定条件下的反应aA(g)+bB(g)cC(g)+dD(s) ΔH=QkJ·mol−1 , 反应过程中化学平衡常数(K)与温度,C的百分含量与时间的关系如图所示,以下说法不正确的是( ) A、Q>0 B、a+b<c C、K越大,A的转化率越大 D、达到平衡后,增加少量D,平衡逆向移动18. 短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4。下列说法正确的是( )A、Y和Z可能形成空间构型为三角锥形的化合物 B、若形成化合物 , 各原子均达到8电子稳定结构的分子 C、X、Y、Z的第一电离能大小顺序为 D、W、Y、Z最简单氢化物的稳定性一定是19. 下列实验设计能达到预期目的的是( )
A、Q>0 B、a+b<c C、K越大,A的转化率越大 D、达到平衡后,增加少量D,平衡逆向移动18. 短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4。下列说法正确的是( )A、Y和Z可能形成空间构型为三角锥形的化合物 B、若形成化合物 , 各原子均达到8电子稳定结构的分子 C、X、Y、Z的第一电离能大小顺序为 D、W、Y、Z最简单氢化物的稳定性一定是19. 下列实验设计能达到预期目的的是( )A
B
C
D
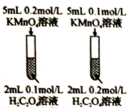
实验



结论
其他条件一定,浓度越大,反应速率越快
恒压漏斗可减小测定H2体积的实验误差
其他条件一定,压强越大,NO2的体积分数越大
酶的催化效率大于硫酸
A、A B、B C、C D、D20. 恒温下容积为2L的密闭容器中,发生反应 , 随时间的变化如表,则下列说法正确的是( )时间/
0
1
2
3
4
5
0.20
0.16
0.13
0.11
0.08
0.08
A、用表示0~4内该反应的平均速率为0.005 B、当混合气体的平均摩尔质量不变时,该反应不一定达到平衡 C、平衡时再通入 , 反应物活化分子百分数增大 D、平衡时若升高温度,会减少21. 下列关于各图像的解释或得出的结论不正确的是( ) A、由甲图可知,反应在时刻可能改变了压强或使用了催化剂 B、由乙图可知,反应在m点可能达到了平衡状态 C、由丙图可知,反应过程中的点是C点 D、由丁图可知,交点A表示反应一定处于平衡状态,此时
A、由甲图可知,反应在时刻可能改变了压强或使用了催化剂 B、由乙图可知,反应在m点可能达到了平衡状态 C、由丙图可知,反应过程中的点是C点 D、由丁图可知,交点A表示反应一定处于平衡状态,此时二、多选题
-
22. 下列关于配合物的说法正确的是( )A、基态原子核外电子的空间运动状态有17种 B、中含有离子键、共价健和配位键 C、该配合物中提供空轨道形成配位键 D、1该配合物和足量溶液反应,能产生3沉淀
三、填空题
-
23. 回答下列问题:(1)、现有六种物质:①碘晶体②晶体硅③晶体④晶体⑤晶体⑥铁,其中属于原子晶体的化合物是(填序号);③在熔化时破坏的作用力为。(2)、①②③
 ④金刚石,这四种物质中碳原子采取杂化的是(填序号);乳酸分子中有个手性碳。 24. 回答下列问题:(1)、在101和298K下,异构化反应过程的能量变化如图所示:
④金刚石,这四种物质中碳原子采取杂化的是(填序号);乳酸分子中有个手性碳。 24. 回答下列问题:(1)、在101和298K下,异构化反应过程的能量变化如图所示:
该异构化反应的 , 使用催化剂(选填“能”“不能”)改变该反应的。
(2)、肼()又称联氨,在航空航天方面应用广泛,可用作火箭燃料。已知键、键的键能分别为391、497 , 与反应的能量变化如图所示: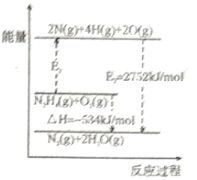
中键的键能为。请写出一定条件下,与反应的热化学方程式为。
四、综合题
-
25.(1)、I.分别取40mL 0.50mol/L盐酸与40mL 0.55mol/L氢氧化钠溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热△H。请回答下列问题:
本实验除烧杯、量筒、环形玻璃搅拌棒外还缺少的玻璃仪器名称为 , 大小烧杯间需要填满碎泡沫塑料的目的是。(2)、若某同学通过该实验测定出中和热偏大,请分析可能的原因是____(填序号)。A、用量筒量取盐酸时仰视读数 B、分多次将溶液倒入盛有盐酸的小烧杯中 C、将盐酸错取为等浓度的醋酸(3)、Ⅱ.为探究化学反应速率的影响因素,设计的实验方案如下表:(已知溶液、溶液、淀粉三种溶液混合,无明显现象,滴入溶液后溶液变蓝)向烧杯中加入的试剂及用量/
0.1溶液
0.1溶液
0.1溶液
淀粉溶液
时间/s
①
25℃
20.0
10.0
5.0
1.0
0.0
②
40℃
20.0
10.0
5.0
1.0
0.0
③
25℃
20.0
5.0
5.0
1.0
V
写出混合溶液中滴入溶液反应的离子方程式为。
(4)、表中的V= , 、、由小到大的顺序为。(5)、对比实验①②可推测实验结论为。26. 回答下列问题:(1)、常温下是一种无色气体,可与一定量的水形成 , 在一定条件下可发生如图所示转化:
①H、O、B中电负性最强的元素是;基态B原子核外能量最高的电子,其电子云的轮廓图形状为。
②中含有的化学键为;与形成 , 则键的键角将变小,原因是。
(2)、B可以与金属形成、、等多种硼化物,金属位于周期表中的位置为 , 其基态原子的外围电子排布式为。(3)、三价B易形成、等配离子,的空间立体构型为 , 的一种阳离子等电子体为。(4)、以天然硼砂为原料,经过一系列反应可以制得:
请写出由制得的化学方程式;有一种晶胞结构与金刚石的晶胞(如图)相似,称为立方 , 可用作耐磨材料的新型无机材料。若晶胞的边长为 , 则晶胞的密度为(用含a、的计算式表示)。
27. 甲醇是重要的化工原料,利用合成气(、、)在催化剂的作用下合成甲醇,可能发生的反应如下:Ⅰ.
Ⅱ.
(1)、已知某反应Ⅲ的化学平衡常数 , 请结合反应Ⅰ、Ⅱ计算反应Ⅲ的 , 若用含、的式子表示该反应的平衡常数 , 则。(2)、在容器初始体积和温度相同的条件下,恒容容器甲和恒压容器乙中均充入和发生上述反应Ⅱ,达到平衡后的转化率:甲乙(选填“>”“<”或“=”)。(3)、若上述反应Ⅰ在恒温、恒压容器中进行,下列可以判断该反应达到平衡状态的是____(填字母)。A、 B、混合气体的压强不变 C、与的比值不变 D、混合气体的密度不变 E、单位时间内断裂2个键的同时断裂3个键(4)、已知在一定条件下,向1L恒容容器中充入1和3发生上述反应Ⅰ,达到平衡状态时的转化率为50%,反应放出热量。①此时产物的体积分数为;该温度下,平衡常数。
②若继续向容器中充入0.5和0.5 , 其他条件不变时平衡移动(选填“正向”“逆向”或“不”)。
③若起始投料方式改为充入1和1 , 达到平衡状态时反应吸收热量。
-