湖南省怀化市2021-2022学年高二上学期期末考试化学试题
试卷更新日期:2022-02-21 类型:期末考试
一、单选题
-
1. 化学在日常生活和生产中有着重要的应用,下列说法不正确的是( )A、泡沫灭火器中的Al2(SO4)3溶液应贮存在玻璃筒内 B、BaSO4在医学上用作钡餐所以Ba2+无毒对人体无害 C、新能源汽车的推广与使用能减少氮氧化合物对环境的污染 D、工业上通常采用铁触媒、400℃~500℃和10MPa~30MPa的条件来合成氨2. 下列化学用语不正确的是( )A、醋酸的电离:CH3COOHCH3COO-+H+ B、硫酸氢钠在水中的电离:NaHSO4=Na++H++SO C、碳酸钙的溶解:CaCO3(s)Ca2++(aq)+CO(aq) D、HS-的水解:HS-+H2OS2-+H3O+3. 镁和卤素单质(X2)反应的相对能量变化如图所示,下列说法正确的是( )
 A、热稳定性:MgF2>MgCl2>MgBr2>MgI2 B、22.4LF2(g)与足量的Mg充分反应,放热1124kJ C、电解熔融MgCl2要放出热量 D、由图中信息可知:MgBr2(s)+Cl2(g)=MgCl2(s)+Br2(l) ΔH=−117 kJ∙mol−14. 下列说法正确的是( )
A、热稳定性:MgF2>MgCl2>MgBr2>MgI2 B、22.4LF2(g)与足量的Mg充分反应,放热1124kJ C、电解熔融MgCl2要放出热量 D、由图中信息可知:MgBr2(s)+Cl2(g)=MgCl2(s)+Br2(l) ΔH=−117 kJ∙mol−14. 下列说法正确的是( ) A、利用I装置制无水AlCl3 B、装置II为酸式滴定管,其读数为12.20mL C、装置III为牺牲阳极法防护钢闸门 D、装置IV为铅酸蓄电池,充电时阴极反应式为PbSO4+2e-=Pb+SO5. 执法交警最常用的一种酒精检测仪的工作原理示意图如图所示,其反应原理为CH3CH2OH+O2=CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法不正确的是( )
A、利用I装置制无水AlCl3 B、装置II为酸式滴定管,其读数为12.20mL C、装置III为牺牲阳极法防护钢闸门 D、装置IV为铅酸蓄电池,充电时阴极反应式为PbSO4+2e-=Pb+SO5. 执法交警最常用的一种酒精检测仪的工作原理示意图如图所示,其反应原理为CH3CH2OH+O2=CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法不正确的是( ) A、电解质溶液中的移向a电极 B、b为正极,电极反应式为O2+2H2O+4e-=4OH- C、呼出气体中酒精含量越高,微处理器中通过的电流越大 D、a极上的电极反应式为CH3CH2OH+H2O-4e-=CH3COOH+4H+6. 处理CO2的一种重要方法是将CO2还原,所涉及的反应为CO2(g)+4H2(g)CH4(g)+2H2O(g),若平衡后将温度从300℃升至400℃,保持其他条件不变,反应重新达到平衡时,CO2的体积分数增加。下列有关判断不正确的是( )A、该反应的ΔH<0 B、升高温度正反应速率增大,逆反应速率也增大且增加的倍数更大 C、升高温度化学平衡常数K增大 D、升高温度CH4的产率降低7. 某汽车尾气净化装置可使有毒气体CO、NO2在一定条件下发生反应4CO(g)+2NO2(g)4CO2(g)+N2(g) ΔH=−1200 kJ∙mol−1 , 从而转化为无毒气体。温度不同(T2>T1)、其他条件相同时,下列图示变化关系不正确的是( )A、
A、电解质溶液中的移向a电极 B、b为正极,电极反应式为O2+2H2O+4e-=4OH- C、呼出气体中酒精含量越高,微处理器中通过的电流越大 D、a极上的电极反应式为CH3CH2OH+H2O-4e-=CH3COOH+4H+6. 处理CO2的一种重要方法是将CO2还原,所涉及的反应为CO2(g)+4H2(g)CH4(g)+2H2O(g),若平衡后将温度从300℃升至400℃,保持其他条件不变,反应重新达到平衡时,CO2的体积分数增加。下列有关判断不正确的是( )A、该反应的ΔH<0 B、升高温度正反应速率增大,逆反应速率也增大且增加的倍数更大 C、升高温度化学平衡常数K增大 D、升高温度CH4的产率降低7. 某汽车尾气净化装置可使有毒气体CO、NO2在一定条件下发生反应4CO(g)+2NO2(g)4CO2(g)+N2(g) ΔH=−1200 kJ∙mol−1 , 从而转化为无毒气体。温度不同(T2>T1)、其他条件相同时,下列图示变化关系不正确的是( )A、 B、
B、 C、
C、 D、
D、 8. 下列实验所得结论不正确的是( )
8. 下列实验所得结论不正确的是( )选项
实验
结论
A
将0.1 mol∙L−1氨水稀释成0.01 mol∙L−1 , 测得pH由11.1变成10.6
稀释后,NH3·H2O的电离程度减小
B
室温下,用pH计分别测定同浓度的NaClO和CH3COONa溶液的pH,NaClO溶液pH大
酸性:HClO<CH3COOH
C
向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,有白色沉淀生成,溶液红色变浅
证明纯碱溶液呈碱性是由CO水解引起的
D
在AgCl悬浊液中滴入数滴0.1 mol∙L−1 KI溶液,生成黄色沉淀
同温下溶解度:AgCl>AgI
A、A B、B C、C D、D9. 已知:H2R为二元弱酸,25℃时,在一定体积某浓度的H2R溶液中逐渐加入NaOH固体(忽略溶液体积的变化),H2R、HR-、R2-三者物质的量浓度随溶液pH变化的关系如图所示,下列叙述不正确的是( ) A、H2R一级电离平衡常数KR1=10-1.3 B、等体积、等浓度的NaOH溶液与H2R溶液混合后,所得溶液能促进水的电离 C、pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-) D、等浓度的NaOH溶液与H2R溶液按体积比1:2混合,所得溶液呈酸性
A、H2R一级电离平衡常数KR1=10-1.3 B、等体积、等浓度的NaOH溶液与H2R溶液混合后,所得溶液能促进水的电离 C、pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-) D、等浓度的NaOH溶液与H2R溶液按体积比1:2混合,所得溶液呈酸性二、多选题
-
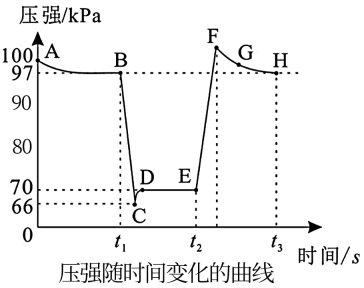
10. 下列各组离子在相应条件下可能大量共存的是( )A、能使pH试纸变蓝的溶液中:CO、K+、Cl-、Na+ B、由水电离产生的c(H+)=1×10−10mol∙L−1的溶液中:NO、Mg2+、Na+、SO C、在=1×1010的溶液中:NH、Fe2+、Cl-、NO D、加水稀释pH增大的溶液:Na+、K+、Cl-、CO11. 利用传感技术可以探究压强对2NO2(g)⇌N2O4(g)化学平衡移动的影响。在室温、100 kPa条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时刻迅速移动活塞至一定位置,并保持活塞位置不变,测定针筒内气体压强变化如图所示。下列说法正确的是( )
 A、t1时刻的操作是向内推活塞 B、E点到H点的过程中,NO2的物质的量先增大后减小 C、E,H两点对应的正反应速率大小为v(H)>v(E) D、B,E两点气体的平均相对分子质量大小为M(B)>M(E)12. 工业上可采用CH3OHCO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物质用*标注。下图为计算机模拟的各步反应的能量变化示意图,下列说法正确的是( )
A、t1时刻的操作是向内推活塞 B、E点到H点的过程中,NO2的物质的量先增大后减小 C、E,H两点对应的正反应速率大小为v(H)>v(E) D、B,E两点气体的平均相对分子质量大小为M(B)>M(E)12. 工业上可采用CH3OHCO+2H2的方法来制取高纯度的CO和H2。我国学者采用量子力学方法,通过计算机模拟,研究了在钯基催化剂表面上甲醇制氢的反应历程,其中吸附在钯催化剂表面上的物质用*标注。下图为计算机模拟的各步反应的能量变化示意图,下列说法正确的是( ) A、温度较低时不利于该反应自发进行 B、决速步骤的能垒(活化能)为53.6kJ/mol C、过渡态II的稳定性小于过渡态V D、由CH3OH*(g)经过渡态I生成CH3O*+H*的过程要释放能量,断裂极性共价键
A、温度较低时不利于该反应自发进行 B、决速步骤的能垒(活化能)为53.6kJ/mol C、过渡态II的稳定性小于过渡态V D、由CH3OH*(g)经过渡态I生成CH3O*+H*的过程要释放能量,断裂极性共价键三、填空题
-
13.(1)、I.已知:①2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) ΔH=−768.2 kJ∙mol−1
②2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g) ΔH=+116.0 kJ∙mol−1
则Cu2S(s)+O2(g)=2Cu(s)+SO2(g) ΔH=。(2)、II.如图所示,E为浸过含酚酞的Na2SO4溶液的滤纸;A、B均为铂片,压在滤纸两端;R、S为电源的电极;M、N是用多微孔的Ni制成的电极,在碱溶液中可视为惰性电极:G为电流计;K为开关;C、D和电解池中都充满浓KOH溶液。若在滤纸中央滴一滴紫色的KMnO4溶液,将开关K打开,接通电源一段时间后,C、D中有气体产生。
回答下列问题:
R为(填“正”或“负”)极。
(3)、通电一段时间后,M极附近溶液的pH(填“变大”、“变小”或“不变”);B极区的电极反应式为。(4)、滤纸上的紫色点向(填“A”或“B”)方向移动。(5)、通电一段时间后,C、D中的气体产生到一定量时,切断外电源并接通开关K,C、D中的气体逐渐减少,C中的电极反应式为。14. 钛及其化合物作用重要,尤其氧化钛、四氧化钛、钛酸钡等应用更广。回答下列问题:(1)、基态钛原子的价层电子排布式为。(2)、二氧化钛是世界上最白的物质,1g二氧化钛可以把450多平方厘米的面积涂得雪白,是调制白油漆的最好颜料。基态Ti4+中核外电子占据的原子轨道数为个。(3)、四氯化钛是种有趣的液体,在潮湿空气中水解生成白色的二氧化钛水凝胶,军事上利用四氯化钛的这种“怪脾气”制造烟雾剂。写出四氯化钛水解的化学方程式。(4)、Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。LiBH4由Li+和BH构成,其中BH的空间构型为;B原子的杂化轨道类型为。(5)、Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下:元素
Mn
Fe
电离能/kJ∙mol−1
I1
717
759
I2
1509
1561
I3
3248
2957
锰元素位于第周期族区;比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是。
15. 高纯硫酸锰是合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如图所示。
已知:①“滤渣1”含有S和SiO2;
②相关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子
Mn2+
Fe2+
Fe3+
Al3+
Mg2+
Zn2+
Ni2+
开始沉淀的pH
8.1
6.3
1.5
3.4
8.9
6.2
6.9
沉淀完全的pH
10.1
8.3
2.8
4.7
10.9
8.2
8.9
回答下列问题:
(1)、“氧化”中添加适量MnO2的作用是。(2)、“除杂1”的目的是除去Zn2+和Ni2+ , 则“滤渣3”的主要成分是(写化学式)。(3)、“除杂2”的目的是除去Mg2+。若1L溶液中Mg2+的初始浓度为0.1mol/L,现欲将Mg2+沉淀完全(即剩余离子浓度小于1×10-5mol/L),则至少需要加入MnF2固体mol(忽略加入固体时溶液体积的变化)。(已知:Ksp(MgF2)=4.0×10-9;MnF2为易溶的强电解质。)(4)、写出“沉锰”的离子方程式。(5)、II.一定量的CO2与足量的碳在体积可变的恒压(P0)密闭容器中反应:C(s)+CO2(g)2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示:
650℃时,反应达平衡后CO2的转化率为。
(6)、T℃时该反应的平衡常数Kp=(Kp是以分压表示的平衡常数,分压=总压×体积分数)16.(1)、I.醋酸是一种常见的弱酸,回答下列问题:
下列措施可以使醋酸溶液中CH3COOH电离程度增大的是_______(填字母序号)。A、升温 B、通入HCl气体 C、加入NaOH固体 D、加入NaHSO4固体I.醋酸是一种常见的弱酸,回答下列问题:下列措施可以使醋酸溶液中CH3COOH电离程度增大的是________(填字母序号)。
(2)、用0.1 mol∙L−1NaOH溶液分别滴定体积均为20mL、浓度均为0.1 mol∙L−1的盐酸和醋酸溶液,滴定过程中溶液pH随加入NaOH溶液体积变化的曲线如图。请回答:
滴定盐酸的曲线是(填“I”或“II”);M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是。
(3)、II.国家标准规定葡萄酒中SO2的最大含量为0.25g∙L−1。某兴趣小组用图1所示装置(夹持装置已略去)收集某葡萄酒中的SO2 , 然后对其含量进行测定。
向B中加入300.00mL葡萄酒和适量稀硫酸,加热使SO2全部逸出,并与C中H2O2完全反应,C中反应的离子方程式为。
(4)、除去C中剩余的H2O2 , 然后用0.0900 mol∙L−1的NaOH标准溶液进行滴定,NaOH标准溶液应盛装在图2中的(填“①”或“②”)中;如用酚酞作指示剂,则滴定终点的现象B为。(5)、滴定测得,消耗NaOH标准溶液25.00mL,则该葡萄酒中SO2的含量为g·L-1。17. 回答下列问题:(1)、基态Cr原子外围电子排布图为;核外有种不同运动状态的电子。(2)、CH3CH2OH与H2O可以任意比例互溶,除因为它们都是分子(极性或非极性)外,还因为。(3)、纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的实例如图所示。化合物甲分子中采取sp2方式杂化的碳原子个数为;化合物乙中各元素的电负性由大到小的顺序为。 (4)、一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(COCl2):2CHCl3+O2→2HCl+2COCl2 , 其中光气(COCl2)分子的立体构型为。(5)、丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图所示。
(4)、一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(COCl2):2CHCl3+O2→2HCl+2COCl2 , 其中光气(COCl2)分子的立体构型为。(5)、丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图所示。
该分子中含有个σ键。