江苏省扬州市邗江区2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-02-17 类型:期末考试
一、单选题
-
1. 2022年北京和张家口联合举办冬奥会,为办成绿色奥运,下列措施不可行的是( )A、大力发展公共交通,提倡绿色出行 B、实施太阳能灯亮化,发展新型能源 C、大量燃放烟花鞭炮,增强奥运气氛 D、开展垃圾分类收集,积极回收利用2. 成语是中华民族灿烂文化的瑰宝。下列成语中涉及化学变化的是( )A、铁杵磨针 B、聚沙成塔 C、火上浇油 D、木已成舟3. 微量元素在人体中起着极其重要的作用,下列属于人体所需的微量元素是( )A、O B、Fe C、C D、Ca4. 下列物质,由原子直接构成的是( )A、水 B、铜 C、氢气 D、氯化钠5. 空气成分中,体积分数约占78%的是( )
A、氮气 B、氧气 C、二氧化碳 D、稀有气体6. 下列标识中,表示“禁止烟火”的是( )A、 B、
B、 C、
C、 D、
D、 7. 生活常识彰显化学素养。下列说法中不正确的是( )A、煮沸的汤比煮沸的水温度更高 B、溶液一定是混合物 C、洗洁精洗去餐具上油污属于溶解现象 D、钢的含碳量较生铁低,韧性更好8. 把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )A、花生油 B、面粉 C、泥土 D、食盐9. 下列物质不属于合金的是( )A、青铜 B、氧化铁 C、不锈钢 D、生铁10. 下列有关实验基本操作,正确的是( )A、滴加液体
7. 生活常识彰显化学素养。下列说法中不正确的是( )A、煮沸的汤比煮沸的水温度更高 B、溶液一定是混合物 C、洗洁精洗去餐具上油污属于溶解现象 D、钢的含碳量较生铁低,韧性更好8. 把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )A、花生油 B、面粉 C、泥土 D、食盐9. 下列物质不属于合金的是( )A、青铜 B、氧化铁 C、不锈钢 D、生铁10. 下列有关实验基本操作,正确的是( )A、滴加液体 B、倾倒液体
B、倾倒液体  C、取固体药品
C、取固体药品  D、量取液体
D、量取液体  11. 化学是一门实验科学,下列实验现象描述不正确的是( )A、铁丝在氧气中燃烧火星四射 B、铜丝放入稀盐酸中有气泡产生 C、二氧化碳通入澄清石灰水变浑浊 D、碳酸氢铵加热固体逐渐减少12. 锌是人体必需的微量元素。一种锌原子的原子核内有 30 和质子,36 个中子,则该原子核外电子数为( )A、4 B、30 C、36 D、6613. 下列关于物质的性质和用途说法不正确的是( )A、二氧化碳用于人工降雨,是利用它升华时吸热 B、铝大量用于做导线,是因为铝导电性好且资源丰富,价格便宜 C、稀有气体充入霓虹灯,是利用稀有气体通电能发出不同颜色的光 D、氧气用于火箭发射,是利用氧气的可燃性14. 下列化学方程式书写正确的是( )A、Cu+AgNO3=CuNO3+Ag B、6HCl+2Fe=2FeCl3+3H2↑ C、S+O2SO2 D、CO+CuO=Cu+CO215. 石灰氮遇水反应的化学方程式为CaCN2 +3H2O=CaCO3+2X,则X的化学式为( )A、NO B、N2 C、CO2 D、NH316. 连花清瘟胶囊含有绿原酸,下列有关绿原酸(C16H18O9)的说法正确的是( )A、绿原酸是氧化物 B、绿原酸的相对分子质量是354g C、绿原酸中氢元素的质量分数最大 D、绿原酸是由三种元素组成17. 肼是一种无色油状液体。点燃时,迅速燃烧,放出大量的热,因此常用做火箭燃料。肼发生燃烧反应的微观示意图如下:
11. 化学是一门实验科学,下列实验现象描述不正确的是( )A、铁丝在氧气中燃烧火星四射 B、铜丝放入稀盐酸中有气泡产生 C、二氧化碳通入澄清石灰水变浑浊 D、碳酸氢铵加热固体逐渐减少12. 锌是人体必需的微量元素。一种锌原子的原子核内有 30 和质子,36 个中子,则该原子核外电子数为( )A、4 B、30 C、36 D、6613. 下列关于物质的性质和用途说法不正确的是( )A、二氧化碳用于人工降雨,是利用它升华时吸热 B、铝大量用于做导线,是因为铝导电性好且资源丰富,价格便宜 C、稀有气体充入霓虹灯,是利用稀有气体通电能发出不同颜色的光 D、氧气用于火箭发射,是利用氧气的可燃性14. 下列化学方程式书写正确的是( )A、Cu+AgNO3=CuNO3+Ag B、6HCl+2Fe=2FeCl3+3H2↑ C、S+O2SO2 D、CO+CuO=Cu+CO215. 石灰氮遇水反应的化学方程式为CaCN2 +3H2O=CaCO3+2X,则X的化学式为( )A、NO B、N2 C、CO2 D、NH316. 连花清瘟胶囊含有绿原酸,下列有关绿原酸(C16H18O9)的说法正确的是( )A、绿原酸是氧化物 B、绿原酸的相对分子质量是354g C、绿原酸中氢元素的质量分数最大 D、绿原酸是由三种元素组成17. 肼是一种无色油状液体。点燃时,迅速燃烧,放出大量的热,因此常用做火箭燃料。肼发生燃烧反应的微观示意图如下:
下列说法不正确的是( )
A、肼分子式为N2H4 B、肼中氮元素与氢元素的质量比为7:1 C、两种生成物均为化合物 D、参加反应的O2与生成的N2的分子数之比为1:118. 将 2.4g 含镁的混合物与足量盐酸反应,生成氢气质量为 0.18g,则混入的另一种物质不可能是( )A、Al B、Fe C、Cu D、Zn19. 下列实验操作能达到实验目的的是( )选项
实验目的
实验操作
A
鉴别H2和CH4
分别点燃,在火焰上方罩一干冷烧杯
B
除去CO2中的少量CO
点燃
C
鉴别空气和氧气
将燃着的木条伸入集气瓶中
D
除去CuSO4溶液中的少量FeSO4
加入足量铜粉
A、A B、B C、C D、D20. 下图是利用缺铁性氧化物[Fe(1-y)O]进行CO2再资源化研究的示意图。下列说法不正确的是( ) A、反应过程中不需要添加 Fe3O4 B、反应②为分解反应 C、反应①提高了铁的氧化物中铁的质量分数 D、整个转化反应的化学方程式可表示为:CO2C+O2
A、反应过程中不需要添加 Fe3O4 B、反应②为分解反应 C、反应①提高了铁的氧化物中铁的质量分数 D、整个转化反应的化学方程式可表示为:CO2C+O2二、填空题
-
21. 化学与生活
 (1)、电视节目《荒野求生》中的生命吸管(如图所示)是一种将污水净化为饮用水的吸管装置,可以除去 99.3% 的细菌和病毒,但难以除去汞等金属离子。野外环境中很多地下水含较多钙离子(写出离子符号)称为硬水;生命吸管中活性炭(“能”或“不能”)使硬水软化。家庭中使硬水软化一般采取方法。(2)、配制1000克0.9%的生理盐水需用到水,其中水作为(选填“溶质”或“溶剂”或“催化剂”或“还原剂”),需要水的质量 , 配制时使用玻璃棒的作用是。(3)、下列固体物质用水即可鉴别的组别是(填字母序号)。
(1)、电视节目《荒野求生》中的生命吸管(如图所示)是一种将污水净化为饮用水的吸管装置,可以除去 99.3% 的细菌和病毒,但难以除去汞等金属离子。野外环境中很多地下水含较多钙离子(写出离子符号)称为硬水;生命吸管中活性炭(“能”或“不能”)使硬水软化。家庭中使硬水软化一般采取方法。(2)、配制1000克0.9%的生理盐水需用到水,其中水作为(选填“溶质”或“溶剂”或“催化剂”或“还原剂”),需要水的质量 , 配制时使用玻璃棒的作用是。(3)、下列固体物质用水即可鉴别的组别是(填字母序号)。a.蔗糖、食盐 b.氢氧化钠、硝酸铵 c.二氧化锰和碳粉
(4)、光催化分解水的过程是将光能转化为能。电解水制氢气时,与直流电源极相连的电极上产生H2 , 电解水的原理用化学方程式表示为。(5)、敦煌壁画色彩艳丽,矿物颜料功不可没,其蓝色源于石青[Cu3(OH)2(CO3)x]。石青中铜元素(+2价)与碳元素的质量比为(用不含x的比值表示)。22. 碳及其化合物的综合利用使世界变得更加绚丽多彩。(1)、Ⅰ、碳的多样性金刚石和C60的化学性质相似,但物理性质却存在着很大差异。原因是。
(2)、从石墨中分离出的单层石墨片(石墨烯)是目前人工制得的最薄材料,单层石墨片属于(填“单质”或“化合物”)。(3)、Ⅱ、“碳中和”的实现“碳中和”是指一定时间内CO2的排放量与吸收量基本相当。CO2的捕集、利用是实现“碳中和”的重要途径。我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。
CO2的过度排放会造成的加剧。结合生活实际,列举可为实现“碳中和”做出直接贡献的一种措施:。
(4)、工业生产中产生的CO2经吸收剂处理可实现CO2的捕集。①NaOH吸收。NaOH溶液吸收CO2生成 NaHCO3的化学方程式为。
②CaO吸收。CaC2O4在高温下分解制得疏松多孔的CaO,同时产生CO、CO2。该反应所得CO、CO2的分子个数之比为。
三、综合题
-
23. 用如下图实验装置,完成实验。
 (1)、仪器X的名称(2)、用装置A制取气体,实验结束时,为防止水槽里的水倒流,应采取的操作是。(3)、用收集的氧气做铁丝燃烧实验,应预先在集气瓶中加入少量的。(4)、用固体混合物加热制取O2 , 发生反应的化学方程式。氧气的密度比空气(填“大”或“小”)。制取干燥的氧气,选用装置(选填“A”“B”“C”);用如下图装置制取干燥CO2气体(浓硫酸可以吸水)。
(1)、仪器X的名称(2)、用装置A制取气体,实验结束时,为防止水槽里的水倒流,应采取的操作是。(3)、用收集的氧气做铁丝燃烧实验,应预先在集气瓶中加入少量的。(4)、用固体混合物加热制取O2 , 发生反应的化学方程式。氧气的密度比空气(填“大”或“小”)。制取干燥的氧气,选用装置(选填“A”“B”“C”);用如下图装置制取干燥CO2气体(浓硫酸可以吸水)。 (5)、制取干燥CO2气体,导管口a接(选填“b”或“c”);(6)、写出实验室制取CO2的化学方程式。24. 金属钛(Ti)因为常温下不与酸、碱反应等优良性能,被誉为“未来金属”。金属钛是航空、宇航、军工、电力等方面的必需原料。由钒钛磁铁矿提取金属钛的主要工艺过程如图,请根据图示回答下列问题:
(5)、制取干燥CO2气体,导管口a接(选填“b”或“c”);(6)、写出实验室制取CO2的化学方程式。24. 金属钛(Ti)因为常温下不与酸、碱反应等优良性能,被誉为“未来金属”。金属钛是航空、宇航、军工、电力等方面的必需原料。由钒钛磁铁矿提取金属钛的主要工艺过程如图,请根据图示回答下列问题: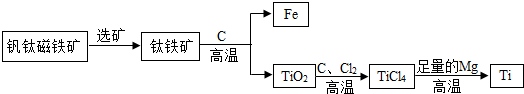
查阅资料:①钛在高温下能与空气中氧气反应;
②金属钛有一定的抗腐蚀性能,浓度小于5%的稀盐酸不和钛反应
(1)、钒钛磁铁矿的主要成分是FeTiO3(钛酸亚铁),其中钛的化合价为价。(2)、TiO2、炭粉混合在高温条件下通入氯气得TiCl4和一种可燃性有毒气体,该步骤发生反应的化学方程式为:。(3)、在氩气的气氛下,用过量的镁在加热条件下与TiCl4反应制得金属钛。①此反应的化学方程式为:;
②此过程中,氩气的作用是;
③该步骤所得金属钛中通常混有少量的杂质是 , 提纯金属钛的主要实验步骤是:先向产物中加入足量的充分反应后,再进行(填操作名称)、洗涤、干燥得金属钛。
25. 使燃料充分燃烧是实现节能减排,低碳生活”的一种重要方法。某化学小组同学探究不同条件下蜡烛燃烧的情况。【查阅资料】蜡烛燃烧时,生成的CO2与CO的浓度比越大,蜡烛燃烧越充分。
【进行实验】利用下图装置完成实验(所用传感器分别为O2、CO、CO2浓度传感器)。

实验序号
容器情况
蜡烛位置
O2起始浓度
CO2与CO的浓度比
熄灭时O2浓度
1
敞口
(模拟通风环节)
如图a
21%
1205.1
持续稳定燃烧,保持在20.4%左右不变
2
半敞口
(模拟有烟囱的环境)
如图a
21%
1202.2
持续稳定燃烧,保持在20.3%左右不变
3
密闭
如图a
21%
223.7
约16 %
4
密闭
如图b
21%
255.6
约16 %
5
密闭
如图c
21%
270.6
约16 %
6
密闭
如图c
22%
344.9
约16 %
7
密闭
如图c
23%
x
约16 %
【解释与结论】
(1)、蜡烛燃烧时会生成CO2和CO,说明蜡烛中一定含有元素。(2)、检验蜡烛燃烧有CO2生成,可在蜡烛火焰上方罩一个内壁涂有的烧杯。(3)、对比实验2和3,蜡烛在条件下燃烧更充分(填“半敞口”或“密闭”)。(4)、对比(填实验序号),可得出“其他条件相同时,蜡烛的位置越分散,燃烧越充分”。(5)、x344.9(填“>”、“=”或“<”)。(6)、【反思与评价】综合以上实验分析,下列说法正确的是____(填字母序号)。A.蜡烛燃烧可以消耗尽密闭容器内氧气
A、蜡烛充分燃烧,可减少污染 B、实验1中氧气浓度基本不变,是因为分子在不断运动 C、燃料在氧气浓度较高的富氧空气中燃烧,能起到节能减排的作用26.(1)、(一)金属材料广泛应用于生产生活中。我国古代运用湿法炼铜,请你写出将铁放入硫酸铜溶液中发生反应的化学方程式。
(2)、铝是一种活泼金属,但常温下铝具有较强的抗腐蚀性,其原因是;(用化学方程式表示化学原理)(3)、对铁生锈的条件为铁与同时接触。为了防止铁制品生锈,应采取的措施是(写出一种)。(4)、(二)兴趣小组同学模仿工业高炉炼铁原理,用图10实验装置(加热装置已省略)探究冶炼铜的化学原理。实验操作过程如下:①将CuO加水制成糊状,用毛笔刷在试管内壁,烘干;然后在试管底部加入一定量焦炭,再向试管里通入干燥的CO2 , 此时用仪器测得CO2含量为ag/L,用气球密封试管口。②用酒精灯加热试管中的氧化铜部位一段时间,无明显现象,随后熄灭酒精灯。
③高温加热焦炭部位一段时间,停止加热,用热成像仪拍摄图1中虚线框部位,数据输出得到图2。恢复至与①相同的条件测得CO2含量为0.2ag/L。
④再次用酒精灯加热氧化铜部位,1分钟左右氧化铜固体完全变色。


操作②中实验现象说明CO2(选填“能”或“不能”)与CuO反应。
(5)、操作③中CO2含量减小的原因是。(6)、操作④中的现象是化学反应方程式为。(7)、实验结束后,一般将装置内的气体灼烧处理,目的是。(8)、由图2可知,刚停止加热后焦炭区温度降低更快,可能的原因是。(9)、(三)请根据化学方程式进行计算:用赤铁矿来炼铁时,若炼得的生铁中含5.6t铁,理论上需加入含氧化铁80%的赤铁矿的质量是多少?(写出计算过程)