江苏省南京市秦淮区2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-02-17 类型:期末考试
一、单选题
-
1. 下列变化中,属于物理变化的是( )A、面粉爆炸 B、石蜡熔化 C、醋的酿造 D、铁的冶炼2. 下列物质在氧气中可发生剧烈燃烧,火星四射,生成黑色固体的是( )A、碳 B、硫 C、镁 D、铁3. 下列金属中,熔点最高的是( )A、汞 B、钨 C、银 D、铁4. 下列实验操作正确的是( )A、氢气验纯
 B、二氧化碳验满
B、二氧化碳验满 C、取用块状固体
C、取用块状固体 D、滴加液体
D、滴加液体 5. 下列变化中,吸收热量的是( )A、硝酸铵固体溶于水 B、氢氧化钠固体溶于水 C、生石灰与水反应 D、镁与盐酸反应6. 下列物质中,属于纯净物的是( )A、磁铁矿 B、过氧化氢溶液 C、冰水混合物 D、黄铜7. 下列有关粒子结构示意图的说法中,正确的是( )
5. 下列变化中,吸收热量的是( )A、硝酸铵固体溶于水 B、氢氧化钠固体溶于水 C、生石灰与水反应 D、镁与盐酸反应6. 下列物质中,属于纯净物的是( )A、磁铁矿 B、过氧化氢溶液 C、冰水混合物 D、黄铜7. 下列有关粒子结构示意图的说法中,正确的是( ) A、①③④属于同种元素 B、②表示的粒子在化学反应中易失去电子 C、③所属的元素位于元素周期表中的第二周期 D、①③表示的都是阳离子8. 下列叙述不正确的是( )A、金刚石可用于制铅笔芯 B、氮气可用作食品保护气 C、干冰可用于人工降雨 D、汽油可用于除去衣服上的油污9. 下列有关灭火说法不正确的是( )A、隔绝氧气能达到灭火的目的 B、清除可燃物能达到灭火的目的 C、降低可燃物的着火点能达到灭火的目的 D、二氧化碳灭火器有降温和隔绝空气的作用10. 下列有关水的说法中,不正确的是( )A、水是海洋中最多的物质 B、水是一种最常用的溶剂 C、生活中通过煮沸可以降低水的硬度 D、电解水实验能够说明水是由氢气、氧气组成的11. 三硝基胺 N(NO2)3是科学家近年新发现的新型火箭燃料下列关于三硝基胺说法中不正确的是( )A、三硝基胺中氮、氧两种元素的质量比为2:3 B、1个三硝基胺分子由 4个氮原子、6个氧原子构成 C、三硝基胺的相对分子质量是152 D、三硝基胺中氧元素的质量分数大于氮元素的质量分数12. 甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示,下列说法正确的是( )
A、①③④属于同种元素 B、②表示的粒子在化学反应中易失去电子 C、③所属的元素位于元素周期表中的第二周期 D、①③表示的都是阳离子8. 下列叙述不正确的是( )A、金刚石可用于制铅笔芯 B、氮气可用作食品保护气 C、干冰可用于人工降雨 D、汽油可用于除去衣服上的油污9. 下列有关灭火说法不正确的是( )A、隔绝氧气能达到灭火的目的 B、清除可燃物能达到灭火的目的 C、降低可燃物的着火点能达到灭火的目的 D、二氧化碳灭火器有降温和隔绝空气的作用10. 下列有关水的说法中,不正确的是( )A、水是海洋中最多的物质 B、水是一种最常用的溶剂 C、生活中通过煮沸可以降低水的硬度 D、电解水实验能够说明水是由氢气、氧气组成的11. 三硝基胺 N(NO2)3是科学家近年新发现的新型火箭燃料下列关于三硝基胺说法中不正确的是( )A、三硝基胺中氮、氧两种元素的质量比为2:3 B、1个三硝基胺分子由 4个氮原子、6个氧原子构成 C、三硝基胺的相对分子质量是152 D、三硝基胺中氧元素的质量分数大于氮元素的质量分数12. 甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示,下列说法正确的是( ) A、甲的溶解度比乙小 B、将等质量甲、乙的两种溶液分别由t2℃降温至 t1℃,析出甲的质量一定比析出乙的质量大 C、t2℃时,甲的饱和溶液中溶质与溶液的质量比为1∶2 D、甲中混有少量乙时,可以采用冷却热的饱和溶液的方法提纯甲13. 除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是( )A、CaCO3固体(CaO)——高温煅烧 B、CO2气体(CO)——点燃气体 C、FeCl2溶液(CuCl2)——加入过量的铁粉,充分反应后过滤 D、KCl固体(KClO3)——加入少量的二氧化锰,加热14. 根据如下微观示意图分析,下列结论正确的是( )
A、甲的溶解度比乙小 B、将等质量甲、乙的两种溶液分别由t2℃降温至 t1℃,析出甲的质量一定比析出乙的质量大 C、t2℃时,甲的饱和溶液中溶质与溶液的质量比为1∶2 D、甲中混有少量乙时,可以采用冷却热的饱和溶液的方法提纯甲13. 除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是( )A、CaCO3固体(CaO)——高温煅烧 B、CO2气体(CO)——点燃气体 C、FeCl2溶液(CuCl2)——加入过量的铁粉,充分反应后过滤 D、KCl固体(KClO3)——加入少量的二氧化锰,加热14. 根据如下微观示意图分析,下列结论正确的是( ) A、该反应属于置换反应 B、该反应前后各元素化合价不变 C、该反应生成的丙与丁的质量比为27∶44 D、参加反应的甲与乙的分子个数比为1∶115. 某化学实验小组将一定浓度的稀盐酸、稀硫酸分别加入装有等质量CaCO3粉末的容器中,相同条件下测得两者产生的CO2体积(V)与反应时间(t)的关系如下图所示。下列判断不正确的是( )
A、该反应属于置换反应 B、该反应前后各元素化合价不变 C、该反应生成的丙与丁的质量比为27∶44 D、参加反应的甲与乙的分子个数比为1∶115. 某化学实验小组将一定浓度的稀盐酸、稀硫酸分别加入装有等质量CaCO3粉末的容器中,相同条件下测得两者产生的CO2体积(V)与反应时间(t)的关系如下图所示。下列判断不正确的是( ) A、0~300s内,两个容器中酸的含量均越来越少 B、0~100s内,反应I、Ⅱ生成CO2的速率均先慢后快 C、反应I、Ⅱ最终产生的CO2的体积均大于10a mL D、反应Ⅱ中0~100s内产生的CO2比100~200s内少5a mL
A、0~300s内,两个容器中酸的含量均越来越少 B、0~100s内,反应I、Ⅱ生成CO2的速率均先慢后快 C、反应I、Ⅱ最终产生的CO2的体积均大于10a mL D、反应Ⅱ中0~100s内产生的CO2比100~200s内少5a mL二、综合题
-
16. 请根据下列装置图,回答有关问题。

 (1)、写出下列仪器的名称:a。(2)、若用大理石和稀盐酸制取二氧化碳,并能随时控制反应的发生和停止,应选用的发生装置是(填写字母);若用H装置收集该气体,则气体应从端进入(填写“b”或“c”)。(3)、实验室加热氯酸钾和二氧化锰固体制取较纯净的氧气,选用的制取装置是(填写字母),写出该反应的化学方程式。(4)、若实验室用6.5g锌与足量的稀硫酸反应,可制得氢气的质量是多少?(利用化学方程式进行计算,写出计算过程)17. 水和溶液在生产生活中有着广泛的应用。(1)、机场、车站等公共场所设有许多直饮水机,其处理水的过程如下图所示。
(1)、写出下列仪器的名称:a。(2)、若用大理石和稀盐酸制取二氧化碳,并能随时控制反应的发生和停止,应选用的发生装置是(填写字母);若用H装置收集该气体,则气体应从端进入(填写“b”或“c”)。(3)、实验室加热氯酸钾和二氧化锰固体制取较纯净的氧气,选用的制取装置是(填写字母),写出该反应的化学方程式。(4)、若实验室用6.5g锌与足量的稀硫酸反应,可制得氢气的质量是多少?(利用化学方程式进行计算,写出计算过程)17. 水和溶液在生产生活中有着广泛的应用。(1)、机场、车站等公共场所设有许多直饮水机,其处理水的过程如下图所示。
图中①对应的作用是(填写字母,下同),③对应的作用是。
A、杀菌消毒 B、吸附杂质
(2)、生理盐水是医疗上常用的一种溶液,其溶质是(填写化学式)。一瓶合格的生理盐水密封放置一段时间后,不会出现浑浊现象,原因是。(3)、打开汽水瓶盖时,汽水会自动喷出来,这说明。(4)、下图是利用海水提取粗盐的过程。
根据海水晒盐的原理,下列说法正确的是____(填写字母)。
A、海水进入贮水池,其中氯化钠的质量减少 B、在蒸发池中,海水中氯化钠的质量逐渐增加 C、在蒸发池中,海水中水的质量逐渐减少 D、析出晶体后的母液是氯化钠的饱和溶液(5)、现有一瓶蒸馏水和一瓶稀氯化钾溶液,请设计实验把它们鉴别开,并填写实验报告。实验步骤
实验现象
实验结论
18. 金属材料在生产生活中具有广泛的用途。(1)、铜丝可以用作导线,主要是因为铜具有较好的。(2)、铁制品锈蚀的过程,实际上是铁与空气中的、等发生化学反应的过程。(3)、某电镀厂排放的废液中含有CuSO4、FeSO4和ZnSO4三种溶质,为减少水污染并节约成本,回收硫酸锌、金属铁和铜,设计流程如下图所示:
Ⅰ、写出X的化学式。
Ⅱ、写出操作③中发生反应的化学方程式。
Ⅲ、写出滤液b中含有的阳离子(填写离子符号)。
(4)、将锌粉和镁粉的混合物加入到盛有一定量硝酸银和硝酸铜混合溶液的烧杯中,充分反应后过滤,得到滤渣和蓝色滤液,则滤渣中一定含有(填写化学式,下同),滤液中一定含有的溶质是。(5)、某金属粉末由镁、锌、铝三种组成,取样品2.4g,向其中加入100g稀硫酸,恰好完全反应,生成0.2g氢气,则反应后所得溶液中溶质的质量为g。19. 能源与环境问题日益成为人们关注的焦点。(1)、下列不属于化石燃料的是____(填写字母)。A、煤 B、石油 C、乙醇 D、天然气(2)、煤燃烧时排放出、(均填写化学式)等污染物,这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨。(3)、在汽油中加入适量乙醇作为汽车燃料,可适当节省石油资源,并在一定程度上减少汽车尾气的污染,写出乙醇燃烧的化学方程式。(4)、二氧化碳和一氧化碳均是由碳、氧元素组成的化合物,它们的性质有很大不同的原因是。20. 图中 A~J是初中化学常见的物质,E、F、G、J由一种元素组成,其余均由两种元素组成。其中,常温下A、B均为气体且能产生温室效应,F、I是红色固体。图中“一”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去。 (1)、写出化学式:A , F。(2)、写出 C→D反应的化学方程式:。(3)、写出H与I反应的化学方程式:。(4)、B与E反应是(填写“放热”或“吸热”)反应。21. 某化学兴趣小组的同学探究木炭与氧化铜的反应。(1)、【实验回顾】如图所示装置进行实验,很快发现澄清的石灰水变浑浊,请写出木炭与氧化铜反应的化学方程式。
(1)、写出化学式:A , F。(2)、写出 C→D反应的化学方程式:。(3)、写出H与I反应的化学方程式:。(4)、B与E反应是(填写“放热”或“吸热”)反应。21. 某化学兴趣小组的同学探究木炭与氧化铜的反应。(1)、【实验回顾】如图所示装置进行实验,很快发现澄清的石灰水变浑浊,请写出木炭与氧化铜反应的化学方程式。 (2)、【实验反思】某同学认为当木炭较多、温度较高时,该反应产生的气体中可能含有一氧化碳。
(2)、【实验反思】某同学认为当木炭较多、温度较高时,该反应产生的气体中可能含有一氧化碳。【查阅资料】碱石灰可以吸收二氧化碳和水蒸气。
【实验探究】同学们在老师指导下设计实验进行了验证。
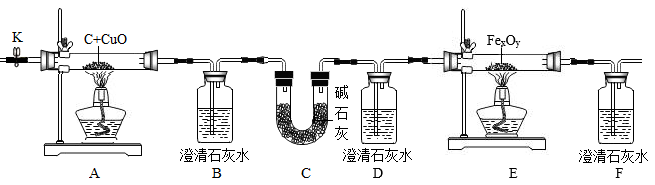
【实验分析】
装置B中澄清石灰水的作用是(用化学方程式表示)。
(3)、实验前,需检查 , 点燃酒精灯前,先打开K,通入一段时间(填写字母)。A、空气 B、氮气 C、一氧化碳 D、二氧化碳
(4)、E装置中,硬质玻璃管和固体药品实验前的总质量为65.8g,当FexOy全部转化为Fe后总质量为64.2g,其中硬质玻璃管的质量为60g,则FexOy中x∶y=(填写最简整数比)。(5)、证明A装置中产物有一氧化碳的现象是。(6)、请指出上述实验设计中的一项缺陷。