广东省广州市黄埔区2021-2022学年九年级上学期末化学试题
试卷更新日期:2022-02-15 类型:期末考试
一、单选题
-
1. 春节是我国最盛大的传统节日。春节活动的内容丰富多彩、形式多样、热闹喜庆。下列活动过程中一定发生化学变化的是( )A、木炭去异味 B、粮食酿酒 C、折剪窗花 D、写春联2. 在测定锌、铟等元素的相对原子质量方面做出卓越贡献的中国科学家是( )A、张青莲 B、杨振宁 C、拉瓦锡 D、屠呦呦3. 锶(Sr)和氧(O)的原子结构示意图如图所示。下列推断正确的是( )
 A、Sr离子核外共有五个电子层 B、O原子在化学反应中易失去6个电子 C、Sr和O可形成化合物SrO D、Sr和O均属于非金属元素4. 金刚石和石墨是常见的碳单质,其结构如图所示。下列说法正确的是( )
A、Sr离子核外共有五个电子层 B、O原子在化学反应中易失去6个电子 C、Sr和O可形成化合物SrO D、Sr和O均属于非金属元素4. 金刚石和石墨是常见的碳单质,其结构如图所示。下列说法正确的是( )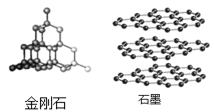 A、构成金刚石和石墨的原子结构不同 B、金刚石和石墨都有吸附性 C、1 g金刚石和1 g石墨所含原子数相同 D、石墨在氧气中能燃烧,但金刚石不能燃烧5. 科研人员制备了一种纳米催化剂,二氧化碳和水在其表面发生反应的微观示意图如图,下列说法正确的是( )
A、构成金刚石和石墨的原子结构不同 B、金刚石和石墨都有吸附性 C、1 g金刚石和1 g石墨所含原子数相同 D、石墨在氧气中能燃烧,但金刚石不能燃烧5. 科研人员制备了一种纳米催化剂,二氧化碳和水在其表面发生反应的微观示意图如图,下列说法正确的是( ) A、两种反应物的分子个数比为1︰1 B、生成物
A、两种反应物的分子个数比为1︰1 B、生成物 的化学式是CH4O
C、催化剂的化学性质在反应前后发生变化
D、该反应中两种生成物的质量比为1:1
6. 宏观辨识与微观探析是化学学科的核心素养之一。下列事实的微观解释正确的是( )A、水在0℃时结冰不能流动——温度降低,分子不再运动 B、干冰升华变成二氧化碳气体——二氧化碳分子变大 C、化学反应前后各物质质量总和不变——反应前后分子的种类、数目、质量均不改变 D、一氧化碳有毒,二氧化碳无毒——不同种分子化学性质不同7. 冬季天气寒冷,流感多发,奥司他韦(C16H28N2O4)可抑制流感病毒在人体内的传播。下列对奥司他韦的说法正确的是( )A、312g奥司他韦中氧元素的质量为16g B、一个奥司他韦分子中含有一个氮分子 C、奥司他韦中碳元素的质量分数最大 D、奥司他韦中C,N元素的质量比为12︰148. 燃料是人类社会重要的能源,下列说法错误的是( )A、汽油中加入适量乙醇作汽车燃料,可以减少尾气污染 B、煤加工成粉末状,可使煤燃烧更充分 C、煤的燃烧可能造成酸雨的原因是排放大量CO2 D、石油炼制可得到石油气、汽油、煤油等产品9. 下列实验操作正确的是( )A、
的化学式是CH4O
C、催化剂的化学性质在反应前后发生变化
D、该反应中两种生成物的质量比为1:1
6. 宏观辨识与微观探析是化学学科的核心素养之一。下列事实的微观解释正确的是( )A、水在0℃时结冰不能流动——温度降低,分子不再运动 B、干冰升华变成二氧化碳气体——二氧化碳分子变大 C、化学反应前后各物质质量总和不变——反应前后分子的种类、数目、质量均不改变 D、一氧化碳有毒,二氧化碳无毒——不同种分子化学性质不同7. 冬季天气寒冷,流感多发,奥司他韦(C16H28N2O4)可抑制流感病毒在人体内的传播。下列对奥司他韦的说法正确的是( )A、312g奥司他韦中氧元素的质量为16g B、一个奥司他韦分子中含有一个氮分子 C、奥司他韦中碳元素的质量分数最大 D、奥司他韦中C,N元素的质量比为12︰148. 燃料是人类社会重要的能源,下列说法错误的是( )A、汽油中加入适量乙醇作汽车燃料,可以减少尾气污染 B、煤加工成粉末状,可使煤燃烧更充分 C、煤的燃烧可能造成酸雨的原因是排放大量CO2 D、石油炼制可得到石油气、汽油、煤油等产品9. 下列实验操作正确的是( )A、 B、
B、 C、
C、 D、
D、 10. 科学研究发现,金星大气的成分之一是三氧化二碳(C2O3),实验证明C2O3的化学性质与CO相似。下列关于C2O3的叙述错误的是( )A、组成:由CO和CO2混合而成 B、用途:可用于冶金工业 C、性质:有可燃性 D、分类:属于非金属氧化物11. 2021世界水日的主题:“Valuing Water”(珍惜水、爱护水);2021中国水周的主题:深入贯彻新发展理念,推进水资源集约安全利用。下列有关水的认识正确的是( )A、农业和园林浇灌改为喷灌、滴灌,可节约用水 B、除去水中含有的少量泥沙,过滤时用玻璃棒搅拌可以加快过滤速度 C、为了保护水资源,禁止使用化肥和农药 D、净化水的方法有沉淀、过滤、吸附、蒸馏、加肥皂水等12. 空气是一种重要的资源。下列有关空气的说法正确的是( )A、洁净的空气属于纯净物 B、碳循环对维持自然界中物质、能量及生态的平衡有重要意义 C、空气质量指数越高,空气质量越好 D、红磷在空气中不能燃烧13. 归纳总结是学习化学的基本方法,下面是某同学整理的部分化学知识。其中你认为都正确的是( )
10. 科学研究发现,金星大气的成分之一是三氧化二碳(C2O3),实验证明C2O3的化学性质与CO相似。下列关于C2O3的叙述错误的是( )A、组成:由CO和CO2混合而成 B、用途:可用于冶金工业 C、性质:有可燃性 D、分类:属于非金属氧化物11. 2021世界水日的主题:“Valuing Water”(珍惜水、爱护水);2021中国水周的主题:深入贯彻新发展理念,推进水资源集约安全利用。下列有关水的认识正确的是( )A、农业和园林浇灌改为喷灌、滴灌,可节约用水 B、除去水中含有的少量泥沙,过滤时用玻璃棒搅拌可以加快过滤速度 C、为了保护水资源,禁止使用化肥和农药 D、净化水的方法有沉淀、过滤、吸附、蒸馏、加肥皂水等12. 空气是一种重要的资源。下列有关空气的说法正确的是( )A、洁净的空气属于纯净物 B、碳循环对维持自然界中物质、能量及生态的平衡有重要意义 C、空气质量指数越高,空气质量越好 D、红磷在空气中不能燃烧13. 归纳总结是学习化学的基本方法,下面是某同学整理的部分化学知识。其中你认为都正确的是( )A.认识微观粒子
①氯化钠是由钠离子和氯离子构成
②分子可分,原子不可分
B.化学与环境
①焚烧植物秸杆以利于耕作
②SO2、NO2是造成酸雨的元凶
C.化学与安全
①夜间发现煤气泄漏开灯寻找泄漏源
②进入深山洞前,先做灯火试验
D.化学与生活
①生活中常用加热煮沸的方法软化硬水
②炒菜时燃气灶火焰呈黄色,锅底出现黑色物质,可调大燃气灶的进风口
A、A B、B C、C D、D14. 下列实验中,现象正确且可得到相应结论的是( )实验操作
现象
结论
A
点燃某液体,在火焰上罩一个内壁沾有澄清石灰水的烧杯
烧杯内壁澄清石灰水变浑浊
该液体为酒精
B
用拇指堵住收集了CH4的试管口,靠近火焰,移开大拇指
发出尖锐爆鸣声
试管中CH4不纯
C
将CO 通入灼热的CuO 粉末中
黑色粉末变为红色
可利用 CO 的可燃性来炼铜
D
称量镁条在空气中燃烧前后质量
质量减少
不遵循质量守恒定律
A、A B、B C、C D、D二、填空题
-
15. 化学与生活、生产、科技发展息息相关。(1)、硅酸钠(Na2SiO3)可用作黏合剂和防火材料,其中Si元素的化合价为。(2)、汽车是重要的交通工具,为了降低污染可以使用电动车,请完成铅酸电池充电反应的方程式:2PbSO4 + 2H2OPb + 2H2SO4 +。(3)、2020年12月3日,我国“嫦娥五号”成功发射,显示我国科技实力的飞速发展。我国空间站“天宫”内的“空气”与地球上的空气组成基本一致,已知同温同压下,相同体积的气体含有相同数目的分子,“空气”中O2与N2的分子个数比约为。(4)、Cu能与空气中的、(写出其中两种物质的化学式)发生化合反应生成“铜锈”[主要成分为Cu2(OH)2CO3]。(5)、一定条件下,CO2和H2反应生成CH4和H2O,见下图。

①该反应的化学方程式是。
②从微观角度分析,A图中的物质属于混合物的原因是。
③请在B图中将该反应的微观粒子补充完整。
三、科普阅读题
-
16. 阅读下面科普短文,回答问题。
2020年3月8日,面对口罩核心材料熔喷布的需求井喷,国务院国资委指导推动相关中央企业加快生产线建设,为新冠肺炎疫情防控提供保障。熔喷布主要以聚丙烯(C3H6)n为原料,纤维直径可以达到1~5微米,具有独特的毛细结构超细纤维,从而使熔喷布具有很好的过滤性、屏蔽性、绝热性和吸油性,是良好的口罩材料。聚丙烯是丙烯(C3H6)的聚合物。全球丙烯的工业化生产工艺主要有裂解法、催化裂化法(FCC)、甲醇制烯烃(MTO/MTP)、丙烷脱氢(PDH)和烯烃歧化法等。我国和全球丙烯的工业化生产工艺方法及份额分别如图1、图2所示:

中国丙烯产能扩张速度稳定,未来产能增量以PDH为主、因PDH的主要成本来自于原料丙烷,丙烷价格越低麇,项目盈利越可观。因此丙烯作为化工领域中重要的基础原料产品,合理布局及发展烯烃产业结构尤为重要。
据文章内容,回答下列问题:
(1)、口罩的核心材料熔喷布主要以为原料,熔喷布是良好的口罩材料,是因为它具有很好的、等优点(任写两点)。(2)、写出丙烯在空气中完全燃烧的化学方程式。(3)、我国生产丙烯份额最多的方法是。由图2可知2015-2025年,全球各地区采用裂解和FCC生产丙烯份额均有下降趋势,而工艺法所产丙烯份额有逐步上升趋势。四、综合题
-
17. 根据所学知识回答:(1)、山西省民兵远程灭火分队在四川凉山执行灭火任务,采用了远程发射灭火弹的方法,灭火弹爆炸后向火中喷洒干粉灭火剂,实现精准灭火作业、喷洒干粉灭火剂能灭火的原因是。为防止火灾发生,游客进入森林旅游时应注意。(2)、如下图所示为制备氧气并探究燃烧条件的实验装置。

①将注射器中的溶液缓缓推入v形管以制备氧气,反应的化学方程式为。
②用80℃的热水同时加热盛有红磷和白磷的w形管时,发现白磷燃烧而红磷不燃烧,由此可说明燃烧需要的条件是。
③白磷燃烧过程中最右侧v形管中液面的变化情况为。
18. 利用如图装置进行气体的制取和性质实验,请回答: (1)、装置B中仪器a的名称是。检查装置B气密性的方法是夹紧止水夹, , 则表明装置气密性良好。(2)、实验室用装置A加热固体混合物制备氧气,反应的化学方程式为。实验结束后,试管炸裂,可能的原因是。(3)、实验室可选用C装置(多孔隔板用来放块状固体)制取二氧化碳,该装置的优点是。(4)、D装置可用于气体的收集、检验、除杂等,该装置能完成的实验是____(填序号)。A、收集氧气,气体从b端通入,将带火星木条放在c端管口进行验满 B、瓶内装有澄清石灰水,气体从b端通入,检验氧气中是否混有二氧化碳 C、瓶内装有水,气体从b端通入,除去一氧化碳中混有的二氧化碳 D、瓶内装满水,在c端接量筒,气体从b端通入,测量氧气的体积(5)、利用E图装置进行所示实验来验证二氧化碳的性质,c、e为喷水的石蕊试纸,d为干燥石蕊试纸。
(1)、装置B中仪器a的名称是。检查装置B气密性的方法是夹紧止水夹, , 则表明装置气密性良好。(2)、实验室用装置A加热固体混合物制备氧气,反应的化学方程式为。实验结束后,试管炸裂,可能的原因是。(3)、实验室可选用C装置(多孔隔板用来放块状固体)制取二氧化碳,该装置的优点是。(4)、D装置可用于气体的收集、检验、除杂等,该装置能完成的实验是____(填序号)。A、收集氧气,气体从b端通入,将带火星木条放在c端管口进行验满 B、瓶内装有澄清石灰水,气体从b端通入,检验氧气中是否混有二氧化碳 C、瓶内装有水,气体从b端通入,除去一氧化碳中混有的二氧化碳 D、瓶内装满水,在c端接量筒,气体从b端通入,测量氧气的体积(5)、利用E图装置进行所示实验来验证二氧化碳的性质,c、e为喷水的石蕊试纸,d为干燥石蕊试纸。①塑料瓶中发生反应的化学方程式为。
②能说明CO2的密度大于空气的实验现象是(写出两种);。
19. 新型材料纳米铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备的主要流程如下图所示: (1)、纳米级Fe粉在氧气中能容易燃烧生成黑色固体,此黑色固体的化学式为。(2)、在制备纳米级Fe粉的工艺流程中,N2不参与反应,根据N2的化学性质,推测流程中N2的作用是。(3)、上述制备纳米级铁粉的化学方程式是。(4)、纳米铁粉能吸附水中的某些污染物,吸附后经沉降、(填操作名称)可除去污染物。(5)、该流程中,12.7kg氯化亚铁固体理论上能制得纳米级Fe粉的质量是kg。20. 硬水加热时易产生水垢,很多工业用水需要对硬水进行软化处理。小组同学利用1.5%的肥皂水比较水的硬度。
(1)、纳米级Fe粉在氧气中能容易燃烧生成黑色固体,此黑色固体的化学式为。(2)、在制备纳米级Fe粉的工艺流程中,N2不参与反应,根据N2的化学性质,推测流程中N2的作用是。(3)、上述制备纳米级铁粉的化学方程式是。(4)、纳米铁粉能吸附水中的某些污染物,吸附后经沉降、(填操作名称)可除去污染物。(5)、该流程中,12.7kg氯化亚铁固体理论上能制得纳米级Fe粉的质量是kg。20. 硬水加热时易产生水垢,很多工业用水需要对硬水进行软化处理。小组同学利用1.5%的肥皂水比较水的硬度。(查阅资料)硬水含较多可溶性钙、镁化合物;软水不含或含较少可溶性钙,镁化合物。
(1)、Ⅰ、探究水的硬度、肥皂水的用量与产生泡沫量的关系(进行实验)向蒸馏水中加入CaCl2和MgCl2的混合溶液,配制两种不问硬度的硬水。
用蒸馏水和两种硬水完成三组实验,记录如下:
组别
第1组
第2组
第3组
实验操作


实验序号
①
②
③
④
⑤
⑥
⑦
⑧
⑨
混合溶液用量/滴
0
0
0
1
x
1
2
2
2
肥皂水用量/滴
5
10
20
5
10
20
5
10
20
产生泡沫量
少
多
很多
无
少
多
无
无
少
(解释与结论)
对比②和⑧可知,肥皂水能区分软水和硬水,依据的现象是。
(2)、设计第2组实验时,为控制水的硬度相同,⑤中x应为。(3)、第2组实验的目的是。(4)、由上述三组实验得到的结论是。(5)、Ⅱ、比较不同水样的硬度(进行实验)用四种水样完成实验,记录观察到泡沫产生时所需肥皂水的用量。
实验操作
水样
肥皂水用量/滴

市售纯净水
2
煮沸后的自来水
6
自来水
9
湖水
14
(解释与结论)
硬度最大的水样是。
(6)、由上述实验可知,能将自来水硬度降低的方法有。(7)、继续实验,发现山泉水的硬度大于自来水的硬度,其实验方案为。
-
-