山东省泰安市高新区2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-02-13 类型:期末考试
一、单选题
-
1. 餐桌上饮品丰富,下列饮品中属于溶液的是( )A、玉米糊 B、豆浆 C、可乐 D、牛奶2. 人人都应践行“绿水青山就是金山银山”的理念,下列说法不符合该理念的是( )A、保护金属资源,提倡合理开发 B、化石燃料取之不尽,提倡大量使用 C、为了使天空更蓝,提倡植树造林 D、倡导“低碳”生活,提倡纸张双面使用3. 下列关于溶液的说法正确的是( )A、溶液都是无色的 B、溶液加水稀释前后溶质的质量不变 C、只有固体和液体可以作为溶质 D、均一、稳定的液体一定是溶液4. 下列物质中,不是合金的是( )A、生铁 B、铁锈 C、黄铜 D、不锈钢5. 若要研究温度对蔗糖溶解快慢的影响,应对比( )
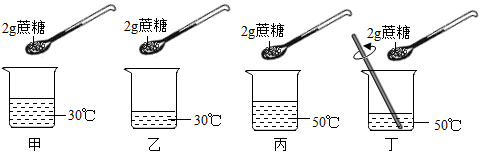 A、甲和乙 B、乙和丙 C、甲和丙 D、丙和丁6. 生理盐水是医疗上常用的一种溶液。下列关于生理盐水的说法中,错误的是( )A、生理盐水的溶剂是水 B、生理盐水中存在的微粒有水分子和氯化钠分子 C、生理盐水是一种混合物 D、各部分一样咸体现了溶液成分的均一性7. 对于30%的KNO3溶液,下列说法正确的是( )A、溶液中溶质和溶剂的质量比为3:10 B、每100g水中溶解30gKNO3 C、某种条件下,可转化为悬浊液 D、若再加30g硝酸钾,则变为60%KNO3溶液8. 酒石酸(C4H6O6)是葡萄酒中主要的有机酸之一,在水溶液中可以电离出H+ , 从而呈现酸性,主要用于饮料添加剂或药物工业原料,下列物质不能与酒石酸反应的是( )A、CO2 B、CuO C、NaOH D、Mg9. 下列常见物质中,碱性最强的是( )
A、甲和乙 B、乙和丙 C、甲和丙 D、丙和丁6. 生理盐水是医疗上常用的一种溶液。下列关于生理盐水的说法中,错误的是( )A、生理盐水的溶剂是水 B、生理盐水中存在的微粒有水分子和氯化钠分子 C、生理盐水是一种混合物 D、各部分一样咸体现了溶液成分的均一性7. 对于30%的KNO3溶液,下列说法正确的是( )A、溶液中溶质和溶剂的质量比为3:10 B、每100g水中溶解30gKNO3 C、某种条件下,可转化为悬浊液 D、若再加30g硝酸钾,则变为60%KNO3溶液8. 酒石酸(C4H6O6)是葡萄酒中主要的有机酸之一,在水溶液中可以电离出H+ , 从而呈现酸性,主要用于饮料添加剂或药物工业原料,下列物质不能与酒石酸反应的是( )A、CO2 B、CuO C、NaOH D、Mg9. 下列常见物质中,碱性最强的是( )物质
橘子汁
西瓜汁
鸡蛋清
肥皂水
pH
3~4
6~7
7~8
9~10
A、橘子汁 B、西瓜汁 C、鸡蛋清 D、肥皂水10. 取少量氧化铜粉末装入试管中,向试管中加入约2mL稀硫酸,振荡。再加热试管,直到氧化铜完全反应。下列说法错误的是( )A、氧化铜粉末是黑色固体,盛放在广口瓶中 B、充分反应后溶液变为黄色 C、振荡的目的是使氧化铜和稀硫酸充分反应 D、加热能加快化学反应的速率11. 推理是学习化学常用的思维方法,下列推理正确的是( )A、活泼金属与酸反应有气体产生,则与酸反应产生气体的一定是活泼金属 B、酸溶液能使紫色石蕊溶液变红,所以能使紫色石蕊变红的溶液一定是酸溶液 C、中和反应生成盐和水,但生成盐和水的反应不一定是中和反应 D、溶液一定是混合物,所以混合物一定是溶液12. 将36.5克10%稀盐酸和4克10%氢氧化钠溶液混合,反应后滴加紫色石蕊颜色变成( )A、红色 B、蓝色 C、无色 D、紫色13. 海水中含量最高的元素是( )A、H B、O C、Na D、Cl14. 草木灰的主要成分是碳酸钾,其性质与碳酸钠相似,下列关于碳酸钾的说法中,正确的是( )A、碳酸钾的化学式为KCO3 B、碳酸钾水溶液中加入无色酚酞试液,溶液仍然为无色 C、向碳酸钾溶液中加入氯化钙不会发生化学反应 D、向稀盐酸中加入碳酸钾会产生气泡15. 甲、乙两种固体的溶解度曲线如图所示。将①②两支试管中的甲、乙饱和溶液(均有少量未溶解的固体)放进盛有热水的烧杯里,升高温度后,下列有关说法正确的是() A、甲的溶解度大于乙的溶解度 B、①②两溶液均变为不饱和溶液 C、①溶液质量增加,②溶液质量减少 D、①溶液中溶质的质量分数一定大于②溶液16. 下列物质不能用复分解反应制取的是A、Fe B、CaSO4 C、HNO3 D、Ca(OH)217. 下列有关金属材料的说法正确的是( )A、黄铜片比纯铜片硬度小 B、焊锡的熔点比纯锡的熔点低 C、钢的含碳量比生铁的含碳量高 D、沙漠地区的铁制品比沿海地区的铁制品更易被锈蚀18. 下列转化不能通过一步反应实现的是( )A、CuO→Cu(OH)2 B、BaCl2→Ba(NO3)2 C、Cu(OH)2→CuCl2 D、Fe→FeCl219. 在CuSO4和AgNO3的混合液中,加入一定的铁片,充分反应后,试管中仍有部分固体,关于该固体成分的说法错误的是( )A、一定有Ag B、可能有Cu C、可能有Ag D、可能有Fe20. A、B、C三种固体物质的溶解度曲线如图所示,下列说法正确的是( )
A、甲的溶解度大于乙的溶解度 B、①②两溶液均变为不饱和溶液 C、①溶液质量增加,②溶液质量减少 D、①溶液中溶质的质量分数一定大于②溶液16. 下列物质不能用复分解反应制取的是A、Fe B、CaSO4 C、HNO3 D、Ca(OH)217. 下列有关金属材料的说法正确的是( )A、黄铜片比纯铜片硬度小 B、焊锡的熔点比纯锡的熔点低 C、钢的含碳量比生铁的含碳量高 D、沙漠地区的铁制品比沿海地区的铁制品更易被锈蚀18. 下列转化不能通过一步反应实现的是( )A、CuO→Cu(OH)2 B、BaCl2→Ba(NO3)2 C、Cu(OH)2→CuCl2 D、Fe→FeCl219. 在CuSO4和AgNO3的混合液中,加入一定的铁片,充分反应后,试管中仍有部分固体,关于该固体成分的说法错误的是( )A、一定有Ag B、可能有Cu C、可能有Ag D、可能有Fe20. A、B、C三种固体物质的溶解度曲线如图所示,下列说法正确的是( )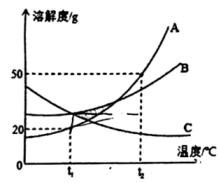 A、阴影区域中,A,C均处于不饱和状态 B、除去A固体中含有的少量C杂质,可采用冷却热饱和溶液的方法提纯A C、将A,B,C三种物质的饱和溶液从t1℃升温到t2℃时,溶质的质量分数大小关系为:A>B>C D、t1℃时,将50g固体A加入到200g水中,所得溶液溶质的质量分数为7%
A、阴影区域中,A,C均处于不饱和状态 B、除去A固体中含有的少量C杂质,可采用冷却热饱和溶液的方法提纯A C、将A,B,C三种物质的饱和溶液从t1℃升温到t2℃时,溶质的质量分数大小关系为:A>B>C D、t1℃时,将50g固体A加入到200g水中,所得溶液溶质的质量分数为7%二、填空题
-
21. 物质的酸碱性与我们的生活密切相关。(1)、酸性是因为物质能电离出离子,可以使紫色石蕊试液变色。(2)、酸碱性强弱可用pH表示,通常洗衣粉、香皂呈碱性,即pH7。自然状态下头皮表面呈弱酸性,有利于头发的生长;所以用洗发水洗发后,最好再使用护发素,使头皮保持弱酸性;由此推测护发素的pH7(选填“>”、“<”、“=”)。22. t1℃时,将等质量的KNO3、KCl分别加入各盛有100g水的甲、乙两只烧杯中,充分搅拌后恢复到t1℃,现象如图I、Ⅱ所示。
 (1)、甲中加入的固体是。(2)、甲中溶液(填“可能”或“一定”)是该溶质的饱和溶液。(3)、若将甲、乙烧杯中溶液的温度从t1℃升高到t2℃,下列有关溶液的分析正确的是(填序号)
(1)、甲中加入的固体是。(2)、甲中溶液(填“可能”或“一定”)是该溶质的饱和溶液。(3)、若将甲、乙烧杯中溶液的温度从t1℃升高到t2℃,下列有关溶液的分析正确的是(填序号)①甲、乙中溶质的质量:甲=乙 ②甲中溶液可能饱和
③乙中溶液一定不饱和 ④甲、乙溶液中溶质质量分数:乙>甲
三、综合题
-
23. 根据“性质决定用途,用途体现性质”回答下列问题:(1)、NaOH可用做某些气体的干燥剂,利用了NaOH的性质是;氢氧化钠溶液敞口放置在空气中应密封保存的原因是(用化学方程式解释)。(2)、碳酸氢钠在医疗上是治疗胃酸过多症的一种药剂,写出反应的化学方程式:。(3)、铝制品具有很好的抗腐蚀性能,其原因是:。(4)、铜可制成导线,主要是利用其有良好的延展性和性。24. 同学们在实验室进行“粗盐中难溶性杂质的去除”实验。
(实验目的)粗盐中难溶性杂质的去除
(实验过程)
①用天平称取5.0g粗盐,加入到盛有150mL水的烧杯里,用玻璃棒搅拌;
②过滤食盐水;
③将所得滤液倒入蒸发皿,加热并用玻璃棒搅拌,当液体蒸干时,停止加热;
④冷却后用玻璃棒把固体转移到纸上,称量,计算所得精盐的产率。
(实验分析)
(1)、步骤①中量取15.0mL正确读数方法:视线与保持水平;为节约能源实验中水的量不宜过多。步骤②得到的液体仍旧浑浊,请分析原因写一种。(2)、如下图所示,步骤③中出现不正确操作,请改正 , 其中玻璃棒的作用是。 (3)、步骤④最终称得固体3.5g,则所得精盐的产率为。某学生在同等实验条件下,所得产品的产量明显比其他同学多,请帮他分析可能的原因。
(3)、步骤④最终称得固体3.5g,则所得精盐的产率为。某学生在同等实验条件下,所得产品的产量明显比其他同学多,请帮他分析可能的原因。A 步骤①中食盐未完全溶解 B.步骤②中有滤渣掉入承接液体的烧杯中
C.步骤③实验过程中有物质溅出 D.步骤④最终所得精盐比较潮湿
25. 某学习小组对铁锈蚀进行探究。(提出问题)铁锈蚀与哪些因素有关?
(查阅资料)
①氯化钙固体可作干燥剂。
②一定条件下,碳可加快铁的锈蚀,但碳本身不参加反应。
(设计与实验)
(1)、实验一:定性探究铁锈蚀的因素取四枚相同的洁净无锈铁钉分别放入试管,进行图实验,现象如表1.
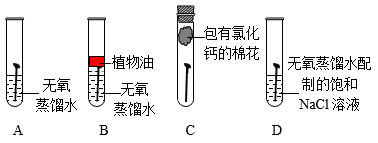
表1
试管
一周后现象
A
铁钉表面有一层铁锈
B
铁钉表面无明显变化
C
铁钉表面无明显变化
D
铁钉表面有较厚铁锈
对比A、B、C试管中实验现象,说明铁锈蚀主要是铁与发生化学反应。
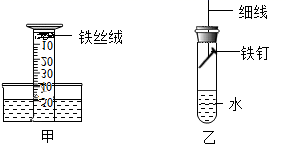
(2)、对比A、D试管中实验现象,说明铁锈蚀还与有关。(3)、铁锈蚀后应及时除锈的原因是。写出用盐酸除铁锈的化学方程式。(4)、实验二:影响铁的锈蚀速度的因素。该小组用图甲装置进行探究铁的锈蚀的实验(量筒内的铁丝绒的量充足),起始时量筒内水面处于50mL刻度处,之后水面缓慢上升。几天后水面最终处于约(填“40”或“10”)mL刻度处。
(5)、小强同学进行如下拓展探究实验:取铁钉用砂纸打磨,称其质量,按图乙安装装置,放置3天,再取出铁钉称量。在不同温度下重复上述实验,得到铁钉质量增加情况如下表。小强同学的实验是探究因素对铁钉锈蚀快慢的影响,结论是。温度/℃
10
20
30
40
50
铁钉质量增加/g
0.02
0.04
0.08
0.16
0.18
四、计算题
-
26. Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组的同学为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
加入稀硫酸的质量(g)
充分反应后剩余固体的质量(g)
第1次
40
m
第2次
40
14.8
第3次
40
12.2
第4次
40
11.2
第5次
40
11.2
试回答下列问题:
(1)、从以上数据可知,表格中,m=。(2)、计算所用稀硫酸中硫酸的质量分数是?