山东省菏泽市鄄城县2021-2022学年九年级上学期期末化学试题
试卷更新日期:2022-02-13 类型:期末考试
一、单选题
-
1. 化学与人类生产、生活密切相关。下列物质的应用涉及化学变化的是( )A、干冰用作人工降雨 B、石墨用作电极 C、液氧用于火箭发射 D、木炭吸附2. 泉城济南,有“四面荷花三面柳,一城山色半城湖”的美誉。保护碧水蓝天,是我们每个公民的责任。下列做法中,不利于环境保护的是( )A、禁止随意焚烧秸杆 B、春节期间尽量不燃放烟花爆竹 C、合理控制化肥和农药的使用 D、生活污水随意排放3. 化学与我们的生活、健康息息相关。下列做法中,合理的是( )A、开发利用新能源:减少化石燃料的使用 B、运输海鲜时用甲醛浸泡保鲜 C、种植蔬菜时喷洒剧毒农药杀虫 D、用发霉的大豆榨油食用4. 化学实验技能是学习化学和实验探究的基础和保证。下列实验操作正确的是( )A、点燃酒精灯
 B、倾倒液体
B、倾倒液体 C、检验装置气密性
C、检验装置气密性 D、给液体加热
D、给液体加热 5. 了解化学安全知识,增强安全防范意识。下列做法不符合安全要求的是( )A、家中天然气泄漏,立即关闭阀门并开窗通风 B、乘坐公交车时,不要携带酒精、汽油等易燃易爆物品 C、炒菜时油锅起火,立即用锅盖盖灭 D、室内用煤炉取暖时为了保暖应封闭严密6. 蛋白质是人类重要的营养物质,它是由多种氨基酸构成的化合物,丙氨酸(图为丙氨酸分子结构模型示意图)是其中的一种。下列有关丙氨酸的叙述正确的是( )
5. 了解化学安全知识,增强安全防范意识。下列做法不符合安全要求的是( )A、家中天然气泄漏,立即关闭阀门并开窗通风 B、乘坐公交车时,不要携带酒精、汽油等易燃易爆物品 C、炒菜时油锅起火,立即用锅盖盖灭 D、室内用煤炉取暖时为了保暖应封闭严密6. 蛋白质是人类重要的营养物质,它是由多种氨基酸构成的化合物,丙氨酸(图为丙氨酸分子结构模型示意图)是其中的一种。下列有关丙氨酸的叙述正确的是( ) A、丙氨酸是由四种原子构成的 B、丙氨酸的化学式为 C、丙氨酸中碳和氮元素质量比为3:1 D、一个丙氨酸分子中含有1个氧分子7. 对下列现象的微观解释正确的是( )A、用水银体温计测量体温——温度升高,分子体积变大 B、湿衣服晾在太阳底下干得快——温度升高,分子运动速率加快 C、氧化汞受热后分解——原子在化学变化中可分 D、氢气和液氢都可以作燃料——物质的所有分子,其化学性质相同8. 在密闭容器中加入甲、乙、丙、丁四种物质,使之充分反应,反应前后测得有关数据如表:
A、丙氨酸是由四种原子构成的 B、丙氨酸的化学式为 C、丙氨酸中碳和氮元素质量比为3:1 D、一个丙氨酸分子中含有1个氧分子7. 对下列现象的微观解释正确的是( )A、用水银体温计测量体温——温度升高,分子体积变大 B、湿衣服晾在太阳底下干得快——温度升高,分子运动速率加快 C、氧化汞受热后分解——原子在化学变化中可分 D、氢气和液氢都可以作燃料——物质的所有分子,其化学性质相同8. 在密闭容器中加入甲、乙、丙、丁四种物质,使之充分反应,反应前后测得有关数据如表:物质
甲
乙
丙
丁
反应前质量g
18
1
2
32
反应后质量g
X·
26
2
12
下列说法中,错误的是( )
A、反应后物质甲的质量为13g B、乙是生成物 C、该反应为分解反应 D、物质丙可能是该反应的催化剂9. 一种新型火箭推进剂在火箭发射过程中,发生发应的微观过程如下图所示。下列说法错误的( ) A、上述四种物质中有两种氧化物 B、氮元素在反应前后化合价一定发生了变化 C、反应生成的丙和丁的质量比为14:9 D、丙和丁分子化学性质不相同10. 类推是学习中常用的思维方法。现有以下类推结果,其中正确的是( )
A、上述四种物质中有两种氧化物 B、氮元素在反应前后化合价一定发生了变化 C、反应生成的丙和丁的质量比为14:9 D、丙和丁分子化学性质不相同10. 类推是学习中常用的思维方法。现有以下类推结果,其中正确的是( )①氧化物一定含有氧元素,所以含有氧元素的化合物定是氧化物;②化学变化一定有新物质生成,有新物质生成的变化一定是化学变化;③分子可以构成物质,物质一定是由分子构成的:④单质和氧气的反应都是化合反应,所以化合反应都是单质和氧气的反应
A、只有① B、只有①②③ C、只有② D、①③④二、填空题
-
11. 用数字和化学用语填空:(1)、保持氧气化学性质的最小微粒。(2)、3个碳酸根离子。(3)、下面是4种粒子的结构示意图:
图中表示粒子共属于种元素,图中表示的阴离子是(用离子符号表示)
 12. 化学就在我们身边,与我们的生活息息相关。请回答以下生活中的问题(1)、黄河是中华文明最主要的发源地,中国人称其为"母亲河"。黄河每年都会生产十七亿吨泥沙,其中有十多亿吨流入大海,某课外活动小组的同学取黄河水样,设计了如下净水方案:
12. 化学就在我们身边,与我们的生活息息相关。请回答以下生活中的问题(1)、黄河是中华文明最主要的发源地,中国人称其为"母亲河"。黄河每年都会生产十七亿吨泥沙,其中有十多亿吨流入大海,某课外活动小组的同学取黄河水样,设计了如下净水方案:
①在操作Ⅱ中,活性炭的作用。
②在操作Ⅲ中,玻璃棒的作用是。
③在操作Ⅳ中,氯气(Cl2)溶于水时,还可与水反应生成盐酸和次氯酸(HClO)试写出该反应的化学方程式。
④为保护黄河水源,下列说法或做法中正确的是(可多选)
A.向黄河中扔秸杆等杂物
B.沿岸居民向黄河内倾倒生活垃圾冲
C.废除黄河两岸生活污水、工业废水排污口,新建污水处理厂
D.全部取缔黄河沿岸的经营性污染场所
(2)、芳芳跟妈妈学炒菜,她先打开了天然气阀门,后打开燃气灶。燃气灶出现“电火花”,天然气燃烧起来。此过程中“电火花”的作用是;炒菜完毕,芳芳关闭燃气管道阀门,使火熄灭,其灭火原理是。13. 近年来,我国航天、航空、高铁等得到长足发展,跻身世界前列。大飞机C919试飞成功,标志着我国航天梦又迈出一大步。大飞机使用的材料如图: (1)、机头外壳用到了钛合金,构成金属钛的粒子是(填“原子”“分子”或“离子”),工业制钛有一种反应为:TiF4+2H2SO44HF+2X+TiO2 , X的化学式为。(2)、机翼和机尾用到了铝合金。铁的强度比铝大,但是制作飞机外壳却不用铁合金,主要原因是铝的密度比铁小且耐腐蚀性强,铝具有很好的抗腐蚀性能的原因是。(3)、小刚查资料发现航母中也用到金属钛,同时还用到锌、铁、铜三种金属。他想探究锌、铁、铜三种金属的活动性强弱,小刚设计了下列实验:向稀盐酸中依次加入足量铁片,充分反应后再加铜片,最后加入锌片。该实验能确定锌的活动性最强的实验现象是。写出实验过程中所发生的所有的化学方程式。
(1)、机头外壳用到了钛合金,构成金属钛的粒子是(填“原子”“分子”或“离子”),工业制钛有一种反应为:TiF4+2H2SO44HF+2X+TiO2 , X的化学式为。(2)、机翼和机尾用到了铝合金。铁的强度比铝大,但是制作飞机外壳却不用铁合金,主要原因是铝的密度比铁小且耐腐蚀性强,铝具有很好的抗腐蚀性能的原因是。(3)、小刚查资料发现航母中也用到金属钛,同时还用到锌、铁、铜三种金属。他想探究锌、铁、铜三种金属的活动性强弱,小刚设计了下列实验:向稀盐酸中依次加入足量铁片,充分反应后再加铜片,最后加入锌片。该实验能确定锌的活动性最强的实验现象是。写出实验过程中所发生的所有的化学方程式。三、综合题
-
14. 在实验桌上有如下几种装置。请你参与实验并回答问题。
 (1)、写出标号①和②的仪器名称:①②。(2)、实验室制取二氧化碳气体的发生装置为(填字母),该反应的化学方程式为。用C装置收集二氧化碳,其验满的方法是:。(3)、检验二氧化碳的方法是。(4)、实验室若用B装置制取氧气的化学方程式为。15. 两位同学帮助老师整理实验室时,在标有“单质”的药柜中发现一瓶失去标签的黑色粉末A,在标有“氧化物”的药柜中发现另一瓶失去标签的黑色粉末B.
(1)、写出标号①和②的仪器名称:①②。(2)、实验室制取二氧化碳气体的发生装置为(填字母),该反应的化学方程式为。用C装置收集二氧化碳,其验满的方法是:。(3)、检验二氧化碳的方法是。(4)、实验室若用B装置制取氧气的化学方程式为。15. 两位同学帮助老师整理实验室时,在标有“单质”的药柜中发现一瓶失去标签的黑色粉末A,在标有“氧化物”的药柜中发现另一瓶失去标签的黑色粉末B.(提出问题)这两瓶黑色粉末A和B分别是什么物质?
(猜想1)甲同学:A是铁粉,B是二氧化锰.
乙同学:A是炭粉,B是氧化铜.
(1)、(实验探究)实验步骤
实验现象
实验结论
①取少量A粉末于试管中,加入适量稀硫酸.
黑色粉末不溶解,没有气体产生.
A粉末一定不是 .
②取少量B粉末于试管中,加入适量稀硫酸.
.
B粉末是氧化铜.
(2)、(反思与拓展)将这两种黑色粉末混合加热(如图),观察到黑色粉末逐渐变为红色,澄清石灰水变浑浊.黑色粉末A和B发生反应的化学方程式为 . 实验结束时,先将导管移出,再熄灭酒精灯的原因是 .
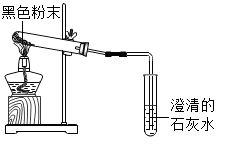
乙同学的猜想正确.
四、计算题
-
16. 为测定某铜、锌合金中铜的质量分数,兴趣小组同学称取10g合金于烧杯中,将40g稀盐酸分四次加入,充分反应,测得实验数据如下表所示:
第一次
第二次
第三次
第四次
加入稀盐酸的质量(g)
10
10
10
10
烧杯中剩余物的质量(g)
19.96
29.92
39.90
49.90
(1)、充分反应后产生气体的总质量g。(2)、该铜、锌合金中铜的质量分数为多少?(写出计算过程)