鲁教版初中化学九年级下册第七单元 常见的酸和碱 单元测试卷
试卷更新日期:2022-02-07 类型:单元试卷
一、单选题
-
1. 下列物质是按照酸、碱、盐顺序排列的是( )A、KNO3、NaOH、HCl B、Ca(OH)2、HCl、NaCl C、H2SO4、Na2CO3、BaSO4 D、HNO3、KOH、CuSO42. 如图所示,U型管内a、b液面相平,当挤压滴管的胶头,试剂X进入锥形瓶内,一段时间后会观察到a液面高于b液面。则试剂X、Y的组合可能是( )
 A、稀盐酸、石灰石 B、水、烧碱 C、稀硫酸、铁粉 D、水、硝酸铵3. 浓硫酸和浓盐酸敞口放置在空气中一段时间后,下列叙述正确的是( )A、质量都增加 B、瓶口都会出现白雾 C、溶质质量分数都减少 D、都没有任何变化4. 食醋里通常含有3%-5%的醋酸(CH3COOH),食醋与鸡蛋壳反应产生能使澄清石灰水变浑浊的气体。下列不能作为醋酸属于酸的证据的是( )A、产生的气体是二氧化碳 B、食醋可以去除金属制品上的的少量锈迹 C、加水稀释食醋,溶液pH变大 D、不宜用铝容器盛装食醋5. 如图所示装置气密性良好、要使注射器中的活塞向右移动,使用的液体M和固体N可能是( )
A、稀盐酸、石灰石 B、水、烧碱 C、稀硫酸、铁粉 D、水、硝酸铵3. 浓硫酸和浓盐酸敞口放置在空气中一段时间后,下列叙述正确的是( )A、质量都增加 B、瓶口都会出现白雾 C、溶质质量分数都减少 D、都没有任何变化4. 食醋里通常含有3%-5%的醋酸(CH3COOH),食醋与鸡蛋壳反应产生能使澄清石灰水变浑浊的气体。下列不能作为醋酸属于酸的证据的是( )A、产生的气体是二氧化碳 B、食醋可以去除金属制品上的的少量锈迹 C、加水稀释食醋,溶液pH变大 D、不宜用铝容器盛装食醋5. 如图所示装置气密性良好、要使注射器中的活塞向右移动,使用的液体M和固体N可能是( )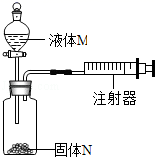
①稀盐酸和石灰石;②稀硫酸和锌;③水和氢氧化钠;④水和硝酸铵.
A、①②③④ B、①②③ C、①②④ D、②③④6. 石蕊、硫酸、氢氧化钙、碳酸钠是常见的四种物质,它们的溶液之间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间反应的主要实验现象,其中描述正确的是( )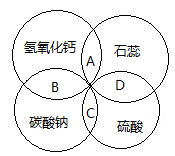 A、石蕊溶液变为红色 B、无明显现象 C、生成无色气体 D、石蕊呈紫色7. 治疗胃酸(主要成分是HCl)过多,可服用含 的药片,制取这类药物不可以使用KOH替代 ,最不科学的理由是( )A、KOH与胃酸不反应 B、KOH易溶于水 C、KOH有强烈的腐蚀性 D、 的来源更广泛8. 下列各图像能正确反映对应变化关系是( )A、向含有少量硫酸的硫酸钠溶液中滴加氯化钡溶液
A、石蕊溶液变为红色 B、无明显现象 C、生成无色气体 D、石蕊呈紫色7. 治疗胃酸(主要成分是HCl)过多,可服用含 的药片,制取这类药物不可以使用KOH替代 ,最不科学的理由是( )A、KOH与胃酸不反应 B、KOH易溶于水 C、KOH有强烈的腐蚀性 D、 的来源更广泛8. 下列各图像能正确反映对应变化关系是( )A、向含有少量硫酸的硫酸钠溶液中滴加氯化钡溶液 B、加水稀释一定量的氢氧化钠溶液
B、加水稀释一定量的氢氧化钠溶液  C、向一定量的氢氧化钡溶液中逐滴加入稀硫酸
C、向一定量的氢氧化钡溶液中逐滴加入稀硫酸  D、高温灼烧一定质量的石灰石
D、高温灼烧一定质量的石灰石  9. 西瓜汁能使石蕊试液变红色,由此可知,西瓜汁显( )A、无法确定 B、碱性 C、中性 D、酸性10. 人体内的一些液体的近似pH如下。下列液体中碱性最强的是( )
9. 西瓜汁能使石蕊试液变红色,由此可知,西瓜汁显( )A、无法确定 B、碱性 C、中性 D、酸性10. 人体内的一些液体的近似pH如下。下列液体中碱性最强的是( )液体
A.胃液
B.胰液
C.胆汁
D.血浆
pH
0.9-1.5
7.5-8.0
7.1-7.3
7.35-7.45
A、A B、B C、C D、D11. 下列实验操作正确的是( )A、点燃酒精灯 B、检查气密性
B、检查气密性  C、滴加液体
C、滴加液体  D、测溶液 pH
D、测溶液 pH  12. 如图是室温下稀盐酸与氢氧化钾溶液反应过程中pH变化的曲线图。下列说法错误的是( )
12. 如图是室温下稀盐酸与氢氧化钾溶液反应过程中pH变化的曲线图。下列说法错误的是( ) A、图中X是稀盐酸 B、c点时,溶液中的K+个数大于Cl-个数 C、b点表示两溶液恰好完全反应 D、滴加方式是将稀盐酸滴入氢氧化钾溶液中
A、图中X是稀盐酸 B、c点时,溶液中的K+个数大于Cl-个数 C、b点表示两溶液恰好完全反应 D、滴加方式是将稀盐酸滴入氢氧化钾溶液中二、填空题
-
13. 如图所示的实验中,A杯溶液逐渐变色;墙角数枝梅,凌寒独自开,遥知不是雪,为有暗香来。”人在远处就能闻到淡淡的梅花香味的原因是冬天暴露在空气中的水管冻裂了,这是因为
 14. 氢氧化钠溶液与盐酸反应的化学方程式为 , 如图是该反应的微观示意图,则该反应前后没有发生变化的离子有 , 从微观角度看,该化学反应的实质是。
14. 氢氧化钠溶液与盐酸反应的化学方程式为 , 如图是该反应的微观示意图,则该反应前后没有发生变化的离子有 , 从微观角度看,该化学反应的实质是。 15. 将氢氧化钠溶液慢慢滴入盛有稀盐酸的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入将氢氧化钠溶液的质量变化曲线如图所示:
15. 将氢氧化钠溶液慢慢滴入盛有稀盐酸的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入将氢氧化钠溶液的质量变化曲线如图所示: (1)、在滴加的过程中,烧杯中溶液的pH如何变化?C点溶液中的溶质是什么?(2)、由图可知,稀盐酸与氢氧化钠溶液发生的反应是吸热反应还是放热反应?
(1)、在滴加的过程中,烧杯中溶液的pH如何变化?C点溶液中的溶质是什么?(2)、由图可知,稀盐酸与氢氧化钠溶液发生的反应是吸热反应还是放热反应?三、综合题
-
16. 酸、碱、盐之间的反应与人们日常生活有着密切的关系。(1)、食醋能作酸味的调味剂,是因为其主要成分醋酸(化学式为CH3OOH)在水溶液中能解离出CH3COO-和(填离子符号)。(2)、胃液分泌过多会引起胃病。服用含有氢氧化铝的药物可缓解病痛,其治疗的化学原理为(用化学方程式表示)。(3)、某同学不小心被黄蜂了(黄蜂毒液呈碱性),为了减轻疼痛可以涂抹下列物质中的(填字母)。
A.食醋(pH=3)
B.浓硫酸
C.食盐水(pH=7)
D.苏打或肥皂水(pH=9~10)
(4)、酿酒厂生产白酒时,常加入适量稀硫酸来控制酸度,发酵完成后进行蒸馏,即可得到白酒,盐酸的价格比硫酸低,同样能控制酸度,请说明控制酸度不用盐酸的原因。17. 对知识的归纳和总结是学好化学的重要方法。在学习了碱的性质后,小丽总结了氢氧化钙的四条化学性质(如图),即氢氧化钙能够与图中四类物质发生化学反应。 (1)、氢氧化钙溶液能使酚酞变 。(2)、为了检验反应③能够发生,你可选择下列哪些物质?A、HCl B、FeCl3 C、CaO D、KOH E、Na2CO3(3)、把石灰乳刷到墙壁上,会发现墙壁变硬“出汗”涉及反应(只需填序号)。18. 构建知识网络模型是化学学习中重要的学习方法。如图1是小明同学利用左手构建的酸的化学性质知识网络(其中A、B表示反应物,C表示生成物)。
(1)、氢氧化钙溶液能使酚酞变 。(2)、为了检验反应③能够发生,你可选择下列哪些物质?A、HCl B、FeCl3 C、CaO D、KOH E、Na2CO3(3)、把石灰乳刷到墙壁上,会发现墙壁变硬“出汗”涉及反应(只需填序号)。18. 构建知识网络模型是化学学习中重要的学习方法。如图1是小明同学利用左手构建的酸的化学性质知识网络(其中A、B表示反应物,C表示生成物)。

请完成下列问题:
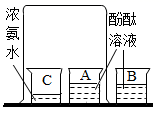
(1)、如用湿润的pH试纸测定盐酸的pH,则结果会(填“偏大”“偏小”或“无影响”)。(2)、图1中①的现象是。(3)、世界卫生组织推广使用中国铁锅,使用铁锅炒菜时,放点食醋可以补充人体中构成血红素的(填“Fe2+”或“Fe3+”),该反应的原理是利用了酸的(填序号“②”“③”“④”或“⑤”)化学性质。(4)、小明用图2来说明稀硫酸与氢氧化钠溶液反应的过程,该过程不发生变化的微粒是(用符号表示),该反应的微观实质可表示为 。依此类推当图1中③是向稀盐酸中滴加硝酸银溶液时,反应的微观实质用同样的方法可表示为。(5)、图1中⑤的性质可用于除铁锈,反应的化学方程式为。(6)、盐酸、硫酸、食醋具有相似化学性质是因为它们水溶液中都含有(用符号表示)。19. 我们接触过的有些化学反应是无明显现象的。下图三组实验都是通过滴加其他试剂的方法,使之产生明显的现象,以证明反应确实发生。请回答下列问题:
 (1)、实验甲中能证明反应发生的现象是溶液由色变为无色,结合图Ⅱ的微观图示,判断图Ⅲ中②代表(填离子符号)。(2)、实验乙中要证明反应的确发生了,应选用的酸碱指示剂是。(3)、小明同学则选用甲反应后的溶液滴入两试管中,观察到先有气泡产生,后有白色沉淀生成。由此既证明了氢氧化钠溶液能与二氧化碳反应,又推断出甲试管反应后溶液中含有的溶质是。(4)、请写出丙试管中生成白色沉淀的化学方程式。
(1)、实验甲中能证明反应发生的现象是溶液由色变为无色,结合图Ⅱ的微观图示,判断图Ⅲ中②代表(填离子符号)。(2)、实验乙中要证明反应的确发生了,应选用的酸碱指示剂是。(3)、小明同学则选用甲反应后的溶液滴入两试管中,观察到先有气泡产生,后有白色沉淀生成。由此既证明了氢氧化钠溶液能与二氧化碳反应,又推断出甲试管反应后溶液中含有的溶质是。(4)、请写出丙试管中生成白色沉淀的化学方程式。四、计算题
-
20. 实验室欲测定一瓶标签 破损的稀硫酸中溶质的质量分数,现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。分析并计算:
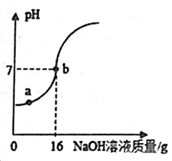 (1)、a点溶液中含有的主要离子是 。(2)、计算稀H2SO4中溶质的质量分数。
(1)、a点溶液中含有的主要离子是 。(2)、计算稀H2SO4中溶质的质量分数。