鲁教版初中化学九年级下册第七单元 第四节 酸碱中和反应
试卷更新日期:2022-02-07 类型:同步测试
一、单选题
-
1. 下列做法不是利用中和反应原理的是( )A、用食醋除去水垢中的氢氧化镁 B、用含碳酸氢钠的发酵粉烘焙糕点 C、用含氢氧化铝的药物治疗胃酸过多 D、用熟石灰处理工厂污水中的硫酸2. 向装有一定量盐酸的密闭隔热容器中,逐滴滴加氢氧化钠溶液,利用数字传感器测出反应时间与溶液温度的变化如图所示。下列说法正确的是( )
 A、由该图像可知该反应先放热后吸热 B、a点所示溶液中,溶质只有NaCl C、b点表示盐酸和氢氧化钠溶液恰好完全反应 D、向70s时的溶液中滴加紫色石蕊溶液,溶液不变色3. 室温下,用数字pH仪连接电脑实时测得稀盐酸和氢氧化钠溶液反应过程中的pH变化曲线如图,下列相关叙述错误的是( )
A、由该图像可知该反应先放热后吸热 B、a点所示溶液中,溶质只有NaCl C、b点表示盐酸和氢氧化钠溶液恰好完全反应 D、向70s时的溶液中滴加紫色石蕊溶液,溶液不变色3. 室温下,用数字pH仪连接电脑实时测得稀盐酸和氢氧化钠溶液反应过程中的pH变化曲线如图,下列相关叙述错误的是( ) A、图中X溶液为氢氧化钠溶液 B、a点溶液能使紫色石蕊溶液变红 C、c点溶液中的溶质是NaCl和NaOH D、b点表示HCl与NaOH等质量反应4. 如图是氢氧化钠与盐酸恰好完全反应的微观示意图,下列结论错误的是( )
A、图中X溶液为氢氧化钠溶液 B、a点溶液能使紫色石蕊溶液变红 C、c点溶液中的溶质是NaCl和NaOH D、b点表示HCl与NaOH等质量反应4. 如图是氢氧化钠与盐酸恰好完全反应的微观示意图,下列结论错误的是( ) A、该反应属于复分解反应 B、反应前后水分子个数不发生变化 C、反应前后所有元素的化合价均无变化 D、该反应的微观实质是H+和OH-结合生成H2O5. 下列能发生中和反应的是( )A、氢氧化钠与二氧化碳 B、石灰水与稀盐酸 C、稀硫酸与氧化铜 D、二氧化碳与氧化钠6. 山药中含有碱性皂角素,有些人皮肤沾上会奇痒难忍,涂抹下列厨房中的某物质能明显缓解不适,该物质是( )A、食醋 B、花生油 C、酱油 D、面粉
A、该反应属于复分解反应 B、反应前后水分子个数不发生变化 C、反应前后所有元素的化合价均无变化 D、该反应的微观实质是H+和OH-结合生成H2O5. 下列能发生中和反应的是( )A、氢氧化钠与二氧化碳 B、石灰水与稀盐酸 C、稀硫酸与氧化铜 D、二氧化碳与氧化钠6. 山药中含有碱性皂角素,有些人皮肤沾上会奇痒难忍,涂抹下列厨房中的某物质能明显缓解不适,该物质是( )A、食醋 B、花生油 C、酱油 D、面粉二、综合题
-
7. 观察下列三幅微观结构示意图,并按要求填空:(1)、图1和图2分别是溴化氢(HBr)和乙醇(C2H5OH)在水中的微观示意图。请你结合已有的酸、碱知识,判断溴化氢的水溶液显(填“酸性”“中性”或“碱性”,下同),乙醇的水溶液显。(2)、图3代表氢氧化钠和盐酸反应的微观过程,由图中可知酸碱中和的实质是和(填离子符号)发生结合。类比写出溴化氢的水溶液和氢氧化钠反应的化学方程式。

 8. 酸、碱、盐在生产、生活中有广泛的应用。(1)、氢氧化钠溶液与稀硫酸反应时,溶液pH变化如图1所示。
8. 酸、碱、盐在生产、生活中有广泛的应用。(1)、氢氧化钠溶液与稀硫酸反应时,溶液pH变化如图1所示。
根据图示判断该实验是将滴入到中。
(2)、测定某酸溶液pH时,如果放pH试纸的玻璃片上的水没有擦干就进行测定,测得的pH(填“偏大”或“偏小”)。(3)、氢氧化镁也是治疗胃酸过多的药物的主要成分,请写出该药品治疗胃酸时发生的化学反应方程式:。三、实验探究题
-
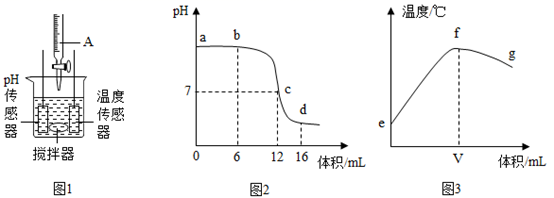
9. 中和反应是一类重要的化学反应。某同学利用图1装置研究稀盐酸与氢氧化钠溶液反应的过程,并用pH和温度传感器测量反应过程中相关物理量的变化情况,得到图2和图3。
 (1)、烧杯中发生反应的化学方程式为。(2)、仪器A中溶液的溶质是(填化学式);(3)、图3中V的数值最接近(填“6”、“12”或“16”);(4)、下列说法错误的是______(填序号)。A、图2中b点所示溶液中的溶质是NaCl和NaOH B、取图2中d点所示溶液加热蒸干所得固体为纯净物 C、图2中c→d所示溶液中NaCl的质量不断增加; D、图3中e→f变化趋势可说明该反应是放热反应(5)、由图4可知,该反应的微观实质是。(6)、若要证明反应已经进行到d点,除了观察pH和温度变化,还可以向反应后的溶液中加入下列物质中的______。(填序号)A、紫色石蕊试液 B、无色酚酞试液 C、镁条 D、碳酸钠 E、硝酸银溶液10. 某化学课堂围绕“酸碱中和反应”,将学生分成若干个小组展开探究。以下是教学片段,请你参加学习并填写空格。
(1)、烧杯中发生反应的化学方程式为。(2)、仪器A中溶液的溶质是(填化学式);(3)、图3中V的数值最接近(填“6”、“12”或“16”);(4)、下列说法错误的是______(填序号)。A、图2中b点所示溶液中的溶质是NaCl和NaOH B、取图2中d点所示溶液加热蒸干所得固体为纯净物 C、图2中c→d所示溶液中NaCl的质量不断增加; D、图3中e→f变化趋势可说明该反应是放热反应(5)、由图4可知,该反应的微观实质是。(6)、若要证明反应已经进行到d点,除了观察pH和温度变化,还可以向反应后的溶液中加入下列物质中的______。(填序号)A、紫色石蕊试液 B、无色酚酞试液 C、镁条 D、碳酸钠 E、硝酸银溶液10. 某化学课堂围绕“酸碱中和反应”,将学生分成若干个小组展开探究。以下是教学片段,请你参加学习并填写空格。(演示实验)将一定质量的稀盐酸加入盛有NaOH溶液的小烧杯中。
(提出问题)实验中未观察到明显现象,某同学提出疑问:反应后溶液中溶质是什么?
(1)、(猜憲与假设)针对疑问,大家纷纷提岀猜想。甲组同学的猜想如下,请补上猜想二、猜想一:只有NaCl 猜想二:
猜想三:NaCl和HCl 猜想四:NaCl、NaOH和HCl
乙组同学认为有一种猜想不合理,不合理的猜想是 , 理由是。
(2)、(实验探究)丙组同学取烧杯中的溶液少许于试管中,滴加几滴CuCl2溶液,(填实验现象),证明溶液中一定没有NaOH。
(3)、为了验证其余猜想,各学习小组利用浇杯中的溶液,并选用了老师提供的pH试纸、K2CO3溶液、AgNO3溶液,进行如下三个方案的探究。实验方案
测溶液的pH
滴加K2CO3溶液
滴加AgNO3溶液
实验操作



实验现象
试纸变色,对照比色卡,pH<7
产生白色沉淀
实验结论
溶液中有HCl
溶液中有HCl
溶液中有HCl
(4)、(得到结论)通过探究,全班同学一致认为猜想正确。(5)、(评价反思)老师对同学们能用多种方法进行探究,并且得出正确结论的活动过程给予肯定,同时指出(2)中存在两处明显不正确。同学们经过反思发现以下两处不正确;①实验操作中的不正确是。
②实验方案中也有一个不正确,错误的原因是。
四、计算题